CR:还有新活儿!武大中南医院团队发现PD-1新机制
来源:奇点糕 2023-11-08 09:35
IL-2或PD-1抑制剂的单独治疗都可取得有限疗效,而当两者联合治疗时,已被证明具有1+1>2的效果。不过,这种协同作用从何而来,还有待探究。
武汉大学中南医院医学研究院的舒红兵、李姝等人的最新研究表明,陷害γc,竟也是免疫抑制因子PD-1的诡计之一。
他们发现,PD-1信号激活会诱导γc失活和泛素化降解,导致肿瘤浸润CD8+T细胞对γc家族细胞因子(如IL-2)介导的免疫激活无法响应。PD-1抑制剂可以恢复γc稳定性和活性,增加CD8+T细胞对IL-2的敏感性,从而被IL-2激活。
这项研究结果,为我们揭示了PD-1抑制剂与IL-2治疗的协同作用的背后机制,文章于今日发表在《细胞研究》期刊上[1]。

论文首页截图
首先,舒红兵和李姝等人利用非小细胞肺癌患者活检样本和小鼠肿瘤模型发现,PD-L1水平与γc水平呈负相关,PD-1抑制剂治疗后γc水平上升。
进一步的体外实验和小鼠实验结果显示,在PD-1/PD-L1信号通路中,PD-1而不是PD-L1介导的信号传导,能够导致T细胞中γc水平下调,从而影响肿瘤浸润CD8+T细胞活化。
随后,研究者们对其机制进行探索。结果发现,在肿瘤微环境中,PD-1通过两种机制抑制γc家族细胞因子触发的信号传导和免疫激活。
一方面,PD-L1/PD-1通路激活后,CD8+T细胞中的蛋白质磷酸酶SHP2被立即招募至PD-1并被激活,进而使γc的Y357位点去磷酸化,导致其失去活性,对γc家族细胞因子失去响应。另一方面,PD-1激活后,转录因子BATF进入细胞核并上调膜相关E3泛素连接酶MARCH5的表达,MARCH5被招募到γc后催化其K315位点发生泛素化,最终导致γc被蛋白酶体降解。
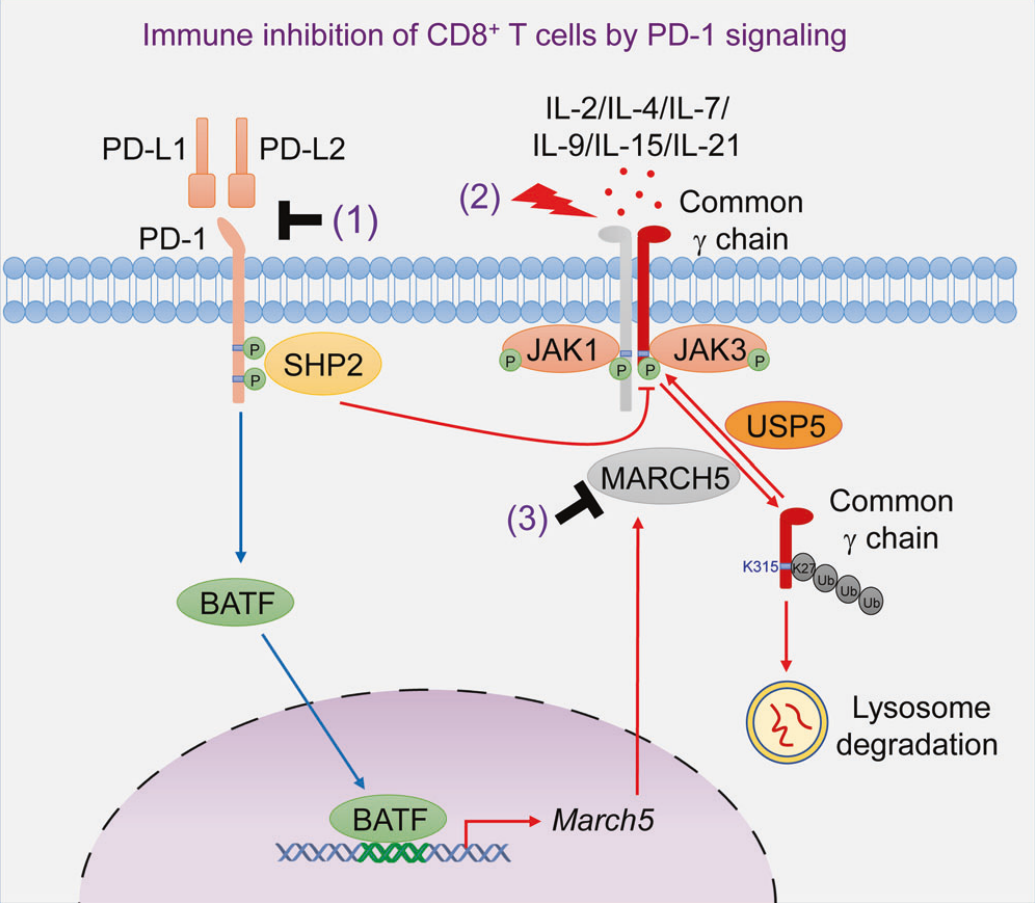
机制图
去泛素化酶USP5可以消除MARCH5诱导的多聚泛素化,过表达USP5能够上调CD8+T细胞中的γc水平。此外,当敲除小鼠全身MARCH5表达时,其各个类型免疫细胞的γc水平也会上调,提高荷瘤小鼠的抗肿瘤免疫力并抑制肿瘤生长。
这些结果表明,MARCH5在PD-1介导的免疫抑制中起重要作用,可作为癌症免疫治疗的潜在靶点。
然而,目前尚未报道MARCH5抑制剂。于是,研究团队在FDA批准的药物中进行筛选,鉴定匹伐他汀钙为最有效的MARCH5特异性抑制剂,在体外实验中提高多种细胞系的γc水平。
匹伐他汀钙具有良好的降胆固醇作用,通过靶向HMG-CoA还原酶来发挥降脂效果。值得注意的是,其它以HMG-CoA还原酶为治疗靶点的他汀类药物如洛伐他汀、辛伐他汀、氟伐他汀钠、瑞舒伐他汀,则对γc水平没有影响。
结直肠癌(MC38)小鼠和黑色素瘤(B16F10)小鼠实验结果显示,匹伐他汀钙单独治疗能够显著抑制肿瘤进展和改善肿瘤微环境,导致免疫细胞的γ水平上调,增强CD8+T细胞的浸润并抑制其耗竭。
当匹伐他汀钙与IL-2和PD-1抑制剂联合治疗时,具有协同效用,与IL-2单独治疗或者IL-2+PD-1抑制剂联合治疗相比抑癌效果更好,抑制肿瘤生长、提高小鼠总生存率。
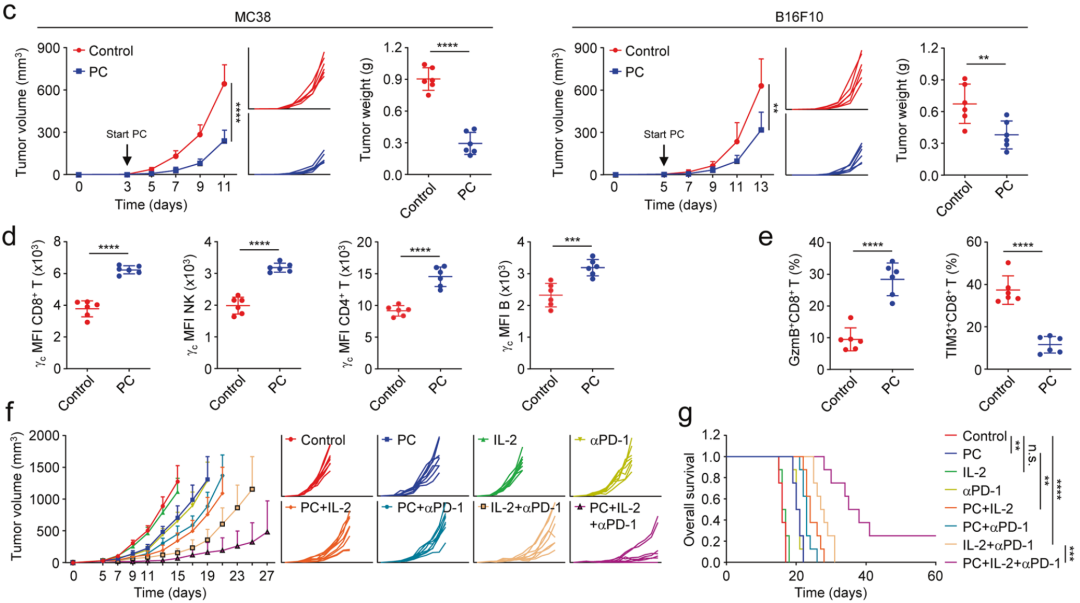
联合治疗效果
细胞因子IL-2具有强大的免疫刺激作用,能够激活细胞毒性T细胞和自然杀伤细胞的活性和增殖,增强它们对肿瘤细胞的攻击能力,因此被用于癌症治疗。PD-1抑制剂则通过阻止PD-1与其配体PD-L1的相互作用,恢复T细胞在肿瘤微环境中的活性,使其能够更有效地识别和摧毁癌细胞。
IL-2或PD-1抑制剂的单独治疗都可取得有限疗效,而当两者联合治疗时,已被证明具有1+1>2的效果。不过,这种协同作用从何而来,还有待探究。
舒红兵、李姝等人完成的这项研究结果,揭示了这种联合治疗的协同效应背后的机制,这对于设计更好的癌症免疫治疗策略至关重要,同时,也为免疫治疗提供了新靶点MARCH5。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


