Nature子刊:东南大学吴富根团队开发基于纳米的原位癌症疫苗,激活全身免疫反应
来源:生物世界 2022-11-21 18:14
在过去的十年中,癌症免疫疗法在癌症治疗中显示出巨大的前景。各种癌症免疫疗法,例如免疫检查点阻断疗法、癌症疫苗、CAR-T疗法等,已被广泛研究并取得了理想的结果。
在过去的十年中,癌症免疫疗法在癌症治疗中显示出巨大的前景。各种癌症免疫疗法,例如免疫检查点阻断疗法、癌症疫苗、CAR-T疗法等,已被广泛研究并取得了理想的结果。
其中,癌症疫苗能引起肿瘤特异性免疫刺激,是最重要的免疫治疗策略之一,在癌症治疗中具有巨大潜力。基于新抗原(Neoantigen)和信使RNA(mRNA)的癌症疫苗在患者中取得了令人鼓舞的结果。
尽管在癌症疫苗的研发上做出了巨大的努力,但目前仍处于癌症预防阶段,在癌症患者中引起大量免疫反应仍然是一个巨大挑战,这主要是由于这些癌症疫苗的免疫原性较弱、免疫抑制肿瘤微环境,以及癌症疫苗中的抗原与特定患者肿瘤之间的地相关性。
为了提高癌症疫苗的治疗效果,自体肿瘤已被用于体外或体内生产癌症疫苗,即所谓的个性化癌症疫苗。基于自体肿瘤细胞的癌症疫苗得益于其肿瘤特异性肿瘤相关抗原(TAA),表现出比传统癌症疫苗更强的免疫反应诱导能力。
然而,体外制备自体肿瘤细胞癌症疫苗存在工艺复杂、收率低、疗效不理想等问题,这限制了自体肿瘤疫苗的临床应用。与之相对,在体内大规模原位生成自体肿瘤细胞癌症疫苗,避免了复杂的体外疫苗制备过程,是生产癌症疫苗的理想选择。
2022年11月1日,东南大学生物科学与医学工程学院吴富根团队在 Nature 子刊 Nature Communications 上发表了题为:In situ generation of micrometer-sized tumor cell-derived vesicles as autologous cancer vaccines for boosting systemic immune responses 的研究论文。
该研究开发了负载了阿霉素(DOX)、酪氨酸激酶抑制剂(TKI)和透明质酸(HA)包被的树枝状聚合物(Dendritic Polymers)组成的纳米颗粒——HDDT纳米颗粒,HDDT纳米颗粒可以将各种癌细胞100%转化为微米尺寸的囊泡(HMVs)。
肿瘤小鼠模型实验显示,HDDT纳米颗粒能够抑制肿瘤生长,诱导强大的免疫原性细胞死亡,并通过原位生产HMVs将原发肿瘤转化为抗原库,作为癌症免疫治疗的个性化癌症疫苗。此外,HDDT纳米颗粒治疗后肿瘤模型小鼠表现出较强的免疫记忆效应,可长期防止肿瘤复发。

在这项研究中,研究团队制作了一系列纳米炸弹(Nanobombs,NBs),包括负载阿霉素(DOX,抗癌药物)和酪氨酸激酶抑制剂(TKI,抗癌药物)和透明质酸(HA,用于肿瘤靶向)包被的树枝状聚合物( Dendritic Polymers),称为HDDT NBs。
研究团队发现,在HDDT NBs处理癌细胞后,几乎所有的细胞(直径10-30微米)都转变为均匀的微米尺寸的囊泡(1.6-3.2微米),细胞到囊泡的转化效率高达100%,也就是所有癌细胞都可以有效地转化为HDDT诱导的微米尺寸的囊泡(HMVs)。
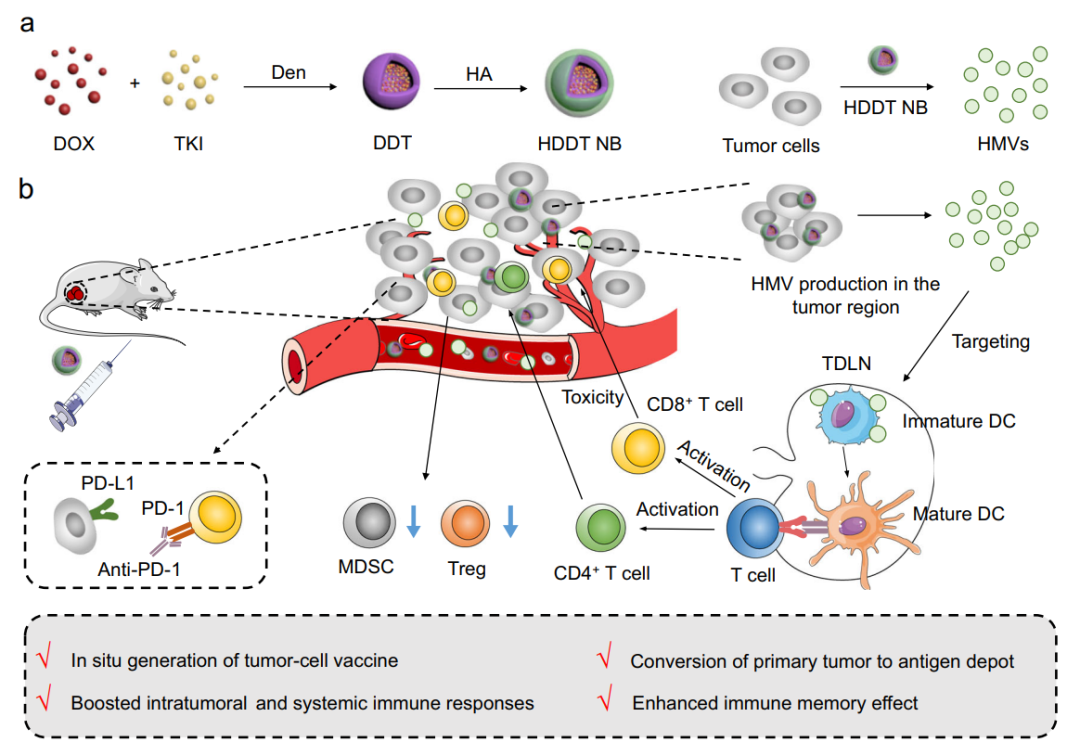
之前的已经报道了几种产生细胞来源的囊泡的策略,但大多数都需要复杂而严格的物理刺激条件(例如挤压、光照、超声、热冲击和冻融等),在体内原位温和的产生癌细胞来源的囊泡非常困难,甚至不可能。
相比之下,该研究开发的基于HDDT NBs的囊泡生成策略,能够诱导癌细胞死亡,实现了癌细胞来源的囊泡的原位大量生成,不需要给予外部刺激,也避免了非原位癌症疫苗所需要的严格存储条件。
进一步研究发现,HDDT NBs在系统给药后,可在肿瘤区域积累,抑制不同肿瘤模型下的肿瘤生长,大规模诱导免疫原性细胞死亡,并在原位产生HMVs,将肿瘤组织转化为抗原库,单独或联合免疫检查点阻断疗法,能够诱导肿瘤内和全身免疫反应,建立强大的免疫记忆效应,治愈小鼠肿瘤,且有效保护不再复发。
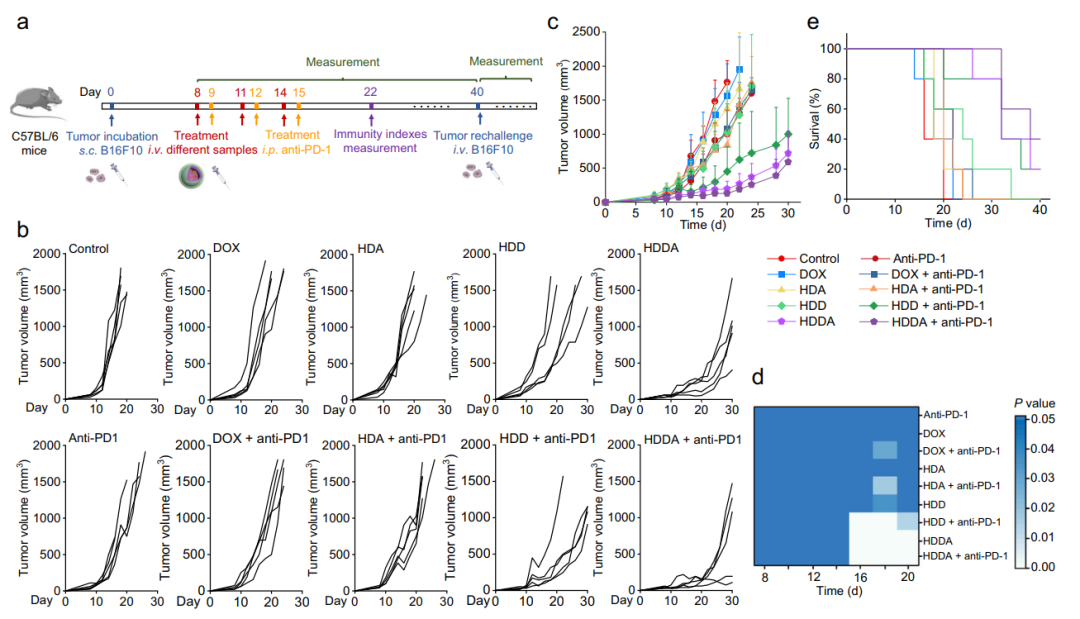
总的来说,该研究开发的HDDT诱导的微米尺寸的囊泡(HMVs),为原位生产自体肿瘤细胞疫苗提供了一个简单而有前途的基于纳米技术的策略,并可能为个性化癌症疫苗的开发提供线索。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


