肌肉干细胞研究新近进展(第4期)
来源:本站原创 2021-03-29 15:23
2021年3月29日讯/生物谷BIOON/---肌肉干细胞可发育分化为成肌细胞(myoblasts),后者可互相融合成为多核的肌纤维,形成骨骼肌最基本的结构。人类胚胎和成人体内都存在肌肉干细胞。胚胎和胎儿的肌肉干细胞增殖使得肌肉组织发展;成年人体内的肌肉干细胞亦被称为卫星细胞,处于休眠状态,沿着肌肉纤维而分布。在经过强烈运动或是受到外界伤害之后,成人的肌肉干
2021年3月29日讯/生物谷BIOON/---肌肉干细胞可发育分化为成肌细胞(myoblasts),后者可互相融合成为多核的肌纤维,形成骨骼肌最基本的结构。
人类胚胎和成人体内都存在肌肉干细胞。胚胎和胎儿的肌肉干细胞增殖使得肌肉组织发展;成年人体内的肌肉干细胞亦被称为卫星细胞,处于休眠状态,沿着肌肉纤维而分布。在经过强烈运动或是受到外界伤害之后,成人的肌肉干细胞会被激活并开始自我增殖,从而增加或是恢复成人的肌肉组织。对于老年人,肌肉干细胞不再具有自我复制的活性,从而表现为肌肉组织的萎缩。
小编针对近年来肌肉干细胞研究取得的进展进行一番盘点,以飨读者。
1.Nature子刊:揭示一种化学物混合物可产生大量的肌肉干细胞
doi:10.1038/s41551-021-00696-y
在一项新的研究中,来自美国加州大学洛杉矶分校的研究人员鉴定出一种化学物混合物,它能够大量地产生可以自我更新并可产生所有类型骨骼肌细胞的肌肉干细胞。这一进展可能导致开发基于干细胞的疗法,以治疗因受伤、年龄或疾病而导致的肌肉损失或损伤。相关研究结果近期发表在Nature Biomedical Engineering期刊上,论文标题为“Skeletal muscle regeneration via the chemical induction and expansion of myogenic stem cells in situ or in vitro”。

图片来自Nature Biomedical Engineering, 2021, doi:10.1038/s41551-021-00696-y。
2.Nat Commun解读!新研究揭示肌肉生长的关键调节因素 有望开发肌肉损伤新疗法!
doi:10.1038/s41467-021-21631-4
当一块肌肉生长时,这块肌肉中的一些干细胞会发育成新的肌肉细胞。这是因为它的主人正在成长或定期锻炼。当受伤的肌肉开始愈合时,也会发生同样的事情。然而与此同时,肌肉干细胞必须产生更多的干细胞,也就是自我更新,否则它们的供给会很快耗尽。这就需要各种参与肌肉生长的细胞相互交流。
在近期一项研究中,Birchmeier和MDC的其他四位科学家与来自日本和法国的研究人员一起发现了第三种蛋白质的关键作用,它与Hes1和MyoD一起,在细胞内形成了一个动态网络。相关研究发表在Nature Communications杂志上,标题为Oscillations of Delta-like1 regulate the balance between differentiation and maintenance of muscle stem cells。
这篇报告中称,这种蛋白质是Notch配体Delta-like1,简称Dll1。“激活的肌肉干细胞以周期性波动的方式产生Dll1,振荡周期持续两到三个小时。每当一部分干细胞表达更多Dll1时,其他细胞中的数量就相应减少。”这种节律性信号决定了干细胞是成为新的干细胞还是发育成肌肉细胞。”Birchmeier解释道。
3.Nature论文解读!发现一种天然蛋白促进肌肉干细胞增殖,可逆转疾病、衰老和创伤造成的严重肌肉萎缩
doi:10.1038/s41586-021-03199-7
当我们撕裂肌肉时,肌肉内的干细胞会进行修复。我们不仅可以看到这种情况发生在严重的肌肉萎缩疾病中,如肌肉萎缩症和在战争中幸存下来的退伍军人的灾难性肢体损伤,而且在我们的日常生活中,当我们拉伤肌肉时,也会发生这种情况。另外,当我们年老体弱时,我们会失去很多肌肉,而我们的干细胞似乎不能像我们年老时一样发挥作用。
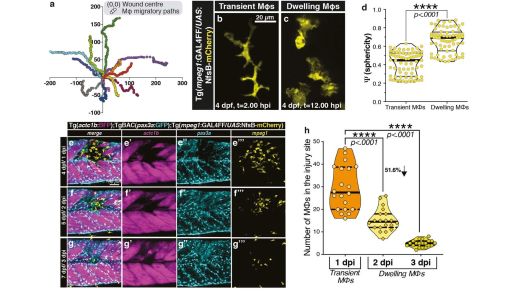
图片来自Nature, 2021, doi:10.1038/s41586-021-03199-7。
4.Front Cell Dev Biol:寡聚DNA促进肌肉分化
doi:10.3389/fcell.2020.616706
成肌细胞是肌肉的祖细胞,在维持肌肉稳态方面起着重要作用。然而,据报道,成肌细胞的分化能力随年龄和疾病而降低,这被认为是肌肉萎缩的原因之一。为了预防或治疗肌肉萎缩症,由信州大学农学部Tomohide Takaya副教授领导的研究小组研究了促进成肌细胞分化的分子。
该研究小组专注于寡核苷酸DNA(短单链DNA),其在体内表现出多种活性。在源自乳杆菌基因组序列的50种寡核苷酸DNA中寻找促进成肌细胞分化的序列的结果,他们发现具有端粒序列的18个碱基的寡DNA对成肌细胞的分化具有极强的诱导作用。这种“成肌寡聚DNA”(myoDN)充当适体,通过形成特征性的三维结构与成肌细胞中的蛋白核仁蛋白结合。结果,发现myoDN通过抑制核仁蛋白功能并最终激活p53信号通路来促进成肌细胞分化。
5.Cell子刊解读!揭秘科学家们如何利用组织干细胞来开发新型靶向性再生医学疗法!
doi:10.1016/j.stem.2020.09.011
干细胞(SCs)能够维持组织稳态并修复创伤,尽管在组织结构和再生需求方面存在一定差异,但干细胞在微环境生境沟通从静态过渡到再生状态方面通常会遵循相似的模式,日前一篇发表在国际杂志Cell Stem Cell上题为“Tissue Stem Cells: Architects of Their Niches”的研究报告中,来自洛克菲勒大学等机构的科学家们通过利用机体中受压力最大的组织中的皮肤上皮组织和骨骼肌组织进行研究强调了干细胞神经成分的相似性和差异性,同时还阐明了干细胞如何介导天然的组织再生并执行损伤所引起的机体的再生行为,此外,研究人员还讨论了在机体老化期间这些通讯网络是如何中断的,以及理解组织中干细胞的特性如何帮助改善再生医学疗法的研究和开发。
文章中,研究人员从:1)皮肤干细胞及其生境;2)静态及与肌肉干细胞生境之间的关联;3)脉管系统在肌肉干细胞生境中的关键角色;4)损伤后的组织修复;5)机体衰老等方面进行了详细阐述;这篇综述文章中,研究人员强调了组织干细胞作为“建筑师”设计并创造自身生境的自我调节角色,这需要精心的设计细胞外基质的结构组分,并将干细胞牢牢锁定到其生境中,合成生长因子和其它细胞类型也参与的细胞因子等;同时还能呈现出接收来自细胞邻居信号的特殊受体,研究者发现了干细胞的显著共性,其在各自的组织再生中的功能并不相同。
6.Nature:谷氨酰胺防止肌肉受伤和衰老
doi:10.1038/s41586-020-2857-9
近日,Massimiliano Mazzone教授(VIB-KU鲁汶癌症生物学中心)领导的团队与Emanuele Berardi博士和Min Shang博士合作,揭示了炎症细胞和肌肉干细胞之间的新的代谢对话。研究人员表明,用GLUD1的抑制剂加强这种代谢串扰可促进谷氨酰胺的释放,并在创伤,局部缺血和衰老等肌肉变性实验模型中改善肌肉再生和身体机能。除了具有转化潜力外,这项工作还在包括肌肉生物学,免疫代谢和干细胞生物学在内的多个研究领域中提供了重要的进展。
Massimiliano Mazzone教授的研究小组观察到,在受损或衰老过程中,肌肉中谷氨酰胺的正常水平由于死去的肌肉组织而降低。研究人员确定了损伤后到达的炎症细胞与驻留的肌肉干细胞之间的代谢对话。这种细胞串扰可重新建立肌肉中谷氨酰胺的原始水平,并在此过程中促使肌肉纤维再生。
7.Cell Stem Cell:深度剖析!科学家开发出首个人类骨骼肌发育的细胞路线图谱!
doi:10.1016/j.stem.2020.04.017
近日,一项刊登在国际杂志Cell Stem Cell上的研究报告中,来自加州大学洛杉矶分校等机构的科学家们通过研究开发出了首个路线图,其能清楚地揭示人类骨骼肌发育的机制,包括肌肉干细胞的形成机制。

图片来源:Broad Stem Cell Research Center。
8.Nature子刊:运动使老鼠的肌肉干细胞返老还童!
doi:10.1038/s42255-020-0190-0
根据斯坦福大学医学院研究人员的一项新研究,每天晚上在转盘上进行短途旅行可以增强年老老鼠的肌肉修复能力。只有年龄较大的老鼠能得到这种益处,研究人员发现这是由于动物肌肉干细胞的再生。
"这对老年动物的影响是非常显着的," 医学博士Thomas Rando说,他是斯坦福大学神经学和神经科学教授,同时也是斯坦福大学格伦衰老生物学中心的主任。"我们发现,有规律的锻炼可以使组织修复恢复年轻。他们的肌肉干细胞的外观和行为开始像那些年轻得多的动物。"
研究人员还发现了一种参与逆转细胞时钟的分子途径。他们认为,控制这一途径的药物可能是运动的有效替代品。Rando是这项研究的资深作者,这项研究于近日发表在Nature Metabolism杂志上。
9.Cell Rep:肌肉干细胞汇编成“地图集”
doi:10.1016/j.celrep.2020.02.067
肌肉修复是一个十分复杂的业务。许多不同类型的细胞不断碰撞,颤抖,并在再生过程中相互协调。
由康奈尔大学Meinig生物医学工程学院助理教授Ben Cosgrove领导的研究人员团队使用了一种新的细胞谱分析技术来探测和分类参与肌肉修复的几乎所有细胞的活性。他们将研究结果整理成肌肉再生的“细胞图册”。该资源提供了组织自我修复中许多错综复杂的细胞相互作用的全面描述,并且可能导致更好的康复策略以及为肌肉损伤中康复患者提供支持。相关结果发表在《Cell Reports》杂志上。
10.Science:全文解读!揭示Pax3 mRNA控制肌肉干细胞命运机制
doi:10.1126/science.aax1694; doi:10.1126/science.aaz4859
组织保持稳态和再生取决于组织特异性的干细胞群体,其中的一些干细胞群体长时间处于静止状态。在脊椎动物中,肌肉干细胞(MuSC)是骨骼肌再生所必需的。近期的研究已表明,久坐不动小鼠中的MuSC对成年肌纤维的维持起着重要的作用,它们对隔膜肌(diaphragm muscle)的贡献较大,而对下后肢肌(lower hindlimb muscle)的贡献较小。
在一项新的研究中,为了理解确定MuSC对成年肌纤维贡献程度的机制,美国斯坦福大学医学院的Thomas Rando及其研究团队测量了MuSC在不同的未遭受损伤的肌肉中激活并进入细胞周期的程度。当在体内用核苷酸类似物5-乙炔基-2'-脱氧尿苷(5-ethynyl-2'-deoxyuridine, EdU)对小鼠进行刺激以标记正在经历DNA复制的细胞后,他们观察到了广泛的EdU掺入。隔膜肌、股薄肌(gracilis)和三头肌(triceps muscle)表现出最高的MuSC数量,它们在稳态条件下自发地打破静止状态并进入细胞周期,而后肢肌(hindlimb muscle)表现出最低的MuSC数量。
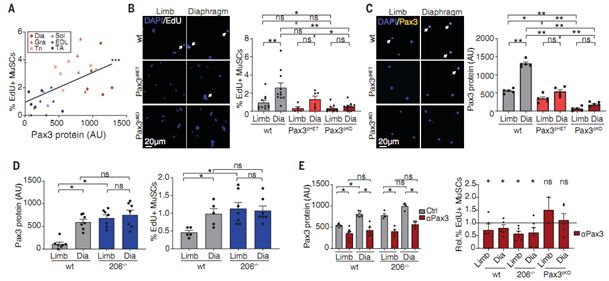
Pax3控制处于稳态条件下的肌肉干细胞激活,图片来自Science, 2019, doi:10.1126/science.aax1694。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


