Nature Cancer:山东大学姜新议/史本康团队开发原位CAR-巨噬细胞疗法,用于肾癌治疗
来源:生物世界 2025-05-03 10:19
这项研究表明,通过合成的 IL-2 受体可以调节 CAR-M 细胞的促炎表型,这有利于 CAR-M 细胞疗法的抗肿瘤免疫治疗,并在其他实体恶性肿瘤中具有广泛的应用前景。
山东大学姜新议教授、史本康教授、荆卫强等人在 Nature 子刊 Nature Cancer 上发表了题为:An in situ engineered chimeric IL-2 receptor potentiates the tumoricidal activity of proinflammatory CAR macrophages in renal cell carcinoma 的研究论文。
该研究开发了一种新型原位 CAR-M 细胞疗法,通过原位工程化的嵌合 IL-2 受体增强 CAR-M 细胞的的肿瘤杀伤活力,用于肾细胞癌的治疗。

在这项最新研究中,研究团队报告了一种原位工程化的嵌合白介素(IL)-2 信号受体(CSR),用于可控地调节嵌合抗原受体巨噬细胞(CAR-M)的促炎表型,增强其持续的抗肿瘤免疫能力。
具体而言,研究团队定制的脂质纳米颗粒(LNP)能够有效地将双环形 RNA 引入巨噬细胞,从而生成具有共刺激信号功能的嵌合抗原受体-巨噬细胞(CAR-M)。CAR-M 的细胞内炎症信号通路可通过合成的 IL-2 受体被 IL-2 治疗剂激活,从而诱导 CAR-M 向抗肿瘤表型转变。在肾癌小鼠模型中,水凝胶介导的 LNP 与 IL-2 的联合治疗可重塑免疫抑制性肿瘤微环境,并促进肿瘤消退。
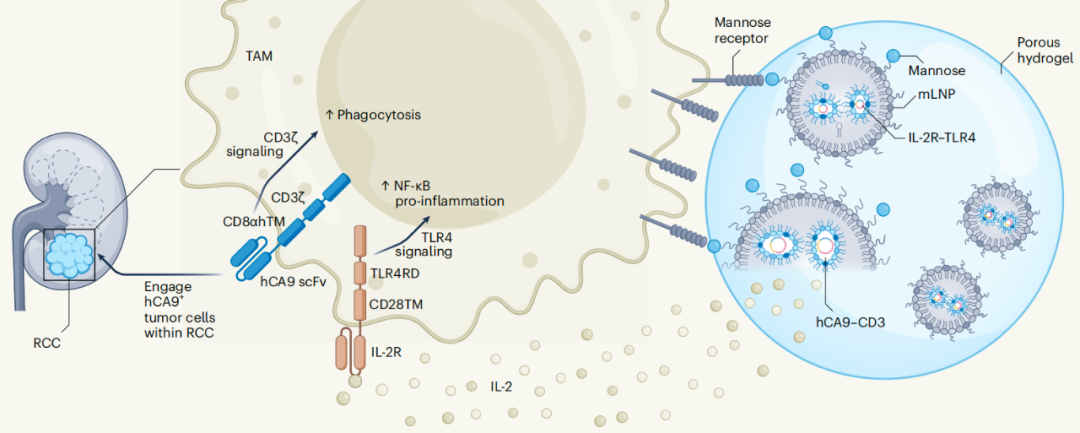
总的来说,这项研究表明,通过合成的 IL-2 受体可以调节 CAR-M 细胞的促炎表型,这有利于 CAR-M 细胞疗法的抗肿瘤免疫治疗,并在其他实体恶性肿瘤中具有广泛的应用前景。
值得一提的是,Nature Cancer 期刊同期配发了题为:In vivo macrophage engineering for renal cancer therapy 的新闻与观点文章。
该文章指出,CAR-巨噬细胞疗法在实体瘤的临床前模型中已展现出良好的活性。姜新议团队将 CAR 技术与脂质纳米颗粒(LNP)相结合以实现体内巨噬细胞工程改造的平台,能够生成具有持续杀伤肿瘤活性的促炎性 CAR-巨噬细胞,成为治疗肾细胞癌的有效疗法。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


