Nature子刊:微生物所刘宏伟/刘双江团队揭示肠道菌群保护心血管健康新机制
来源:中国生物技术网 2022-10-27 09:36
研究揭示了肠道微生物失调,特别是肠道支链氨基酸代谢异常在CVD疾病发生、发展中的关键作用,证明了靶向调控肠道菌群微生态在治疗CVD疾病中的重要潜力,为临床治疗提供了新的思路。
心血管疾病(CVD)严重威胁人类健康,每年在全世界造成约 1700 多万人死亡。动脉粥样硬化(AS)是心血管疾病病理变化的基础,其发病机制复杂,缺乏针对性的治疗药物和手段。人体肠道微生物组学研究发现肠道菌群在 CVD 中发挥关键作用,多种肠道微生物来源的代谢物显示出抗或促 AS 的作用。
微生物所刘宏伟/刘双江团队发现一种真菌活性分子可以显著改善小鼠动脉粥样硬化症状,进一步肠道菌群分析发现口服该分子后,肠道核心细菌粪副拟杆菌 Parabacteroid merdaede丰度上升了420倍。分析一个来自中国的动脉粥样硬化队列和一个欧洲人群CVD队列,科研人员发现肠道粪副拟杆菌丰度与CVD疾病显著负相关。ApoE-/-动脉粥样硬化小鼠定植一株人源粪副拟杆菌后,显著减轻动脉硬化症状,。进一步靶向代谢组分析发现,粪副拟杆菌定植后小鼠粪便支链短链脂肪酸水平显著升高,粪便和血液中支链氨基酸显著降低。血液支链氨基酸水平升高已被证实与胰岛素抵抗、脂肪肝和心血管疾病的发生、发展密切相关。基因组分析和体外发酵实验证实粪副拟杆菌具有将支链氨基酸降解为支链短链脂肪酸的能力。将粪副拟杆菌支链氨基酸分解关键基因porA敲除后,该菌的抗动脉粥样硬化作用消失。研究证实,粪副拟杆菌通过促进肠道支链氨基酸的分解代谢,降低血液支链氨基酸浓度,改善胰岛素抵抗,抑制动脉斑块巨噬细胞mTORC1信号通路激活,发挥抗动脉粥样硬化作用。
长期高脂饮食和高胆固醇饮食可以通过不同的病理机制诱发动脉粥样硬化。研究发现粪副拟杆菌对高脂诱导肥胖伴随胰岛素抵抗的动脉粥样硬化改善效果优于对高胆固醇饮食造成的动脉粥样硬化模型。人群CVD队列进一步分析表明,CVD病人血液支链氨基酸水平显著高于健康人群,肠道菌群porA基因丰度显著低于健康对照人群。研究揭示了肠道微生物失调,特别是肠道支链氨基酸代谢异常在CVD疾病发生、发展中的关键作用,证明了靶向调控肠道菌群微生态在治疗CVD疾病中的重要潜力,为临床治疗提供了新的思路。
相关研究结果已在线发表于国际权威期刊Nature Metabolism,题为“Gut Parabacteroides merdae protects against cardiovascular damage by enhancing branched-chain amino acid catabolism”。Nature Metabolism同期以“A gut bacterium tackles atherosclerosis”为题发表了Herbert Tilg 教授的专题评述“News & Views”。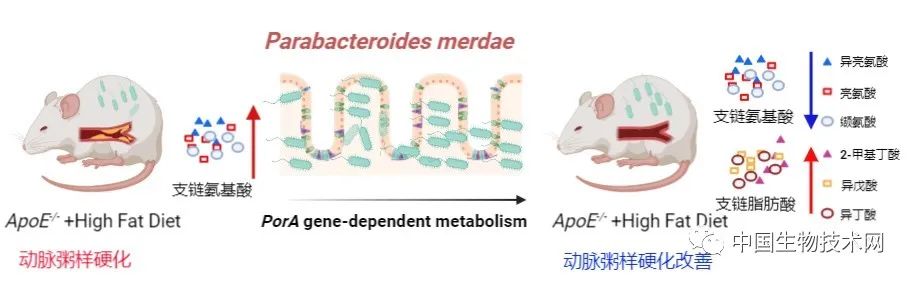
图1. 粪副拟杆菌 Parabacteroid merdaede改善动脉粥样硬化机制
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


