Science:谷氨酰胺阻断药物增强抗肿瘤反应,有望用于CAR-T细胞疗法中
来源:本站原创 2019-11-10 16:29
2019年11月10日讯/生物谷BIOON/---在一项新的研究中,美国约翰霍普金斯大学研究人员发现他们开发出的一种阻断谷氨酰胺代谢的化合物可以延缓肿瘤生长,改变肿瘤微环境,并促进持久性的高活性抗肿瘤T细胞的产生。相关研究结果于2019年11月7日在线发表在Science期刊上,论文标题为“Glutamine blockade induces divergent metabolic program
2019年11月10日讯/生物谷BIOON/---在一项新的研究中,美国约翰霍普金斯大学研究人员发现他们开发出的一种阻断谷氨酰胺代谢的化合物可以延缓肿瘤生长,改变肿瘤微环境,并促进持久性的高活性抗肿瘤T细胞的产生。相关研究结果于2019年11月7日在线发表在Science期刊上,论文标题为“Glutamine blockade induces divergent metabolic programs to overcome tumor immune evasion”。
作为谷氨酰胺拮抗剂DON的一种“前体药物(prodrug)”,这种化合物在体内经过酶促反应后产生它的活性形式(即DON)在肿瘤内发挥作用。论文通讯作者、约翰霍普金斯大学基梅尔癌症中心癌症免疫治疗研究所副所长Jonathan Powell博士说,从理论上讲,鉴于谷氨酰胺在促进肿瘤疯狂生长所需的代谢中发挥的关键作用,这种化合物可能能够用于治疗多种癌症类型。
他们的研究揭示出癌细胞和效应T细胞在提供能量的代谢途径中存在令人吃惊的差异,这些途径之前被认为是非常相似的。Powell说,这些差异可能用作癌症治疗的“代谢检查点(metabolic checkpoint)”。
他说:“通过靶向谷氨酰胺代谢,我们不仅能够抑制肿瘤生长并改变肿瘤微环境,而且还能以一种显著增强癌症免疫疗法的方式改变T细胞。”
Powell说,尽管谷氨酰胺代谢是身体所有细胞所必需的,但是这种DON前体药物选择性地靶向肿瘤细胞,这是因为它们对谷氨酰胺的需求最为迫切。“代谢疗法中出现的这种新情形---对我来说,这就是为什么它令人非常兴奋的原因---是像我们这样的治疗变得有选择性的原因在于它优先影响对谷氨酰胺有最大需求的癌细胞。”
Powell及其同事们在结肠癌、淋巴瘤和黑色素瘤的小鼠模型中测试了一种名为JHU083(也写作JHU-083)的DON前体药物。
Powell说:“一开始,我们的想法是,如果我们可以靶向肿瘤代谢,那么我们就可以实现两个目标:延缓肿瘤生长和改变肿瘤微环境。”肿瘤微环境---肿瘤附近的细胞、血管和营养物---可阻止免疫反应产生,这是因为它通常是酸性、低氧和营养物缺乏的。他说:“从某种意义上说,肿瘤在自身周围产生的这种免疫屏障是肿瘤代谢的直接结果。”
这些研究人员发现在多种不同的小鼠癌症模型中,使用JHU083治疗可通过破坏肿瘤细胞代谢及其对肿瘤微环境的影响,显著降低肿瘤生长,并提高了生存率。在许多小鼠中,仅使用JHU083进行治疗就可导致持久性治愈。这种治愈是由于这种代谢疗法激活的天然抗肿瘤免疫反应所导致的。当向这些因治愈没有癌症的小鼠中重新注入新的肿瘤时,他们发现几乎所有小鼠都对新肿瘤产生免疫排斥,这就提示着JHU083治疗产生了强大的免疫记忆力,从而能够识别和攻击新的癌症。
他们还用JHU083和抗PD-1免疫检查点抑制剂对这些小鼠进行了治疗,其中免疫检查点抑制剂是一类免疫治疗药物,可解除癌细胞对T细胞的抑制。Powell说:“起初,我们认为我们需要依次使用这种两种药物,以避免代谢疗法对免疫疗法的任何潜在影响。但是,值得注意的是,事实证明,当我们同时给予它们时,这种联合治疗的效果最好。”相比于仅使用抗PD-1免疫检查点抑制剂,同时使用这种两种药物可增强它们的抗肿瘤作用。
Powell说:“我们发现JHU083对T细胞产生非常积极的非常直接的作用,我们必须研究其中的原因。”
在分析和比较了接受治疗的肿瘤细胞和一种称为效应T细胞的免疫细胞中的基因表达后,Powell及其同事们注意到这两种细胞中与代谢相关的基因表达存在差异,这使得他们能够猜测这些T细胞为自身提供能量的方式。
这些研究人员发现了一些相似之处,但是从根本上说,肿瘤细胞和效应T细胞的代谢途径是非常不同的,正是基于这些差异,他们才进行谷氨酰胺阻断药物治疗。
这些差异使得效应T细胞能够通过产生持久且高效的肿瘤浸润T细胞来响应谷氨酰胺阻断,这些T细胞在肿瘤微环境中似乎是活跃的而没有发生衰竭。Powell指出:“通过阻断谷氨酰胺代谢,我们让这些细胞更具持久性,更像是一种免疫记忆细胞。”
这些研究人员还证实用JHU083治疗肿瘤可增强过继细胞疗法的疗效。作为一种免疫疗法,过继细胞疗法首先收集T细胞并在实验室中对它们进行大量增殖,然后再将它们移植到患者体内来增强对癌症的免疫反应。这些发现提示着这种新方法也可能用于增强一类有前景的称为CAR-T细胞疗法的过继细胞疗法。在未来的研究中,Powell及其同事们想要研究JHU083如何与不同类型的免疫疗法组合使用,以探究某些肿瘤是否可以克服JHU083产生的代谢陷阱(metabolic trap)。
Powell说,潜在地,产生避免JHU083影响的代谢途径的肿瘤可能会发现它们自己处于“死胡同”中。“通过添加其他的代谢拮抗剂,也有可能清除耐药性肿瘤。”(生物谷 Bioon.com)
参考资料:
1.Robert D. Leone et al. Glutamine blockade induces divergent metabolic programs to overcome tumor immune evasion. Science, 2019, doi:10.1126/science.aav2588.
2.Glutamine-blocking drug slows tumor growth and strengthens anti-tumor response
https://medicalxpress.com/news/2019-11-glutamine-blocking-drug-tumor-growth-anti-tumor.html
3.Revamped cancer drug starves tumors in mice
https://www.sciencemag.org/news/2019/11/revamped-cancer-drug-starves-tumors-mice

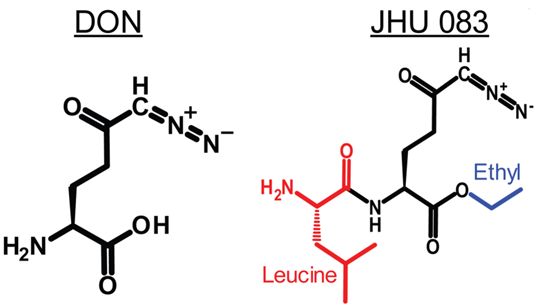
谷氨酰胺拮抗剂DON及其前体药物JHU-083的化学结构,图片来自Translational Oncology, 2019, doi:10.1016/j.tranon.2019.05.013。
作为谷氨酰胺拮抗剂DON的一种“前体药物(prodrug)”,这种化合物在体内经过酶促反应后产生它的活性形式(即DON)在肿瘤内发挥作用。论文通讯作者、约翰霍普金斯大学基梅尔癌症中心癌症免疫治疗研究所副所长Jonathan Powell博士说,从理论上讲,鉴于谷氨酰胺在促进肿瘤疯狂生长所需的代谢中发挥的关键作用,这种化合物可能能够用于治疗多种癌症类型。
他们的研究揭示出癌细胞和效应T细胞在提供能量的代谢途径中存在令人吃惊的差异,这些途径之前被认为是非常相似的。Powell说,这些差异可能用作癌症治疗的“代谢检查点(metabolic checkpoint)”。
他说:“通过靶向谷氨酰胺代谢,我们不仅能够抑制肿瘤生长并改变肿瘤微环境,而且还能以一种显著增强癌症免疫疗法的方式改变T细胞。”
Powell说,尽管谷氨酰胺代谢是身体所有细胞所必需的,但是这种DON前体药物选择性地靶向肿瘤细胞,这是因为它们对谷氨酰胺的需求最为迫切。“代谢疗法中出现的这种新情形---对我来说,这就是为什么它令人非常兴奋的原因---是像我们这样的治疗变得有选择性的原因在于它优先影响对谷氨酰胺有最大需求的癌细胞。”
Powell及其同事们在结肠癌、淋巴瘤和黑色素瘤的小鼠模型中测试了一种名为JHU083(也写作JHU-083)的DON前体药物。
Powell说:“一开始,我们的想法是,如果我们可以靶向肿瘤代谢,那么我们就可以实现两个目标:延缓肿瘤生长和改变肿瘤微环境。”肿瘤微环境---肿瘤附近的细胞、血管和营养物---可阻止免疫反应产生,这是因为它通常是酸性、低氧和营养物缺乏的。他说:“从某种意义上说,肿瘤在自身周围产生的这种免疫屏障是肿瘤代谢的直接结果。”
这些研究人员发现在多种不同的小鼠癌症模型中,使用JHU083治疗可通过破坏肿瘤细胞代谢及其对肿瘤微环境的影响,显著降低肿瘤生长,并提高了生存率。在许多小鼠中,仅使用JHU083进行治疗就可导致持久性治愈。这种治愈是由于这种代谢疗法激活的天然抗肿瘤免疫反应所导致的。当向这些因治愈没有癌症的小鼠中重新注入新的肿瘤时,他们发现几乎所有小鼠都对新肿瘤产生免疫排斥,这就提示着JHU083治疗产生了强大的免疫记忆力,从而能够识别和攻击新的癌症。
他们还用JHU083和抗PD-1免疫检查点抑制剂对这些小鼠进行了治疗,其中免疫检查点抑制剂是一类免疫治疗药物,可解除癌细胞对T细胞的抑制。Powell说:“起初,我们认为我们需要依次使用这种两种药物,以避免代谢疗法对免疫疗法的任何潜在影响。但是,值得注意的是,事实证明,当我们同时给予它们时,这种联合治疗的效果最好。”相比于仅使用抗PD-1免疫检查点抑制剂,同时使用这种两种药物可增强它们的抗肿瘤作用。
Powell说:“我们发现JHU083对T细胞产生非常积极的非常直接的作用,我们必须研究其中的原因。”
在分析和比较了接受治疗的肿瘤细胞和一种称为效应T细胞的免疫细胞中的基因表达后,Powell及其同事们注意到这两种细胞中与代谢相关的基因表达存在差异,这使得他们能够猜测这些T细胞为自身提供能量的方式。
这些研究人员发现了一些相似之处,但是从根本上说,肿瘤细胞和效应T细胞的代谢途径是非常不同的,正是基于这些差异,他们才进行谷氨酰胺阻断药物治疗。
这些差异使得效应T细胞能够通过产生持久且高效的肿瘤浸润T细胞来响应谷氨酰胺阻断,这些T细胞在肿瘤微环境中似乎是活跃的而没有发生衰竭。Powell指出:“通过阻断谷氨酰胺代谢,我们让这些细胞更具持久性,更像是一种免疫记忆细胞。”
这些研究人员还证实用JHU083治疗肿瘤可增强过继细胞疗法的疗效。作为一种免疫疗法,过继细胞疗法首先收集T细胞并在实验室中对它们进行大量增殖,然后再将它们移植到患者体内来增强对癌症的免疫反应。这些发现提示着这种新方法也可能用于增强一类有前景的称为CAR-T细胞疗法的过继细胞疗法。在未来的研究中,Powell及其同事们想要研究JHU083如何与不同类型的免疫疗法组合使用,以探究某些肿瘤是否可以克服JHU083产生的代谢陷阱(metabolic trap)。
Powell说,潜在地,产生避免JHU083影响的代谢途径的肿瘤可能会发现它们自己处于“死胡同”中。“通过添加其他的代谢拮抗剂,也有可能清除耐药性肿瘤。”(生物谷 Bioon.com)
参考资料:
1.Robert D. Leone et al. Glutamine blockade induces divergent metabolic programs to overcome tumor immune evasion. Science, 2019, doi:10.1126/science.aav2588.
2.Glutamine-blocking drug slows tumor growth and strengthens anti-tumor response
https://medicalxpress.com/news/2019-11-glutamine-blocking-drug-tumor-growth-anti-tumor.html
3.Revamped cancer drug starves tumors in mice
https://www.sciencemag.org/news/2019/11/revamped-cancer-drug-starves-tumors-mice
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


