干细胞助力,纳米技术破局!Front Pharmacol:创新性的治疗体系——LNPs@S/T系统,骨关节炎治疗迎来新曙光
来源:生物谷原创 2025-01-02 10:02
该研究成功开发出LNPs@S/T系统,其通过调节胆固醇代谢、招募滑膜间充质干细胞并诱导其分化,有效防止软骨降解、促进基质再生,在骨关节炎大鼠模型中展现出良好治疗效果,为骨关节炎治疗提供了新方向。
在医学研究的前沿领域,骨关节炎(OA)一直是一个亟待攻克的重要课题。作为一种常见的退行性关节疾病,OA让许多患者饱受疼痛和活动受限之苦,也给社会带来了沉重的医疗负担。传统治疗方法如物理治疗、药物治疗或手术干预,大多只能暂时缓解症状,无法逆转软骨的退变进程,更不用说从根本上解决问题了。
然而,最近一项发表于J Nanobiotechnology的研究“Targeted lipid nanoparticles distributed in hydrogel treat osteoarthritis by modulating cholesterol metabolism and promoting endogenous cartilage regeneration”的研究揭示了一个令人振奋的消息:通过调节胆固醇代谢并促进内源性软骨再生,科学家们开发出了一种创新性的治疗体系——LNPs@S/T系统。
想象一下,如果我们能够修复受损的软骨,就像修理一辆磨损的汽车零件一样,那该有多好?研究人员发现,软骨细胞内的胆固醇代谢失衡是导致OA恶化的一个关键因素。具体来说,CH25H-CYP7B1-RORα这一胆固醇代谢轴的异常调控会引发一系列不良连锁反应,导致软骨细胞外基质(ECM)降解加剧,使得软骨变得脆弱易损,最终加速其磨损与破坏。

为了应对这个问题,研究人员设计了一种高度靶向性的脂质纳米颗粒(Lipid Nanoparticles, LNPs),这些纳米颗粒经过特殊修饰后,可以精准地将siRNA递送到炎症软骨细胞中,从而下调关键基因CH25H的表达。
这种精确打击不仅减少了软骨细胞的凋亡和活性氧(Reactive Oxygen Species, ROS)的产生,还上调了Col2A1和SOX9等与软骨基质合成相关的分子表达,抑制了Adamts5、MMP13、MMP9等分解代谢酶的活性。换句话说,这个过程就像是给软骨细胞注入了一剂强心针,帮助它们恢复活力。
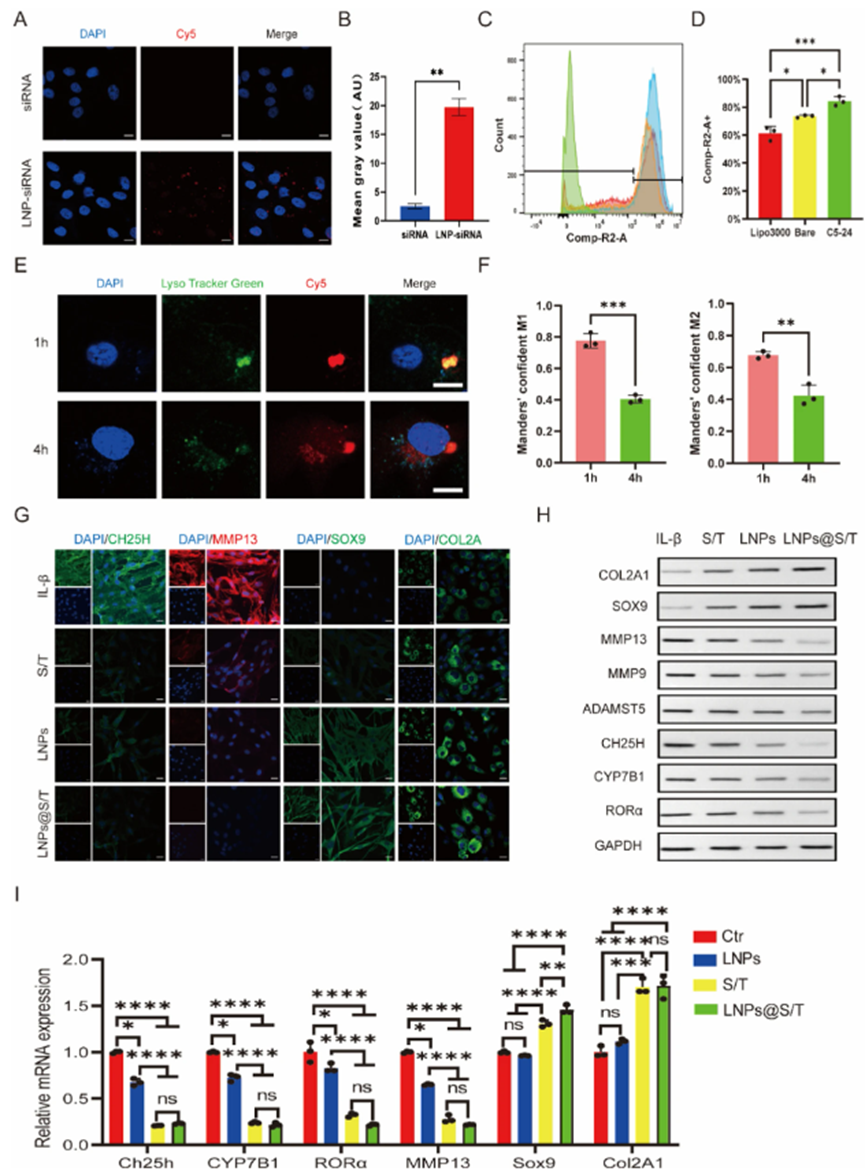
图1. 在大鼠炎症软骨细胞中,siCH25H介导胆固醇代谢调控及对OA软骨退变的缓解作用
但这还不是全部。自组装肽水凝胶也是LNPs@S/T系统的核心组成部分。研究团队合成了特定的肽序列Fmoc-K(Fmoc)SKPPGTSS和Fmoc-LIANAK,并运用溶剂切换技术成功制备出具有优异性能的肽水凝胶。
借助扫描电子显微镜(SEM)、透射电子显微镜(TEM)、圆二色光谱(CD)、傅里叶变换红外光谱(FTIR)和流变学测试等多种先进的表征手段,研究人员全面证实了该水凝胶具有高度有序的纳米纤维结构、良好的生物相容性和适宜的流变学特性。其中,SKPPGTSS肽序列能够有效地招募SMSCs,而LIANAK肽序列则可以有力地促进SMSCs向软骨细胞分化。
在体外实验中,Transwell实验、活/死细胞检测和细胞骨架染色等结果清晰地表明,LNPs@S/T系统能够显著促进SMSCs的迁移、增殖和分化,为软骨修复提供了充足的细胞来源。
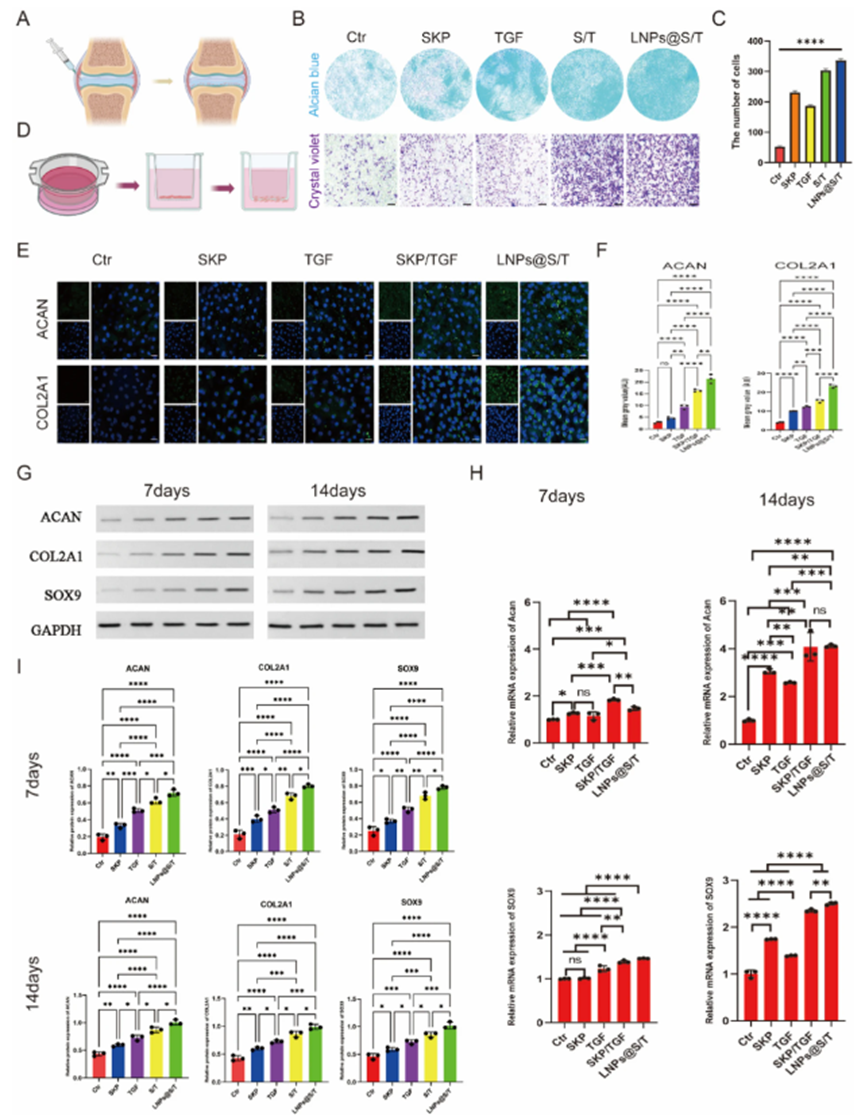
图2. LNP@S/T介导滑膜间充质干细胞(SMSCs)招募诱导及软骨分化促进作用
在体内实验阶段,研究人员使用了OA大鼠模型来验证这一系统的疗效。结果显示,C5-24-LNPs在OA关节中的滞留时间显著延长,确保了药物能在病变部位持续发挥作用。而水凝胶标记的荧光在注射后两周内依然清晰可见,证明了LNPs-siRNA可以在体内实现稳定且持续的释放。
治疗四周后,接受LNPs@S/T治疗的大鼠关节状况明显改善,关节肿胀、炎症、骨赘生长等问题得到了有效缓解。微CT扫描和组织学染色结果进一步证实,软骨完整性得以维持,退变程度显著降低,患者的疼痛症状也大幅减轻。
深入分析表明,LNPs@S/T系统不仅调节了软骨细胞内的胆固醇代谢,还对SMSCs的行为产生了深远影响。mRNA测序显示,与对照组相比,LNPs@S/T处理后的SMSCs中有3774个差异表达基因(Differentially Expressed Genes, DEGs),涉及细胞分化、迁移、增殖等多个生物学过程。此外,在软骨细胞方面,也有5055个DEGs发生了显著变化,特别是那些与胆固醇代谢、软骨发育和炎症反应相关的基因。
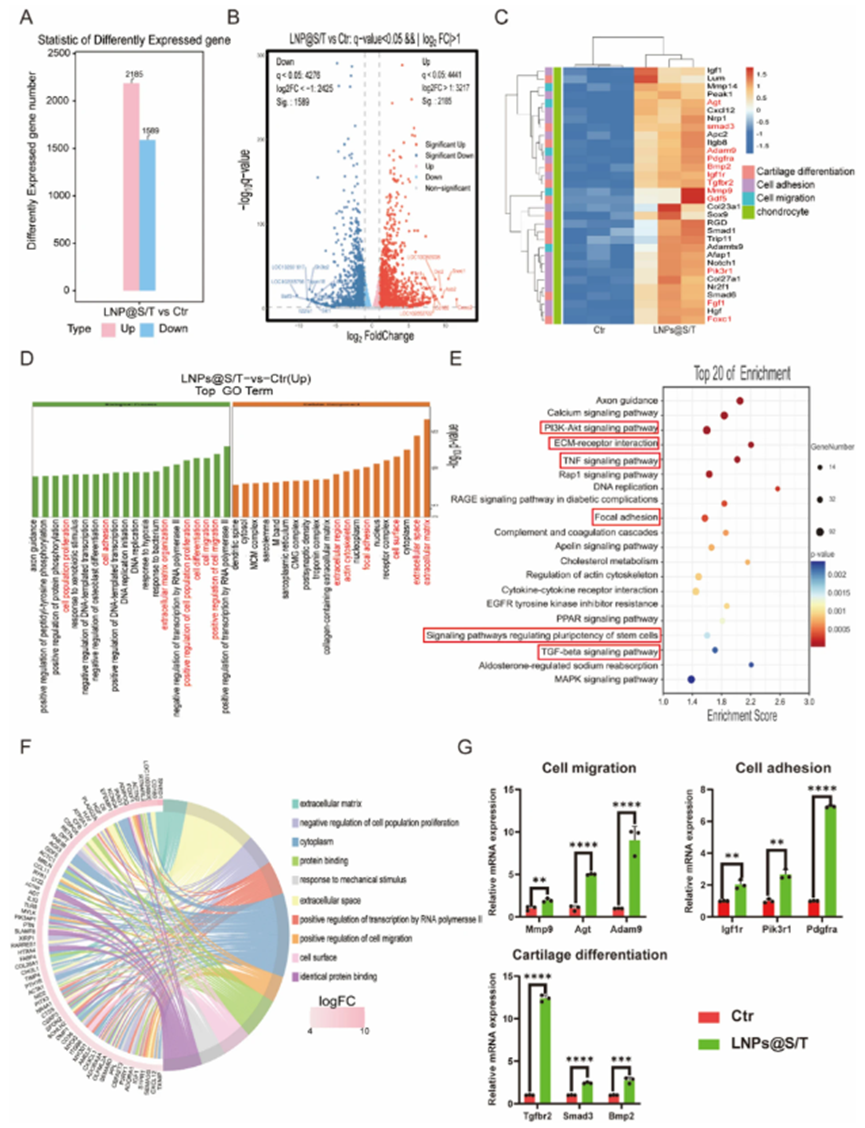
图3. LNP@S/T对SMSCs行为影响的内在机制
尽管这项研究已经取得了令人瞩目的成果,但科学家们并没有止步于此。他们意识到,对于老年患者而言,由于SMSCs的数量或质量可能有所下降,单纯依赖体内招募的方法可能会受到限制。因此,研究团队计划探索与生长因子联合治疗的可能性,比如添加血小板衍生生长因子(PDGF)或转化生长因子-β(TGF-β),以增强SMSCs的招募和活性。对于SMSCs严重减少的患者,则考虑采用自体或异体SMSCs移植的方法,力求最大程度地提高治疗效果。
总之,LNPs@S/T系统的出现为OA治疗开辟了一条充满希望的新途径。它不仅结合了干细胞技术和纳米技术的优势,还展示了多学科交叉合作在医学研究中的巨大潜力。随着科研的不断深入,这一创新疗法有望为OA患者带来更多的福音,显著提升他们的生活质量。(生物谷Bioon.com)
参考文献:
Zhao Z, Wang P, Li Z, et al. Targeted lipid nanoparticles distributed in hydrogel treat osteoarthritis by modulating cholesterol metabolism and promoting endogenous cartilage regeneration. J Nanobiotechnology. 2024;22(1):786. Published 2024 Dec 20. doi:10.1186/s12951-024-02965-9
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


