盘点:2022年终盘点:类器官重要研究成果解读及相关政策
来源:生物谷 2022-12-27 14:11
时至岁末,转眼间2022年即将谢幕,迎接我们的将是崭新的2023年,在过去的一年里科学家们在类器官研究领域取得了多项突破性的研究成果,同时国家也相继出台了类器官的相关政策
时至岁末,转眼间2022年即将谢幕,迎接我们的将是崭新的2023年,在过去的一年里科学家们在类器官研究领域取得了多项突破性的研究成果,同时国家也相继出台了类器官的相关政策,本文中,小编就对本年度科学家们在该研究领域取得的重磅级研究成果以及类器官相关的政策进行整理,分享给大家!
一、2022年类器官研究领域的重要成果:
【1】Nat Biomed Eng:中国科学家通过人星形胶质细胞再生脑类器官从而修复脊髓损伤
Xu, J., Fang, S., Deng, S. et al. Generation of neural organoids for spinal-cord regeneration via the direct reprogramming of human astrocytes. Nat. Biomed. Eng (2022). doi:10.1038/s41551-022-00963-6
中枢神经损伤包括脊髓损伤导致不可逆的中枢神经组织丧失,其治疗一直是神经科学与再生领域面临的重大科学难题。严重脊髓损伤患者出现下肢瘫痪,给患者、家庭及社会带来沉重的经济负担。研究发现,通过移植不同类型的神经细胞可在不同程度上改善SCI小鼠的运动功能,这表明神经细胞移植治疗脊髓损伤具有重大的应用潜力。诱导多能干细胞衍生的2D神经细胞移植可以避免免疫排斥,但存在成瘤风险、定向分化操作复杂以及移植后的随机扩散等问题。脊髓是高度特化的神经组织,神经细胞具有多样性和严格的空间分布,其发挥精细的神经信号传导和处理功能。目前,无论体外还是体内诱导产生具有精细结构的脊髓组织都面临巨大挑战。
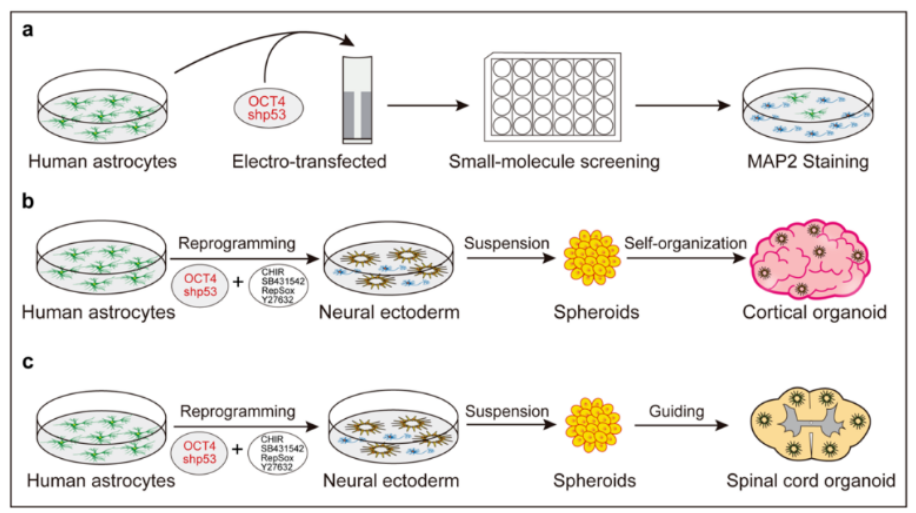
人星形胶质细胞重编程再生神经类器官
图片来源:Nat. Biomed. Eng (2022). doi:10.1038/s41551-022-00963-6
近年来,直接重编程内源性胶质细胞为神经元成为中枢神经系统(Central Nervous System,CNS)损伤修复的新策略,该策略不需要进行细胞移植即可促进神经元再生,且避免了免疫排斥反应。前期研究表明调控基因表达或使用小分子药物,小鼠和人的星形胶质细胞可以在体外和体内重编程为不同类型的神经元。然而,这些诱导的神经元不具备增殖和神经器官发生的能力。因此,利用中枢神经细胞直接再生出具有精细结构的3D脑与脊髓类器官,将为中枢神经组织损伤修复提供更大的应用潜力。
近日,一篇发表在国际杂志Nature Biomedical Engineering上题为“Generation of neural organoids for spinal-cord regeneration via the direct reprogramming of human astrocytes”的研究报告中,来自中国复旦大学的科学家们通过研究发现,人星形胶质细胞可被直接重编程为早期神经外胚层细胞,被重编程细胞不仅自组装形成皮层类器官,且在特定脊髓发育信号的激活下,可以定向诱导为具有背-腹侧空间结构的特异性脊髓类器官,将该脊髓类器官移植到完全脊髓损伤(SCI)小鼠模型中,发现其能存活,分化成脊髓神经细胞并与宿主神经元形成突触连接。
这项研究中,研究人员首次实现了直接利用体细胞再生3D神经组织修复中枢神经系统损伤,为今后开发内源性胶质细胞促进神经组织器官再生的研究奠定坚实的基础,加速中枢神经再生基础与临床转化研究。
【2】Cancer Discov:科学家成功制造出人类骨髓“类器官”来改善抗癌疗法
Abdullah O. Khan,Antonio Rodriguez-Romera,Jasmeet S. Reyat, et al. Human bone marrow organoids for disease modelling, discovery and validation of therapeutic targets in hematological malignancies, Cancer Discovery (2022). DOI:10.1158/2159-8290.CD-22-0199
由于缺乏能再现人类骨髓复杂性的模型,这或许就会阻碍科学家们对正常和恶性造血机制的研究以及对新型疗法的验证;近日,一篇发表在国际杂志Cancer Discovery上题为“Human bone marrow organoids for disease modelling,discovery and validation of therapeutic targets in hematological malignancies”的研究报告中,来自牛津大学等机构的科学家们通过研究首次制造出了能捕捉人类骨髓关键特征的骨髓“类器官”(organoids),这项新技术或能帮助同时筛选多种抗癌药物,并检测单一癌症患者个体化疗法治疗的效果。
文章中,研究人员描述了这种新方法,其能产生一种特殊的类器官,并能忠实地模拟造血骨髓(产生血细胞)的细胞、分子和架构特征。研究者指出,这种特殊的类器官能提供一种微环境来接受并支持来自于血液恶性肿瘤患者机体细胞的生存,包括多发性骨髓瘤细胞等,这些细胞在人体外是很难维持生长和生存的。研究者Abdullah Khan说道,值得注意的是,我们发现,这种新型骨髓类器官中的细胞不仅在活性和功能方面与真正的骨髓细胞相似,而且在架构关系方面也很相似,其细胞类型能在类器官中自我组织并进行排列,就好像其在人体的骨髓中一样。
这种栩栩如生的结构或许就能帮助研究人员研究骨髓中的细胞如何相互作用来支持正常的血细胞产生,以及这一点是如何在骨髓纤维化(bone marrow fibrosis)中被扰乱,骨髓疤痕会在骨髓中堆积,并引起骨髓功能衰竭,骨髓纤维化会在特定类型的血液癌症患者中发生,且仍然无法治愈。为了正确理解血液癌症发生的机制和原因,研究人员还需要利用实验系统来密切模仿真正的人类骨髓的工作机制,而此前研究人员还未拥有这样的系统。
开发并验证模式是关键的第一步,而在研究人员当前正在进行的研究中,他们将会同其它研究团队合作来更好地研究理解骨髓在健康人群中是如何工作的,以及当其患上血液疾病时机体到底出了什么问题;最后,研究者希望这种新型技术未来将能帮助加速发现并检测新的血液癌症疗法,同时帮助改进患者的药物治疗以及进行相应的临床试验。
【3】Cell:通过肝脏类器官揭示与GCKR-rs1260326突变有关的NAFLD/NASH风险较高
Masaki Kimura et al. En masse organoid phenotyping informs metabolic-associated genetic susceptibility to NASH, Cell, 2022, doi:10.1016/j.cell.2022.09.031.
众所周知,背景会影响许多领域。如今,一篇发表在国际杂志Cell上题为“En masse organoid phenotyping informs metabolic-associated genetic susceptibility to NASH”的研究报告中,来自日本东京医科大学等机构的科学家们通过研究发现,患者的健康背景(即患者的其他疾病)可以决定特定的基因突变是有益还是有害。研究人员揭示一种与肝脏疾病有争议关系的基因突变,根据患者是否患有糖尿病,给患者带来不同程度的风险。
非酒精性脂肪肝是一种最常见的肝脏疾病,并可发展为涉及肝脏中脂肪堆积、损害和炎症的非酒精性脂肪性肝炎(nonalcoholic steatohepatitis, NASH)。已知的遗传变异仅解释了患有NAFLD/NASH风险的一小部分,而且科学家们对某些突变的重要性有不同意见。研究者Masaki Kimura说,“葡萄糖激酶调节蛋白(GCKR)-rs1260326突变与NAFLD的关系存在广泛争议。这种突变似乎可以保护患者免受糖尿病和慢性肾脏疾病的影响,但与NAFLD和其他疾病的风险增加有关。”
为了更好地了解GCKR-rs1260326在NAFLD/NASH中的作用,这些作者从24名供者者身上提取细胞,并将它们培养成微小的肝脏样器官,即肝脏类器官(liver organoids)。他们给这些肝脏类器官提供额外的脂肪酸会导致脂肪堆积、炎症和胰岛素抵抗,这些特征在NASH患者的肝脏中都可以看到。他们然后密切分析了遗传变异和肝脏类器官特征之间的联系。
这一发现表明了一种新的治疗方法可能对那些对标准药物治疗没有反应的携带有这种突变的糖尿病患者的生活产生实际影响。由于NAFLD影响着全球近10亿人,较早识别需要不同类型治疗的患者可能会改善对NASH的预防和治疗。此外,这项新的研究表明,在培养皿中研究类器官并将这些信息与临床数据相结合,可能为复杂的常见疾病提供丰富的新见解。
【4】Nature:将人类皮层类器官移植到大鼠大脑中来研究大脑连接性和功能性
Omer Revah et al. Maturation and circuit integration of transplanted human cortical organoids. Nature, 2022, doi:10.1038/s41586-022-05277-w.
近日,一篇发表在国际杂志Nature上题为“Maturation and circuit integration of transplanted human cortical organoids”的研究报告中,来自美国斯坦福大学的研究人员开发出一种研究方法,可以更详细地探究与一些神经疾病和精神疾病相关的大脑过程。这是通过在体外培养人类皮层类器官(cortical organoids)并将它们移植到发育中的啮齿动物大脑内以观察它们随着时间的推移如何整合和发挥功能来实现的。
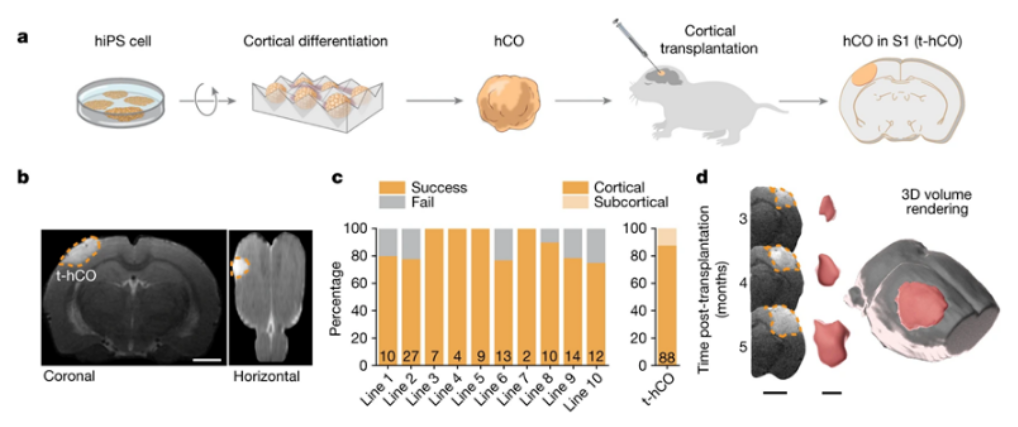
人类皮层类器官移植在发育中的大鼠皮层内。
图片来源:Nature, 2022, doi:10.1038/s41586-022-05277-w。
在这项新的研究中,斯坦福大学的Sergiu Pasca博士及其同事们证实,利用人类干细胞培养出的皮层类器官可以移植并整合到发育中的大鼠大脑内,以研究某些发育和功能过程。他们的研究结果表明,移植的皮层类器官可能为研究与疾病产生相关的过程提供一种强大的工具。科学家们有时使用人类皮层类器官---人类干细胞的三维培养物,可以反映典型大脑中的一些发育过程---作为研究人类大脑某些方面如何发育和发挥功能的模型。然而,皮层类器官缺乏典型人类大脑中的连接性,限制了它们在理解复杂大脑过程中的作用。人们一直试图通过将人类神经元移植到成年啮齿动物大脑中来克服其中的一些限制。虽然这些移植的神经元与啮齿动物的脑细胞连接在一起,但由于成年大鼠大脑的发育限制,它们并没有完全整合在一起。
文章中,作者通过将完整的人类皮层类器官移植到发育中的大鼠大脑内,推进了大脑类器官的研究使用。这项技术构建了一个可以被检查和操纵的人类组织单元。他们使用Pasca实验室之前开创的方法:利用人类诱导性多能干细胞---成体皮肤细胞经过重编程后进入一种未成熟的类似干细胞的状态---构建出人类皮层类器官。他们随后将所构建的人类皮层类器官植入大鼠初级体感皮层,即大脑中参与处理感觉的一部分。
【5】Nature:利用人类大脑类器官绘制人类大脑发育图谱
Jonas Simon Fleck et al. Inferring and perturbing cell fate regulomes in human brain organoids. Nature, 2022, doi:10.1038/s41586-022-05279-8.
人类的大脑很可能是整个生物世界中最复杂的器官,长期以来一直是科学家们着迷的对象。然而,研究大脑,特别是调节和指导它的发育的基因和分子开关,并不是一件容易的事。迄今为止,科学家们一直在使用动物模型(主要是小鼠)进行研究,但他们的发现不能直接适用于人类。小鼠的大脑结构与人类不同,缺乏人类大脑典型的皱褶表面。迄今为止,细胞培养物在这一领域的价值有限,因为细胞在培养皿上生长时往往会扩散到大片区域;这与大脑的自然三维结构不相符。
近日,一篇发表在国际杂志Nature上题为“Inferring and perturbing cell fate regulomes in human brain organoids”的研究报告中,来自瑞士苏黎世联邦理工学院生物系统科学与工程系的Barbara Treutlein教授及其团队采取了一种新的方法来研究人类大脑的发育:他们正在培养和使用类器官---毫米大小的可以利用所谓的多能性干细胞培育出的三维组织。只要这些多能性干细胞接受到正确的刺激,他们就能将它们编程成为身体中存在的任何一种细胞,包括神经元。当它们聚集成一个小的组织球,然后暴露在适当的刺激下,它们甚至可以自我组装,形成具有复杂组织结构的三维大脑类器官。
研究者Treutlein和她的同事们如今在不同的时间点和非常详细地研究了人类大脑类器官内的数千个细胞。他们的目标是用分子遗传学术语来描述这些细胞:换句话说,所有基因转录本(转录组)的总量作为基因表达的衡量标准,同时基因组可访问性作为调节活性的衡量标准。然而,这个过程产生了巨大的数据集:这种大脑类器官中的每个细胞有2万个基因,而每个大脑类器官又由成千上万个细胞组成。论文共同第一作者、Treutlein团队的博士生Jonas Fleck解释说,“这导致了一个巨大的矩阵,而我们能够解决它的唯一方法是借助合适的程序和机器学习。”为了分析所有这些数据并预测基因调节机制,这些作者开发了他们自己的程序。Fleck说,“我们可以用它来为每个基因生成一个完整的相互作用网络,并预测当该基因失效时在真实的细胞中会发生什么。
对由人类细胞材料组成的类器官的研究有一个优势,即所获得的研究结果可以适用于人类身上。它们不仅可以用来研究基本的发育生物学,还可以研究基因在疾病或大脑发育障碍中的作用。例如,Treutlein和她的同事们正在用这种类型的类器官研究自闭症和异位(heterotopia)的遗传原因;在异位中,神经元出现在大脑皮层的正常解剖位置之外。类器官也可用于测试药物,并可能用于培养可移植的器官或器官部分。Treutlein证实,制药行业对这些细胞培养物非常感兴趣。然而,培养类器官需要时间和精力。此外,每个细胞团都是单独发育的,而不是以标准化的方式发育。这就是为何Treutlein和她的团队正在努力改进类器官并使得它们的制造过程自动化。
【6】Cell:利用人类大脑类器官成功再现人类大脑发育中的关键事件
Ana Uzquiano et al. Proper acquisition of cell class identity in organoids allows definition of fate specification programs of the human cerebral cortex. Cell, 2022, doi:10.1016/j.cell.2022.09.010.
类器官(organoid)是在培养皿中精心培养的细胞集合,旨在比传统的细胞培养物更好地模拟器官结构和组成,使得人们对大脑等器官的生长和发育有了独特的看法。为了使它们在实验中发挥作用,科学家们需要确定这些模型如何忠实地再现体内细胞的行为。近日,一篇发表在国际杂志Cell上题为Proper acquisition of cell class identity in organoids allows definition of fate specification programs of the human cerebral cortex”的研究报告中,来自美国布罗德研究所的研究人员发现人类大脑类器官重现了正在发育的负责运动、感知和思考的人类大脑皮层中的许多重要细胞和分子事件。
这些作者利用干细胞培育出了大脑类器官,并在六个月的时间里仔细研究了它们的生长情况,为此他们使用了在单细胞水平上随着时间的推移绘制细胞位置、基因表达和染色质可及性---决定了基因活性如何受到调节---的工具。他们随后构建了一个“图谱”,描述了从大脑类器官中提取的60多万个在发育和成熟过程中被采样的细胞。他们发现,第一个月后,在他们制作的每个大脑类器官中,相同类型的细胞以相同的顺序发育,并表达了与发育中的人类胚胎相同的基因。
研究者Paola Arlotta表示,这对我们来说证实这一点是非常重要的。这告诉我们,我们可以用这些人类大脑类器官来研究我们之前无法研究的人脑发育过程。这些作者还能够确定人类特有的基因表达模式和其他关键发育因子。他们建议,由于这些大脑类器官是相当准确的早期大脑发育模型,并且可以在实验室中利用一小部分干细胞相对大量地培育出,这些模型可能能够有助于加快对大脑健康和神经发育障碍的研究。
此外,这些作者还分析了通常只发生在子宫内的早期发育阶段。他们观察到一种叫做胼胝体投射神经元(callosal projection neuron)的细胞,在成年人中比小鼠有更多的亚型,即使在这些早期阶段也已经变得多样化。这些细胞在人类中比其他物种更丰富,并且在人类进化过程中对大脑皮层的扩张做出了贡献。科学家们长期以来一直想知道这些特殊细胞是如何以及何时在人类大脑中产生和分化的。
【7】Cell Rep:肠道和肺部类器官或有望帮助开发新型先天性免疫细胞疗法
Geraldine M. Jowett,Emily Read,Luke B. Roberts, et al. Organoids capture tissue-specific innate lymphoid cell development in mice and humans, Cell Reports (2022). doi:10.1016/j.celrep.2022.111281
近日,一篇发表在国际杂志Cell Reports上题为“Organoids capture tissue-specific innate lymphoid cell development in mice and humans”的研究报告中,来自伦敦大学国王学院等机构的科学家们通过研究发现了一种新型创新性的方法或能在培养皿中扩大并促进先天性免疫细胞成熟;这一研究发现或有望帮助科学家们开发出新型的人类细胞疗法,从而帮助抵御多种人类慢性炎性疾病。
文章中,研究人员利用迷你肠道和肺部类器官来进行研究,结果发现,上皮细胞或能驱动组织特异性的先天性淋巴细胞(ILC,innate lymphoid cell)的发育。研究者表示,当对这些类器官进行培养时,所有的先天性淋巴细胞亚群都能成熟并呈现指数式的扩增,而且当基质被耗尽时,这一过程或许就能得到明显改善,这或许就颠覆了基于永生性机制供体细胞的金标准方法。
研究者Jowett博士说道,我们在小鼠上皮系统中的研究结果非常不错且是可重复的,但在项目早期,人类干细胞衍生的肠道类器官共培养物无法与小鼠模型的效率进行竞争,当我们开发间质细胞的剔除步骤时,我们希望非上皮部分的表现优于上皮器官,因为永生性的间质细胞是体外ILC研究的黄金标准。上皮细胞所产生的影响让研究人员大吃一惊,于是他们从对小鼠的数据中推测,上皮细胞对于组织特异性的ILC的印记非常重要,但研究人员从未提出,相比肠道间质而言,其能作为成熟的更强大的驱动力,正是这一研究发现或许就让科学家们对类器官的研究变得有趣且有意义。
研究人员希望这种基于人类类器官的系统或能提供一种重要的进展,不仅仅是为了基本理解先天性淋巴细胞如何在远端粘膜位点进行发育,而且还能被应用来作为机体炎症的强大调节子。综上,本文研究结果有望帮助揭示先天性淋巴细胞的活性机制以及其发育如何在慢性炎性疾病中失调。
【8】Cell Stem Cell:科学家有望优化人类小肠类器官的产生
Gui-Wei He et al. Optimized human intestinal organoid model reveals interleukin-22-dependency of Paneth cell formation. Cell Stem Cell, 2022, doi:10.1016/j.stem.2022.08.002.
近日,一篇发表在国际杂志Cell Stem Cell上题为“Optimized human intestinal organoid model reveals interleukin-22-dependency of paneth cell formation”的研究报告中,来自荷兰皇家艺术与科学学院等机构的研究人员改进了人类小肠类器官的培育,这将帮助人们更好地研究小肠在健康和疾病期间的功能。具体来说,他们成功地开发出了包含成熟的潘氏细胞(Paneth cell)的小肠类器官,而潘氏细胞在以前的人类小肠类器官中是不存在的。
类器官的培育对于人类器官和组织的功能研究意味着很多。这与这些微型器官能很好地代表人类生物学这一事实有关。然而,目前可用的一些人类类器官,如小肠类器官,还不能完全类似于天然的小肠器官。因此,这些作者开发出一种新的、优化版本的微型小肠:包括人类小肠所有细胞类型的类器官。为了诱导人类小肠类器官中潘氏细胞的形成,这些作者研究了多种分子的影响。他们发现,白细胞介素-22(IL-22)增加了潘氏细胞的数量和活性。IL-22对潘氏细胞的影响是令人惊讶的。论文共同第一作者、荷兰皇家艺术与科学学院研究员Gui-Wei He解释了其中的原因:“目前,人们认为IL-22能促进干细胞功能。我们的研究实际上表明,IL-22并没有这样做,而是刺激了潘氏细胞的激活。”因此,这种新发现的IL-22功能被用来增加人类小肠类器官中活跃的潘氏细胞的数量。这导致了模拟健康小肠的类器官的构建。
现在有了优化的人类小肠类器官,科学家们可以扩展他们的研究内容。例如,他们可以使用这种小肠类器官让细胞的DNA发生突变。通过这种方式,他们可以确定发生在IBD等疾病中的突变如何影响小肠的功能。
【9】Cell Rep:实验室培育的“迷你肾脏”类器官或能帮助解锁人类罕见疾病的成因
Adam Pietrobon,Julien Yockell-Lelièvre,Trevor A. Flood, et al. Renal organoid modeling of tuberous sclerosis complex reveals lesion features arise from diverse developmental processes, Cell Reports (2022). DOI: 10.1016/j.celrep.2022.111048
结节性硬化症(TSC,Tuberous sclerosis complex)是一种由TSC1和TSC2缺失所引起的多系统肿瘤性疾病,其在肾脏的表现主要为囊肿和血管平滑肌脂肪瘤。近日,一篇发表在国际杂志Cell Reports上题为“Renal organoid modeling of tuberous sclerosis complex reveals lesion features arise from diverse developmental processes”的研究报告中,来自渥太华医院研究所等机构的科学家们通过研究发现了在结节性硬化症患者机体中引发肿瘤的特殊细胞,文章中,研究人员开发了遗传工程化的肾脏类器官,即利用人类组织来生长这种“迷你肾脏”。
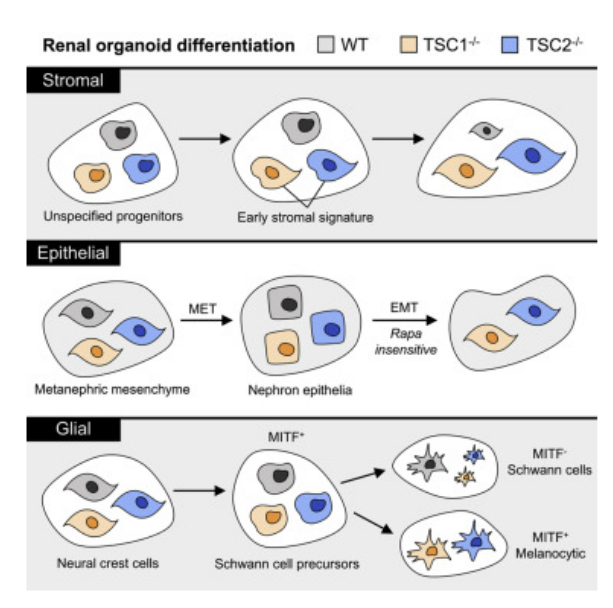
实验室培育的“迷你肾脏”类器官或能帮助解锁人类罕见疾病的成因。
图片来源:Cell Reports (2022). DOI: 10.1016/j.celrep.2022.111048
研究者Bill Stanford表示,几十年来,关于结节性硬化症肿瘤的起源细胞,对于科学家们而言一直是一个谜题,本文研究结果或许就能帮助研究人员找到这种挑战性疾病的新型疗法靶点。TSC是一种罕见的遗传性疾病,其会在皮肤、大脑、肾脏、心脏或肺部中引起肿瘤,且TSC的肿瘤多样化,往往起源于儿童或成年人机体中,其症状由轻度到危及生命的程度,通常包括癫痫发作和肾脏问题等,目前针对该病尚无有效的治愈方法,且治疗方案也非常有限。
肾脏疾病是TSC患者发生死亡的主要原因,大约60%-80%的患者都会在肾脏中形成肿瘤,这通常会降低患者的肾脏功能,有时还会导致灾难性的出血现象,目前研究人员并没有足够的实验室模型来研究TSC是如何影响肾脏的,因此研究人员急需在该研究领域取得重大进展。TSC是由TSC1或TSC2基因的突变所致,对于大部分患者而言,这些突变会在机体发育过程或生命早期自发产生,而并非是遗传自父母;这就使得TSC成为科学家们难以研究的一种疾病,由于科学家们通常会利用动物来研究人类疾病,目前并没有动物模型能完全捕获到TSC对肾脏的影响。
综上,本文研究结果揭示了TSC1和TSC2双等位基因失活所产生的多种发育结局,同时也提供了对TSC肾脏病变发病机制的见解。
【10】Nat Cancer:类器官研究揭开结直肠癌化疗后易复发的关键
Adrián Álvarez-Varela, Laura Novellasdemunt, Francisco M Barriga, et al. Mex3a marks drug-tolerant persister colorectal cancer cells that mediate relapse after chemotherapy, Nat Cancer
. 2022 Sep;3(9):1052-1070. doi: 10.1038/s43018-022-00402-0
结直肠癌(Colorectal Cancer)是全世界范围内发病率第三的癌症,每年新增发病人数近200万,仅次于乳腺癌和肺癌,每年导致的死亡人数接近100万,仅次于肺癌。大约每25个人就有1人会在其一生中患上结直肠癌。
化疗通常被用于结直肠癌的治疗,而且在最初的治疗中是有效的,但大多数患者在化疗后会出现病情复发。近日,一篇发表在国际杂志Nature Cancer上题为“Mex3a marks drug-tolerant persister colorectal cancer cells that mediate relapse after chemotherapy”的研究报告中,来自西班牙巴塞罗那科学技术学院的科学家们通过使用来自结直肠癌患者的肿瘤样本构建了类器官(Organoids),通过类器官研究发现,具有 Mex3a 蛋白活性的肿瘤干细胞在化疗时处于潜伏状态,因此对化疗产生耐药性,在化疗之后环境有利时,这些潜伏的肿瘤干细胞会被重新激活并再生肿瘤。这些潜伏状态的肿瘤干细胞是结直肠癌化疗后复发的关键。
研究人员表示,对于结直肠癌的治疗,化疗显然是有效的,它能够杀死大部分肿瘤细胞,但并不是全部。这项研究揭示了对化疗耐药的一群肿瘤干细胞,它们在化疗后能继续再生肿瘤。这一发现为开发真毒性清除这类细胞的药物铺平了道路,有望进一步增强化疗效果并提高结直肠癌患者生存率。
这项研究主要使用来自患者的肿瘤样本构建的类器官(Organoids)进行,通过对类器官的观察,研究团队能够追踪整个化疗过程中肿瘤细胞的变化,并观察它们对化疗的反应。研究团队还使用了结直肠癌小鼠模型,进一步在体内观察和再现这些细胞的行为,并将在患者结直肠癌细胞来源的类器官和结直肠癌小鼠模型中获得的结果与患者肿瘤样本的转录组分析进行对比。
本文研究结果表明,这些研究结果表明,肿瘤干细胞对逆境适应可以保护它们免受化疗的影响,并确定了导致结直肠癌化疗治疗后复发的候选细胞。研究团队表示,后续研究工作将侧重于分析背后的分子机制,特别是 Mex3a 蛋白如何将肿瘤干细胞维持在这种休眠状态。
【11】Sci Transl Med:利用人类肾脏类器官确定化合物SCR7有望阻止肾脏损伤和治疗慢性肾脏病
Navin Gupta et al. Modeling injury and repair in kidney organoids reveals that homologous recombination governs tubular intrinsic repair. Science Translational Medicine, 2022, doi:10.1126/scitranslmed.abj4772.
在某种程度上,肾脏在受伤后有自我修复的能力,但是这种内在修复会转变为不完全修复,从而导致不可逆的损伤和慢性肾脏病(CKD)。近日,一篇发表在国际杂志Science Translational Medicine上题为“Modeling injury and repair in kidney organoids reveals that homologous recombination governs tubular intrinsic repair”的研究报告中,来自麻省总医院研究人员利用人类干细胞衍生的肾脏类器官鉴定出对维持肾脏健康修至关重要的基因。这些发现可能会导致人们发现新的靶标,以协助预防或治疗CKD。
尽管在动物研究中已经确定了参与肾脏修复的多种因子,但将这些发现转化为临床是很困难的,因为许多在动物身上被认为是安全和有效的治疗方法后来在临床试验中被发现是有毒或无效的。人类肾脏类器官,就像微型的肾脏,可能会帮助科学家们避免这些挫折。当Gupta和他的同事们将人类肾脏类器官暴露于化疗药物顺铂中时,这种治疗改变了正在进行内在修复的肾细胞中的159个基因表达和29条信号通路。他们确定的许多基因,包括两个名为FANCD2和Rad51的基因,在内在修复过程中被激活,但是当肾脏损伤变得不可逆时,它们的表达就会下降。这些基因编码的蛋白在细胞中的DNA受损时发挥着修复作用。在小鼠肾脏损伤模型和人类肾脏活组织中进行的其他实验证实了这些在肾脏类器官中发现的结果。
最后,通过药物筛选试验,这些作者确定了一种称为SCR7的化合物,它有助于维持FANCD2和RAD51的活性,以拯救正常的组织修复,并防止在顺铂诱导的肾脏类器官损伤模型中出现CKD进展。
【12】Nat Cancer:利用功能性类器官筛选鉴定出靶向实体瘤中癌干细胞的抗体MCLA-158
Bram Herpers et al. Functional patient-derived organoid screenings identify MCLA-158 as a therapeutic EGFR × LGR5 bispecific antibody with efficacy in epithelial tumors. Nature Cancer, 2022, doi:10.1038/s43018-022-00359-0.
近日,一篇发表在国际杂志Nature Cancer上题为“Functional patient-derived organoid screenings identify MCLA-158 as a therapeutic EGFR × LGR5 bispecific antibody with efficacy in epithelial tumors”的研究报告中,来自西班牙巴塞罗那生物医学研究院等机构的科学家们通过研究揭示了导致MCLA-158发现的临床前数据及其对癌干细胞的作用机制。这种被命名为派森妥单抗(Petosemtamab)的抗体MCLA-158能防止癌症转移的发生(即癌症扩散到其他重要器官),并减缓癌症实验模型中原发性肿瘤的生长。
在这篇论文中,他们描述了他们如何创建他们的纳米胶囊,以及当在患有胶质母细胞瘤的小鼠身上进行测试时它的效果如何。这项研究也为制药公司在药物发现过程中使用类器官模型奠定了基础。类器官是可以在实验室中生长的患者衍生性样本,它们再现了肿瘤区室的某些方面。到目前为止,它们的用处正在个性化癌症医学中得到探索---意思是它们在帮助医生决定每名患者的最佳治疗方面的价值。然而,为了选择MCLA-158,首次使用了来自癌症患者的类器官生物库,在数百种新抗体中分辨出哪一种最有效并最适合大多数患者。
为了开发和表征这种抗体,来自HUB Organoids的研究人员建立了一个大型生物库,其中包括来自结肠癌患者的类器官,结肠癌转移到肝脏的类器官,以及来自正常非癌组织的类器官。来自OcellO公司(OcellO B.V.)的科学家们利用这些类器官进行了高通量筛选。在药物开发的早期阶段使用类器官有助于识别那些对大多数患者有效的抗体,甚至对携带特定突变的肿瘤有效的抗体。使用来自健康组织的类器官,还有一个好处是可以确定药物对器官的不必要的副作用。这种方法使得研究人员能够评估药物对健康细胞的有害影响,从而在研究的最初阶段撤回具有更大毒性的抗体。
【13】Nature:科学家利用人类多能干细胞生成3D泪腺类器官!
Hayashi, R., Okubo, T., Kudo, Y. et al. Generation of 3D lacrimal gland organoids from human pluripotent stem cells. Nature (2022). doi:10.1038/s41586-022-04613-4
泪腺是眼睛的主要外分泌腺体。它们位于眼眶内,上眼睑后面,朝向每只眼睛的颞叶侧,分泌泪液作为泪膜的主要成分。泪腺对建立和维持健康的泪膜、保持良好的视力有重要作用。泪腺功能障碍和泪液分泌减少与一系列病因有关,并且是最常见的自身免疫性疾病之一——斯约克伦综合症的特征,在这种情况下会导致干眼症。胎儿哺乳动物的泪腺细胞具有再生能力。然而,在成人中,泪腺的再生能力似乎很小。因此,科学家们将泪腺确定为旨在使用人多能干(PS)细胞进行再生治疗和药物发现的研究靶标。
近日,一篇发表在国际杂志Nature上题为“Generation of 3D lacrimal gland organoids from human pluripotent stem cells”的研究报告中,来自日本大阪大学的科学家们从人类多能干细胞生成了3D泪腺类器官。在本研究中,他们鉴定了具有泪腺原基特征的细胞,这些细胞出现在从人类多能干细胞培养的二维眼样类器官中。含有眼表上皮样细胞的SEAM区3会产生泪腺的前体。他们采用流式细胞仪对从分离的泪腺样簇中获得的细胞进行分析,使用先前确定的抗体组合(抗ITGB4、抗SSEA-4和抗CD200)来识别眼表上皮干细胞。研究发现,泪腺样细胞簇被纳入SEAM内的眼表上皮干细胞群中,细胞群被鉴定为由hiPS细胞制造的泪腺样类器官的起源。
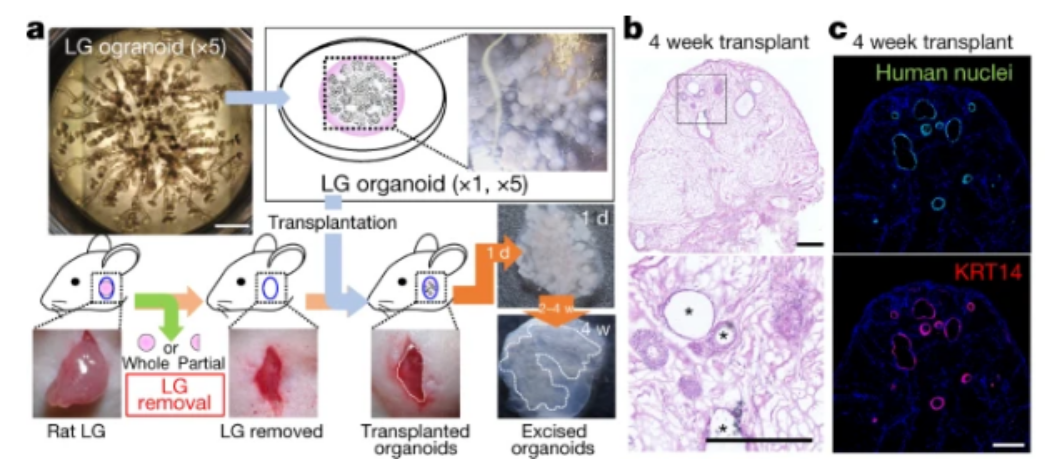
泪腺样类器官的移植
图片来源:Nature (2022). doi:10.1038/s41586-022-04613-4
研究人员筛选了泪腺样类器官形成的最佳培养基,即EGF/Y-27632培养基,并在此培养基上形成了泪腺样组织类器官。当通过细胞分选分离并在规定的条件下生长时,这些细胞形成了一个三维的泪腺样组织器官,具有导管和尖头,通过出芽和分支得以实现。克隆集落分析表明,该类器官起源于多潜能的眼表上皮干细胞。器官体在形态、免疫标记特征和基因表达模式方面与本地泪腺有明显的相似性,当移植到受体大鼠的眼睛附近时,会发生功能成熟,形成管腔并产生泪膜蛋白。
【14】Nat Commun:利用人类皮层类器官揭示小胶质细胞在阿尔茨海默病产生中的作用
Bilal Cakir et al. Expression of the transcription factor PU.1 induces the generation of microglia-like cells in human cortical organoids. Nature Communications, 2022, doi:10.1038/s41467-022-28043-y.
在科学家们寻找阿尔茨海默病的根源时,他们很难确定小胶质细胞---一种对大脑发育和成体大脑维护至关重要的免疫系统细胞---是朋友还是敌人。有证据显示,小胶质细胞的缺乏有助于淀粉样蛋白斑块的积累,其中淀粉样蛋白斑块是阿尔茨海默病的一种典型特征。另外,小胶质细胞过多也与神经元和大脑突触的破坏有关,这也是这种疾病的神经变性特征。
近日,一篇发表在国际杂志Nature Communications上题为“Expression of the transcription factor PU.1 induces the generation of microglia-like cells in human cortical organoids”的研究报告中,来自美国耶鲁大学的研究人员开发出一种方法来梳理出可能决定小胶质细胞发挥哪些作用的因素。研究者表示,我们成年后拥有的所有小胶质细胞都是在我们出生前产生的。小胶质细胞在神经发生中至关重要,因为它们进行突触修剪,使神经元能够正常交流。
在这项新研究中,来自Park实验室的Bilal Cakir和Yoshiaki Tanaka开发了一种方法,在人类皮层类器官中产生功能性小胶质细胞,其中这种皮层类器官是由早期干细胞形成的,是模拟发育中大脑的小型三维结构。在实验室测试中,他们确定了一个在发育早期产生的活性基因,该基因对小胶质细胞的产生至关重要。然后,他们能够激活该基因,诱导大脑皮层类器官中的小胶质细胞产生。
在初步实验中,他们发现缺乏小胶质细胞的大脑皮层类器官容易积累淀粉样蛋白,即一种形成与阿尔茨海默病有关的斑块的蛋白。但是,具有正常功能的小胶质细胞的大脑皮层类器官则不会这样。这些研究结果表明,在这种情形下,小胶质细胞起到了保护作用。他们说,这种大脑皮层类器官可用于研究与阿尔茨海默病产生有关的其他基因的影响。
【15】Nature:利用大脑类器官揭示不同的自闭症风险基因对大脑发育产生相同的影响
Bruna Paulsen et al. Autism genes converge on asynchronous development of shared neuron classes. Nature, 2022, doi:10.1038/s41586-021-04358-6.
自闭症谱系障碍(ASD)与数百个不同的基因有关,但这些不同基因发生的突变如何在患者身形成相似的病理仍然是个谜。近日,一篇发表在国际杂志Nature上题为“Autism genes converge on asynchronous development of shared neuron classes”的研究报告中,来自哈佛大学等机构的研究人员发现三个不同的自闭症风险基因实际上影响着神经形成的相似方面以及发育中的人类大脑中相同类型的神经元。通过在称为“大脑类器官(brain organoid)”的人类大脑微型三维模型中测试这些基因突变,他们发现在这三个风险基因中,每个都存在类似的整体缺陷,尽管每个风险基因都通过独特的潜在分子机制发挥作用,这些结果使人们对自闭症谱系障碍有了更好的了解,并向寻找治疗这种疾病的方法迈出了第一步。
研究者Paola Arlotta博士表示,该领域的许多努力都致力于了解与自闭症相关的许多风险基因之间是否存在共性。找到这样的共同特征可能会突出广泛的共同靶标用于开发治疗干预措施,而与疾病的遗传起源无关。我们的数据显示,多种致病性突变确实集中在一起影响相同的细胞和发育过程,但通过不同的机制。Arlotta实验室专注于人类大脑皮层的类器官模型,其中大脑皮层是大脑中负责认知、感知和语言的部分。这种模型是由干细胞长成一种三维组织而形成的,含有大脑皮层的许多细胞类型,包括能够放电和形成电路的神经元。
研究者Silvia Velasco表示,在2019年,我们公开了一种允许产生具有独特的可重复生长能力的类器官的方法。它们始终如一地以相同的顺序形成与发育中的人类大脑皮层相同类型的细胞。如今看到类器官可以用来发现像自闭症这样复杂的疾病的一些意想不到和非常新的东西,这真地是梦想成真。
【16】Science:利用人类大脑类器官揭示结节性硬化症的起源
Oliver L. Eichmüller et al. Amplification of human interneuron progenitors promotes brain tumors and neurological defects. Science, 2022, doi:10.1126/science.abf5546.
近日,一篇发表在国际杂志Science上题为“Amplification of human interneuron progenitors promotes brain tumors and neurological defects”的研究报告中,来自奥地利科学院等机构的科学家们在大脑类器官的帮助下,揭示了结节性硬化症(tuberous sclerosis complex, TSC)是一种罕见的神经发育遗传性疾病,它是在发育过程中产生的,而不仅仅是在遗传上。通过这些来自患者的人类大脑实验室模型,他们将这种疾病的起源确定为人类特有的尾侧晚期中间神经元祖细胞,这些研究结果进一步表明,只有使用人类衍生的大脑类器官模型才能很好地理解影响人类大脑的疾病的病理。
人类大脑的复杂性很大程度上是由于发育涉及到人类独有的过程,其中许多过程仍是我们当前科学知识中的空白。TSC在这方面也不例外,因为长期以来,基于动物模型获得的数据,它被描述为一种主要的遗传性疾病。如今,论文共同通讯作者、奥地利科学院分子生物技术研究所科学主任Jürgen A. Knoblich及其研究团队的突破性研究利用患者衍生的大脑类器官模型来揭开这种罕见的神经发育疾病的神秘面纱。Knoblich解释说,“我们对TSC根源的研究结果使我们发现了一种人类大脑特有的祖细胞类型。这解释了为什么其他实验室模型不能很好地确定这种疾病的病理。”
在这项新的研究中,Knoblich团队培养出了源自几名受影响的患者的大脑类器官,这种方法可以研究患者大脑在发育过程中某个阶段存在的分子和细胞机制。论文第一作者Oliver Eichmüller解释说,“通过这种方法,我们发现,就像在患者的大脑中一样,这类大脑类器官长出了肿瘤,并有类似于患者结节的无序区域。”然而,重现一种疾病的病理生理学特征仅仅是第一步。Eichmüller说,“通过进一步挖掘原因,我们发现这两种异常都是由人类大脑特有的一种细胞类型过度增殖引发的。这些细胞被称为尾侧晚期中间神经元祖细胞,简称CLIP细胞。它们在人类大脑的发育阶段被发现,但在像小鼠这样的动物中没有。”Corsini说,“我们的研究表明,我们的大脑非常复杂,比大多数动物的大脑要复杂得多。”
【17】Adv Sci:利用类器官芯片实现人体肝脏-胰岛互作仿生模拟
Tingting Tao, Pengwei Deng, Yaqing Wang, et al. Microengineered Multi-Organoid System from hiPSCs to Recapitulate Human Liver-Islet Axis in Normal and Type 2 Diabetes, Adv Sci (Weinh)
. 2022 Feb;9(5):e2103495. doi: 10.1002/advs.202103495
糖尿病发病率逐年上升,威胁人类健康。人体内糖稳态调控受多种组织影响,包括脑、胰腺、肝脏和肌肉等,其中肝脏和胰岛在血糖调控过程中存在复杂的功能联系,在机体糖稳态调控中发挥重要作用。胰岛分泌的激素(如胰高血糖和胰岛素)可通过调控肝糖的合成和分解,维持体内血糖稳态的平衡。调控作用失衡往往引起体内血糖水平失调及代谢紊乱,并可导致2型糖尿病(T2DM)发生。尽管目前已有细胞和动物模型用于糖尿病研究,但仍缺少能够反映人体复杂器官间关联作用的研究体系。
近日,一篇发表在国际杂志Advanced Science上题为“Microengineered Multi-Organoid System from hiPSCs to Recapitulate Human Liver-Islet Axis in Normal and Type 2 Diabetes”的研究报告中,来自中国科学院大连化学物理研究所的科学家们利用类器官芯片建立了人诱导多能干细胞(hipsC)来源的肝-胰岛类器官互作体系;在体外模拟人体肝脏-胰岛轴及其在生理和病理条件下的糖刺激响应,为糖尿病等复杂代谢性疾病研究和新药发现等提供了新策略和新技术。
该工作中,科研人员将类器官与器官芯片前沿技术结合,构建了由人多能干细胞衍生的肝-胰岛类器官互作体系。在分区设计的微阵列芯片上实现了肝、胰岛类器官的动态培养和相互作用研究,类器官功能维持可长达1个月。研究发现,该共培养体系有利于维持肝和胰岛类器官活性,并促进肝和胰岛类器官的分泌功能增强,提高器官特异性的功能基因和蛋白表达。该研究首次利用类器官芯片技术,在体外再现了人体肝脏-胰岛的交互作用特点及其在生理和病理条件下的糖调控响应,为2型糖尿病等复杂代谢性疾病研究和药物开发等提供了新的策略和技术。
【18】Science:组织的几何形状或会引导类器官的形成
N. GJOREVSKI,M. NIKOLAEV,XT. E. BROWN,et al. Tissue geometry drives deterministic organoid patterning, Science (2022). DOI:10.1126/science.aaw9021
干细胞衍生的类器官是体外组织和器官的模拟物,其能作为研究人类器官发育和疾病发生的重要模型,同时也能作为药物发现和诊断的平台,对于设计新型细胞和基因疗法也至关重要;然而,目前研究人员并不清楚类器官发育背后的干细胞自组装过程是如何被控制的,从而就会导致现有的类器官培养物普遍缺乏可重复性,比如小鼠肠道类器官(其或许是迄今为止被最好描述地类器官系统)中隐窝样结构的位置和数量是无法进行控制的,而且类器官的形状、大小和多细胞组成也是无法控制的,目前类器官模型的较高变异性给基于类器官的基础和转化研究带来了重大的挑战。
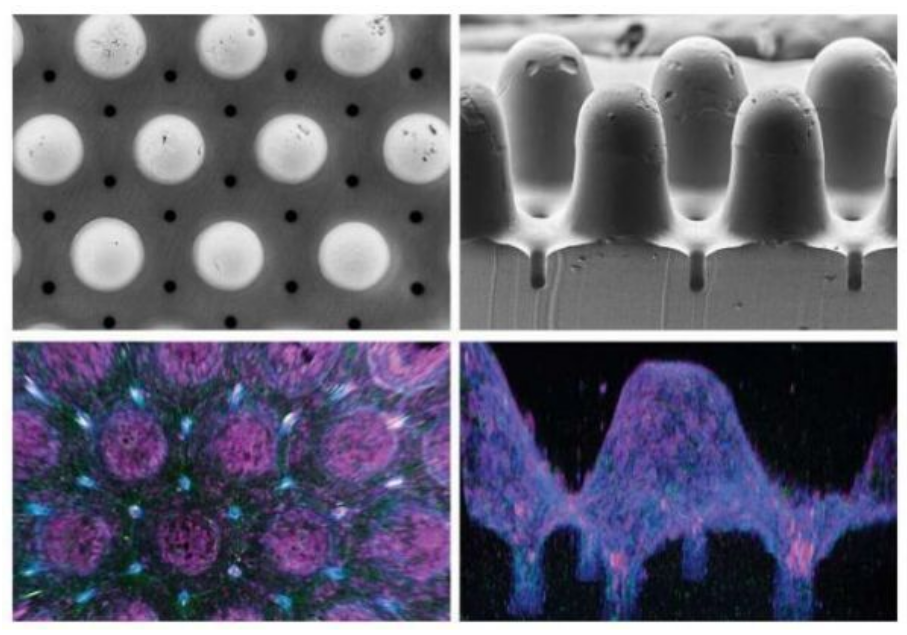
具有活体组织结构的生物工程类器官。
图片来源:Mike Nikolaev (EPFL)
近日,一篇发表在国际杂志Science上题为“Tissue geometry drives deterministic organoid patterning”的研究报告中,来自瑞士的科学家们通过研究发现,形状或许会引导类器官的生长;研究者表示,对类器官形成和所产生结构进行控制既能帮助理解潜在的形态发生机制,还能帮助建立与“本地对应物”更为相似的模型。真实器官的最终功能结构是上皮细胞自组装程序和外在微环境控制器之间相互作用的产物,从体内发育中得到启发,研究人员利用外部调节机制来补充类器官的自组装,尤其是,研究人员能尝试通过物理特性来控制肠道类器官的模式和形态发生,尤其是组织自身的初始几何形状。
文章中,研究人员开发了生物工程性策略,通过水凝胶力学的原位模式和水凝胶微加工模式,从外部来控制肠道干细胞的自组装过程;他们发现,微环境力学的局部模式和预定的水凝胶微貌或能用来建立具有可控最初尺寸和形状的类器官,同时研究者还能预测并影响其发育的过程,尤其是隐窝结构的数量和未知。研究人员能利用对类器官发育的可预测性来识别出上皮细胞模式化背后的基本机制。
综上,本文研究结果表明,研究人员提出了一种能引导基于干细胞的器官生成的方法,这一过程完全是由随机的自组装过程所驱动的,研究人员还验证了长期存在但并未被充分探究的形态发生范式,即组织的现有形状能帮助模式化并指定发育的过程,因此这也是组织的未来形状。在肠道隐窝形成的案例中,研究者总结道,出芽不仅仅能跟随帕内特细胞细胞的出现,也可以在其之前出现;研究人员所开发的类器官培养物或能用于回答现有的类器官和动物模型不容易解决的问题,而且其可能还会使得类器官技术转化为对现实世界的应用。
二、和类器官领域相关的政策
除了科学家们在类器官研究领域取得的多项重要研究成果外,关于类器官领域的支持性政策也在相继推出,类器官能用于建立疾病的相关模型,与2D疾病模型相比,其在阐明疾病的发展、稳态和发病机制方面更具优势。
【1】2022年7月10日,《类器官药物敏感性检测指导肿瘤精准治疗临床应用专家共识》(2022年版)由中国抗癌协会肿瘤标志专业委员会、中国癌症防治杂志、广东省类器官工程技术研究中心、广东省精准医学应用学会类器官与器官芯片分会联合正式发布,在肿瘤精准医学的发展中具有里程碑意义。
【2】2022年07月30日,《肿瘤类器官诊治平台的质量控制标准中国专家共识》(2022年版)由中国抗癌协会肿瘤多学科诊疗专业委员会、中国抗癌协会肿瘤内分泌专业委员会联合正式发布,虽然类器官在指导临床治疗中的应用尚处于起步阶段,但是利用肿瘤类器官指导患者治疗的需求日趋增长;希望通过专家共识,提高中国临床工作者及医学研究者对于类器官药物敏感性检测的认识,规范类器官诊治平台的质量控制,指导类器官药物敏感性检测在国内肿瘤精准治疗方案选择中的临床应用。
【3】2022年9月24日,《人肠癌类器官》《人肠道类器官》团体标准发布,其是国内首个肠类器官标准;该团体标准于2022年10月31日正式实施。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


