Nat Commun:开发出强效的γδT细胞,有望实现通用的癌症免疫疗法
来源:生物谷原创 2023-11-13 15:33
“现成的(off-the-shelf)”细胞疗法,也称为异体细胞疗法(allogenic cell therapy),使用的免疫细胞来自健康的捐献者,而不是患者。这
“现成的(off-the-shelf)”细胞疗法,也称为异体细胞疗法(allogenic cell therapy),使用的免疫细胞来自健康的捐献者,而不是患者。这种方法可以更及时地为更多患者提供诸如嵌合抗原受体(CAR)T细胞疗法之类的细胞疗法,而这正是为患者提供这些救命疗法的主要障碍之一。
在一项新的研究中,来自美国加州大学洛杉矶分校的研究人员开发出一种新方法,可以设计出更强大的免疫细胞,这些细胞有可能用于“现成的”细胞疗法,以治疗具有挑战性的癌症。这种新方法是朝着开发更有效的细胞疗法迈出的关键一步,这种细胞疗法成本更低,等待时间更短,可以大规模生产并运送到世界各地的医院,从而使CAR-T细胞疗法更便宜,并为更广泛的患者所接受。相关研究结果于2023年11月8日发表在Nature Communications期刊上,论文标题为“Unlocking the potential of allogeneic Vδ2 T cells for ovarian cancer therapy through CD16 biomarker selection and CAR/IL-15 engineering”。

论文通讯作者、加州大学洛杉矶分校微生物学、免疫学与分子遗传学副教授Lili Yang说,“在治疗晚期癌症患者时,时间往往是至关重要的。目前,这类疗法需要根据患者的具体情况量身定制。我们必须从患者体内提取称为T细胞的免疫细胞,对这些细胞进行基因改造,然后再将它们重新灌注回患者体内。这个过程可能需要几周到几个月的时间,治疗每名患者可能需要花费数十万美元。”
在这项新的研究中,Yang和她的团队重点研究了γδT细胞(gamma delta T cell),这类免疫细胞因能靶向包括实体瘤在内的多种癌症而闻名,但不会引起移植物抗宿主病,而移植物抗宿主病是异体细胞疗法中常见的并发症。
尽管之前研究过基于γδT细胞的疗法,但由于供体的可变性、短暂的持续性以及癌细胞逃避或躲避人体免疫反应的能力,这些疗法的临床成功率有限。
然而,Yang和她的团队发现,高表达CD16表面标志物的供体γδT细胞杀死癌细胞的能力更强。Yang说,“这些CD16高表达的γδT细胞表现出独特的特征,提高了它们识别肿瘤的能力。它们显示出更高水平的效应分子,并具备对癌细胞产生抗体依赖性细胞毒性的能力。我们发现,通过使用CD16作为供体选择的生物标志物,可以提高它们的抗癌特性。”
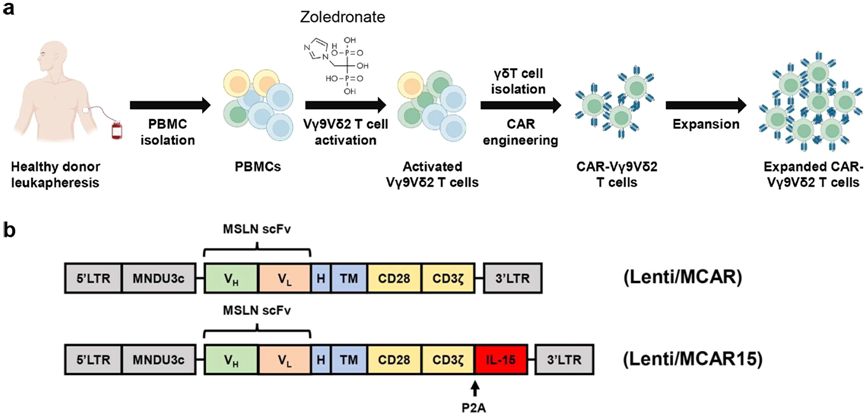
高表达CD16的Vδ2 T细胞经过基因改造表达CAR/IL-15后,同时保持扩增能力和记忆状态。图片来自Nature Communications, 2023, doi:10.1038/s41467-023-42619-2。
Yang和她的团队还克服了之前的γδT细胞治疗研究中出现的一些问题,他们对这些细胞进行了基因改造,使它们表达CAR和IL-15,这两种重要成分有助于增强γδT细胞的抗癌能力。
这些作者随后能够有效地大量制造出这些更强效的经过基因改造的γδT细胞,并在两种不同的临床前卵巢癌模型上进行了测试。他们发现,这些γδT细胞能够攻击肿瘤,并能在这两种模型中持续很长一段时间,从而使它们能够继续发挥抗肿瘤作用。此外,没有出现移植物抗宿主病等并发症的迹象。
Yang说,“这项新研究的成果揭示了这些经过基因改造的高表达CD16的γδT细胞的可行性、治疗潜力和显著的安全性。我们希望这能成为一种在未来治疗癌症的可行疗法。”(生物谷 Bioon.com)
参考资料:
Derek Lee et al. Unlocking the potential of allogeneic Vδ2 T cells for ovarian cancer therapy through CD16 biomarker selection and CAR/IL-15 engineering. Nature Communications, 2023, doi:10.1038/s41467-023-42619-2.
Scientists engineer potent immune cells for 'off-the-shelf' cancer immunotherapy
https://medicalxpress.com/news/2023-11-scientists-potent-immune-cells-off-the-shelf.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


