Nature子刊:人造病毒载体,容量更大成本更低,可用于基因编辑和治疗
来源:生物世界 2023-06-01 13:40
在概念验证实验中,研究团队生成了含有蛋白和核酸物质的人造病毒载体(AVV),用于展示在基因组改造方面的用途。 在实验室中,这一平台能成功递送全长抗肌萎缩蛋白基因(Dystrophin)到人类细胞中,
病毒(Virus)是我们地球上数量最多、分布最广的生物,它们也是一些最有效的生物机器。尽管病毒体积小,基因组成简单,但它们可以引起致命的感染和全球流行病,如艾滋病、流感和COVID-19等等。这是因为病毒进化出了高效机制,可以在短时间内复制和组装出后代,对于细菌病毒(噬菌体)来说,这个过程只需短短几分钟。
如果我们能够利用病毒的这些有效机制构建出人工病毒载体(Artificial Viral Vectors,AVV),用来递送治疗性分子,而不是在宿主细胞内复制,就能实现更好的细胞和基因治疗。尽管多年来科学家们进行了多次尝试,但AVV的开发仍处于早期阶段。
天然人类病毒,例如单链DNA病毒腺相关病毒(AAV)和单链RNA病毒慢病毒(Lentiviruse),已被设计并广泛应用于体外和体内的基因递送载体。例如,全世界最贵药物Hemgenix就是一款基于AAV病毒载体的血友病B型基因疗法。而FDA批准的6款CAR-T细胞疗法则全部基于慢病毒载体。
然而,这些天然病毒载体都有局限性,它们最多只能携带一到两个治疗性基因,很难再结合复杂修复所必需的额外治疗性分子。此外,这些病毒载体还存在一些安全性问题,例如对人类细胞的广泛感染性、在人体中预先存在的免疫原性,以及对人类基因组的潜在整合问题等。
2023年5月30日,美国天主教大学的研究人员在 Nature 子刊 Nature Communications 上发表了题为:Design of bacteriophage T4-based artificial viral vectors for human genome remodeling 的研究论文。
该研究报告了一种制作人工病毒载体(AVV)的方法,这种载体能进入人类细胞执行特定任务,可携带更大的基因,且制造成本相对更低,这种大容量、可定制化的纳米材料可以为未来基因疗法和定制化医疗的受试者带来前景。

在这项研究中,Venigalla Rao 团队设计了一种方法,用一类称为T4噬菌体、能感染细菌的病毒,制造人造病毒载体(AVV)。这类AVV有很大的内部容量和一个大的外表面,可编程和递送治疗性生物分子。
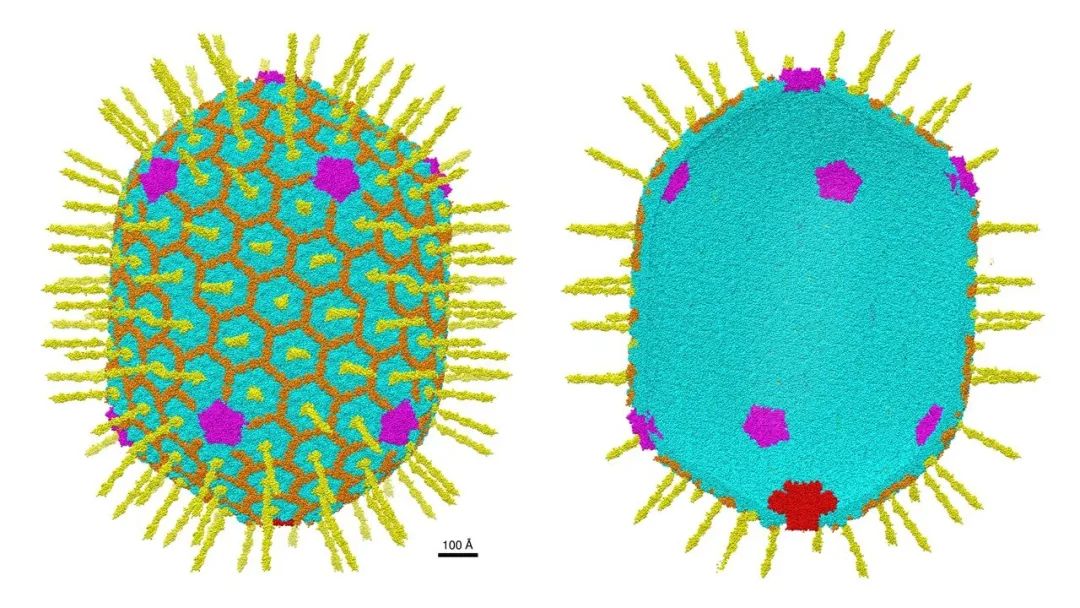
噬菌体T4-AVV的结构
在概念验证实验中,研究团队生成了含有蛋白和核酸物质的人造病毒载体(AVV),用于展示在基因组改造方面的用途。
在实验室中,这一平台能成功递送全长抗肌萎缩蛋白基因(Dystrophin)到人类细胞中,并执行各种分子操作改造人类基因组。
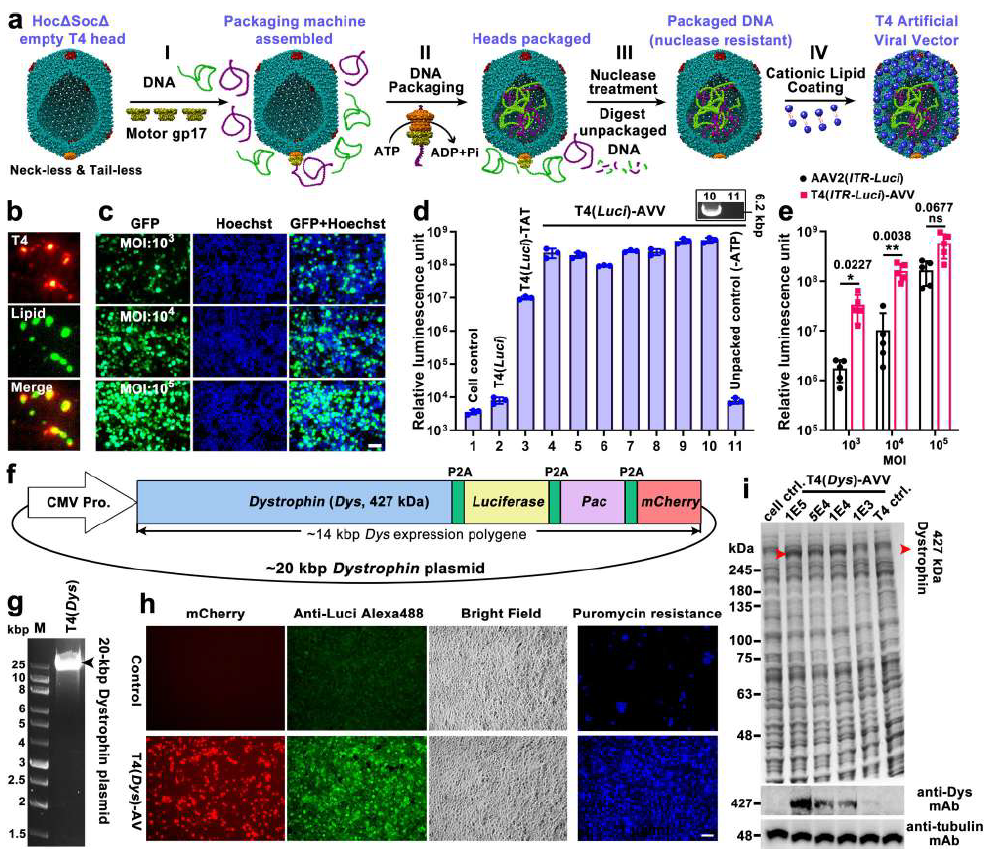
AVV用于递送全长Dystrophin基因
Dystrophin基因突变会导致杜氏肌营养不良(DMD),该基因非常巨大,有多达79个外显子,转录本长达14kb,远超病毒递送载体的装载极限,用于体内基因治疗递送的腺相关病毒(AAV)装载极限仅4.7kb,因此,难以通过腺相关病毒递送全长Dystrophin基因进行DMD治疗。
人造病毒载体(AVV)还能用来递送RNP和DNA,用于CRISPR-Cas9基因编辑及基因重组。还可以用来递送RNA,实现基因沉默、基因编辑,以及蛋白表达。
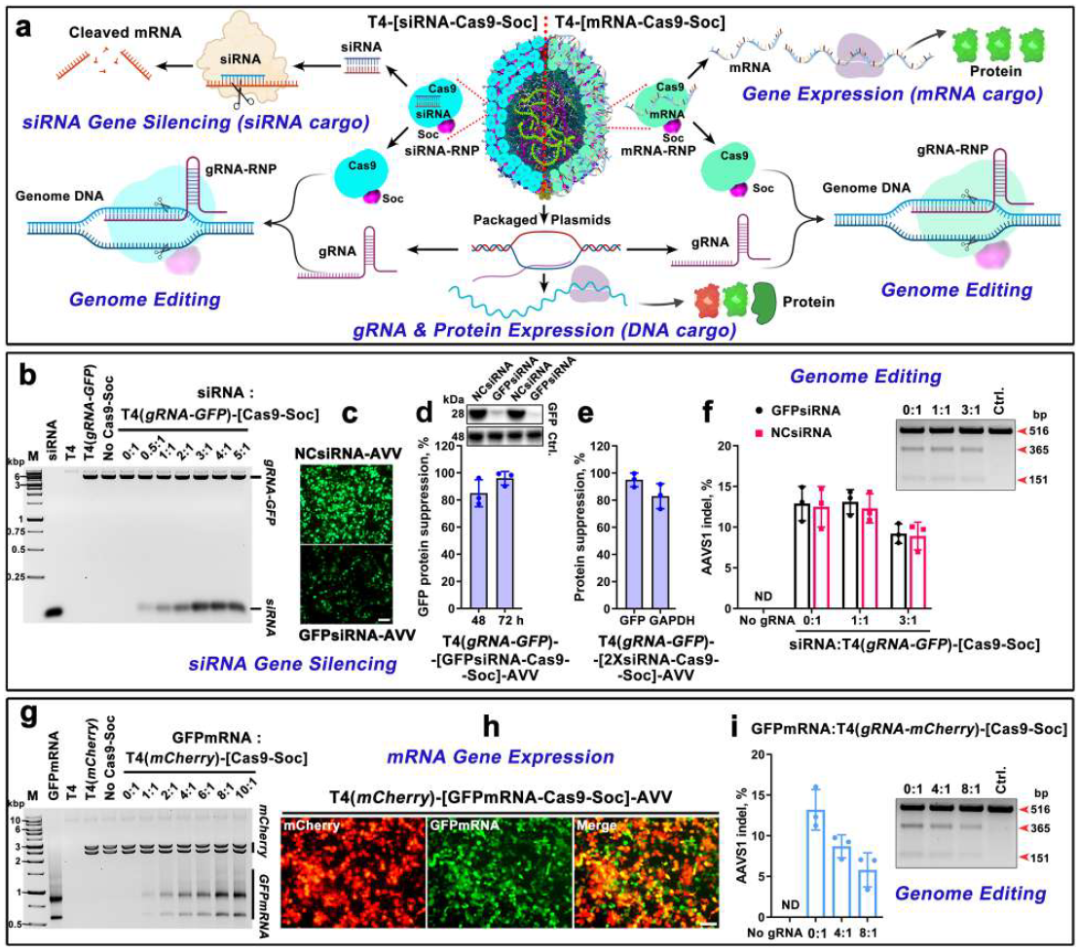
AVV用于RNA递送
此外,这种人造病毒载体(AVV)大量生产时成本不昂贵,并且这些纳米材料可以保持稳定数个月。研究团队总结道,尽管还需要进一步工作来评估该人造病毒载体的安全性,但这一方法已展现未来前景,可用于临床治疗人类疾病和罕见病。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


