Science:全基因组遗传筛选揭示了人类色素沉着的决定因素
来源:生物探索 2023-10-16 09:25
斯坦福大学Joanna Wysocka团队在Science 在线发表题为“A genome-wide genetic screen uncovers determinants o
斯坦福大学Joanna Wysocka团队在Science 在线发表题为“A genome-wide genetic screen uncovers determinants of human pigmentation”的研究论文,该研究利用黑色素的光散射特性对黑色素形成的调节因子进行了全基因组筛选。该研究确定了169个功能多样的基因,这些基因聚集在黑色素小体的生物发生、内体运输和基因调控上,其中135个与色素沉着有关,这是以前未知的。
该研究进一步揭示了KLF6作为体内调节黑色素小体成熟和色素沉着的转录因子的功能,以及内体运输蛋白COMMD3在调节黑色素小体pH中的功能。该研究揭示了大量的黑色素促进基因,对人类变异、细胞生物学和医学具有广泛的意义。

皮肤和头发颜色是遗传衍生的特征,在人群之间和人群内部高度可变,并由黑色素的数量、类型和分布决定。黑素细胞发育起源于胚胎神经嵴细胞,位于表皮,并在称为黑色素小体的亚细胞溶酶体相关细胞器中合成黑色素。在黑色素合成过程中,黑色素小体经历了典型的成熟阶段,其中I期黑色素小体含有腔内小泡,II期黑色素小体沉积PMEL原纤维,在其上发生黑色素生成,III期和IV期黑色素小体分别代表部分和完全黑色素化的黑色素小体。成熟的黑色素小体被细胞外运输到周围的表皮角质形成细胞,导致皮肤和头发色素沉着。
人类色素沉着的关键见解来自与色素沉着不足和色素沉着过多疾病相关的基因定位,以及人类正常范围皮肤和头发颜色变异的候选基因和全基因组关联研究(GWASs)。此外,对模式生物的研究,特别是对小鼠皮毛颜色的研究,已经揭示了与色素沉着有关的基因和途径,其中许多都集中在黑色素合成途径上。尽管如此,GWASs估计了在特定人群中发现的主要肤色遗传变异的累积贡献,只能解释所分析人群中相对较小的一部分肤色变异(23 - 35%)。同样,使用基于GWAS汇总统计的方法,作者估计来自UK Biobank (UKBB)的英国白人个体中,只有15.2%的肤色变异可以用与该人群的全基因组显著肤色GWAS匹配的基因组区域集来解释。综上所述,这些观察结果表明,尽管人们已经发现了控制人类色素沉着的关键基因座,但其他有贡献的基因座仍有待发现。
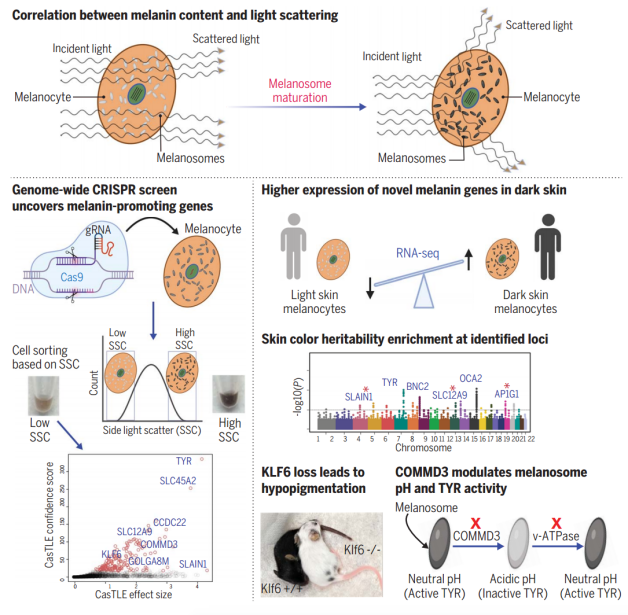
基因筛选发现了以前未确定的人类黑色素形成的位点(图源自Science )
黑色素是一种异质且结构不明确的生物聚合物,包括两种形式,即黑色或棕色的真黑色素和红色或黄色的现象黑色素。产生的黑色素的数量和类型决定了其物理化学性质,如高折射率,这构成了黑色素特有的吸光和散射特性的基础。这些被认为是保护皮肤免受阳光照射相关损伤的关键。
该研究证明了细胞黑色素浓度确实决定了色素细胞的光散射特性。利用这一特征,并使用SSC作为黑色素水平的代表,进行了基于CRISPR-Cas9的遗传筛选,以鉴定人类色素沉着的调节因子,从而发现了169个具有黑色素生成前功能的候选基因。该研究验证了筛选命中的一个子集,证实了它们在来自深色皮肤个体的原代黑素细胞中的转录上调,以及它们参与黑色素小体生物发生的不同阶段。此外,通过后续的功能研究,该研究发现转录因子KLF6在体内黑色素小体成熟和色素沉着中的作用,以及内体运输蛋白COMMD3在调节黑色素小体pH中的作用。因此,该研究将为进一步研究人类肤色多样性的遗传结构提供丰富的资源。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


