Nature子刊:复旦大学开发碱基编辑疗法,长期恢复隐性基因突变耳聋小鼠听力
来源:生物世界 2024-08-14 09:58
本研究提示,腺嘌呤碱基编辑器(ABE)可用于挽救听觉突触病病例的听力功能,从而为遗传性听力损失提供了潜在的精准治疗策略。
复旦大学附属眼耳鼻喉科医院舒易来教授团队在 Nature Biomedical Engineering 期刊发表了题为:A base editor for the long-term restoration of auditory function in mice with recessive profound deafness 的研究论文。
该研究利用腺嘌呤碱基编辑器(ABE)介导的基因编辑疗法有效修复了耳聋小鼠模型的Otof致病突变,恢复了88%的内耳内毛细胞的耳畸蛋白(Otoferlin)表达水平,同时改善了内耳内毛细胞的突触胞吐功能,并在长达1.5年的时间内将听力恢复到接近野生型的水平,且没有明显的脱靶效应。据悉,这是耳聋基因治疗领域,在动物模型中迄今观察时间最长的有效结果。

近年来,碱基编辑器(base editor)在高胆固醇血症、苯丙酮尿症、酪氨酸血症、早衰症、杜氏肌营养不良、Leber氏先天性黑蒙症、镰状细胞病及β-地中海贫血等多种遗传病的治疗中显示出巨大潜力。
值得注意的是,碱基编辑疗法已开始进入早期临床试验,用于治疗PCSK9基因突变引起的杂合子家族性高胆固醇血症,以及治疗急性淋巴细胞白血病。
碱基编辑器,例如腺嘌呤碱基编辑器(ABE)和胞嘧啶碱基编辑器(CBE),它们分别可以精确地将A·T转换为G·C,将C·G转换为T·A,而不会引起DNA双链断裂,被认为比基于CRISPR-Cas9的基因编辑技术更安全。
2020年6月,碱基编辑技术开创者刘如谦教授等人在 Science Translational Medicine 期刊发表论文【2】,通过双AAV载体递送胞嘧啶碱基编辑器(CBE),部分恢复了Tmc1基因隐性突变导致的完全耳聋小鼠的听力。这是人类首次通过基因编辑技术解决隐性遗传突变导致的遗传疾病,但治疗的小鼠只有部分听力恢复,并且这一效果在6周内减弱。这强调了在临床转化中进一步优化长期治疗疗效的必要性。
在这项最新研究中,研究团队评估了6种优化的腺嘌呤碱基编辑器(ABE)及sgRNA对Otof c.2482C>T(p.Q828X)从无义突变的A·T突变修复为野生型的G·C碱基对的效率。然后,研究团队将其中最有希望的ABE(由脱氨酶ABE7.10max和Cas9变体SpCas9-NG组成)-sgRNA组合包装到双载体腺相关病毒(AAV)血清型PHP.eB中(该AAV血清型对毛细胞转导效率高),并通过内耳注射给出生后1-3天的OtofQ828X/Q828X小鼠模型。
结果显示,这种ABE介导的基因编辑疗法有效修复了Otof致病突变,恢复了88%的内耳内毛细胞的耳畸蛋白(Otoferlin)表达水平,同时改善了内耳内毛细胞的突触胞吐功能,并在长达1.5年的时间内将听力恢复到接近野生型的水平,且没有明显的脱靶效应。
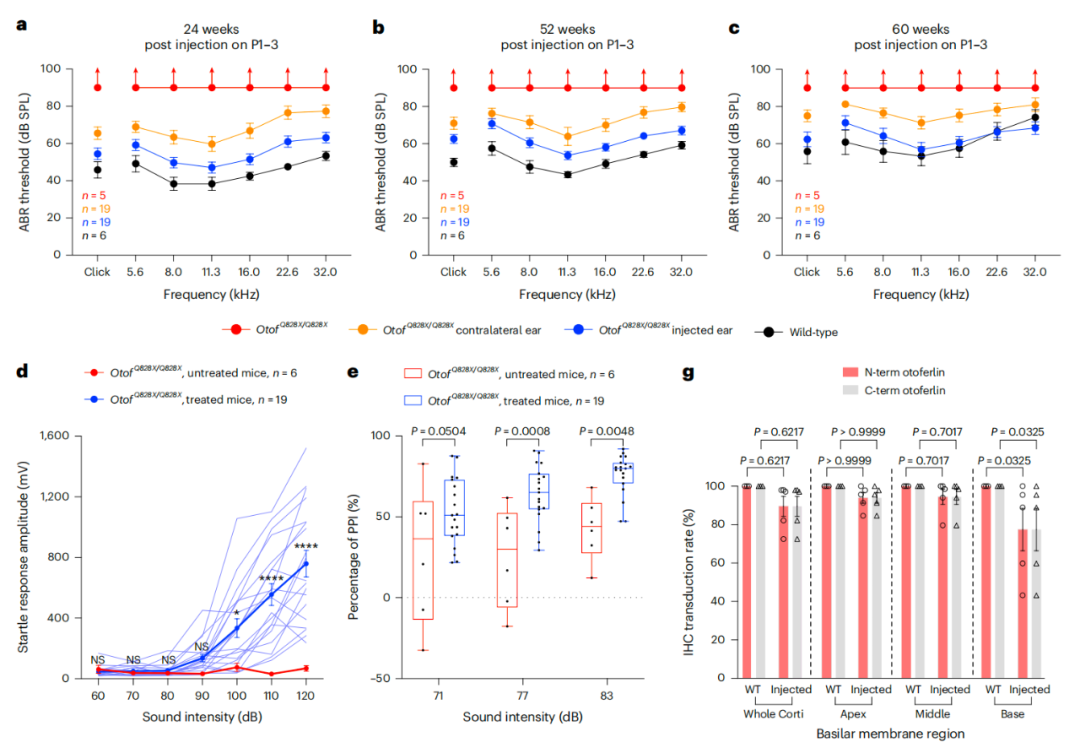
此外,即使给出生13-14天的OtofQ828X/Q828X小鼠模型治疗,它们的听觉功能也能得到显著恢复。研究团队还开发了针对人OTOF c.2485C>T(p.Q829X)位点的ABE治疗策略,将人源化OtofQ828X/Q828X小鼠模型的听力恢复到了与野生型小鼠相当的水平。
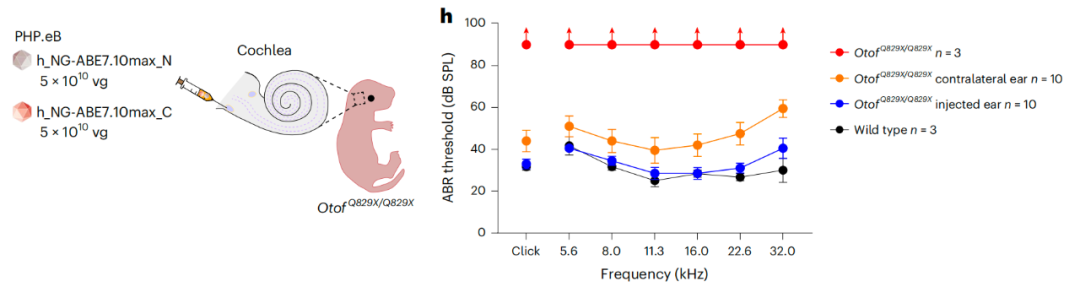
这些发现提示,腺嘌呤碱基编辑器(ABE)可用于挽救听觉突触病病例的听力功能,从而为遗传性听力损失提供了潜在的精准治疗策略。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


