由患者自身干细胞培育的人诱导多能干细胞来源心肌细胞(hiPSC-CMs),是修复心梗、心衰受损心脏的革命性方案 —— 它能为坏死心肌 “补新”,重建心脏收缩功能,被视为再生医学的核心希望。
但一个致命瓶颈长期阻碍临床转化:移植的 hiPSC-CMs 常因发育不成熟、电信号难以与原生心肌同步,引发致命性心律失常,让 “救命疗法” 暗藏风险。
近日,《Science》发表的一项重磅研究彻底破局:哈佛大学团队将临床获批的自组装肽 RADA16 与柔性网状纳米电子技术结合,既让移植细胞快速成熟、精准融入原生心脏,又能实时监测电活动,成功抑制心律失常,为心脏再生疗法装上 “安全锁”。

多年来,干细胞生物学家和心脏研究人员始终在探索改善 hiPSC-CMs 成熟与整合的方法,但核心难题在于:移植细胞一旦植入体内,就像 “黑箱”—— 其结构发育、电信号耦合情况无法直接观测,只能通过体表心电图等间接手段推测,难以精准优化方案。
而哈佛大学 Jia Liu 教授与 Richard T. Lee 教授团队的跨学科合作,恰好破解了这一困境:他们将 Liu 实验室开发的柔性网状纳米电子器件嵌入 hiPSC-CMs,打造出 “赛博格类器官” 平台,实现了对移植细胞长达数月的高分辨率监测。
这款柔性纳米电子器件堪称 “心脏微型监测仪”——它薄如蝉翼、可随心脏跳动灵活形变,32 通道的高密度微电极阵列能精准捕捉单个细胞的电信号,还能从原生心肌的强信号中,清晰分离出移植细胞的电活动特征,准确定位异步放电的 “问题细胞”。“此前没有技术能直接揭示心脏内部的移植细胞动态,”Jia Liu 表示,“我们的器件结合计算分析,实现了跳动心脏内移植细胞电活动的实时记录,这是前所未有的突破。”
借助这一平台,团队测试了多种优化策略,其中临床已获批作为止血剂的自组装肽 RADA16 表现最为亮眼。RADA16 能在体内自组装成纳米纤维支架,模拟心脏原生细胞外基质,为 hiPSC-CMs 提供 “生长土壤”。
研究人员将 RADA16 与 hiPSC-CMs 混合后移植到裸鼠心脏左心室壁,通过免疫荧光染色、空间转录组分析等技术发现,RADA16 带来了三重关键改善:一是促进血管新生,移植区域的宿主血管吻合率显著提升,CD31 阳性血管面积占比远超单独移植组,为细胞提供充足氧气和营养;二是加速结构成熟,hiPSC-CMs 的肌节排列更规整,成年型肌球蛋白重链(MYH7)表达上调,胎儿型(MYH6)表达下降,3 个月时的肌节长度和组织化程度已接近成年心肌;三是增强电信号耦合,缝隙连接蛋白 GJA1 表达升高,让细胞间电信号传递更顺畅。
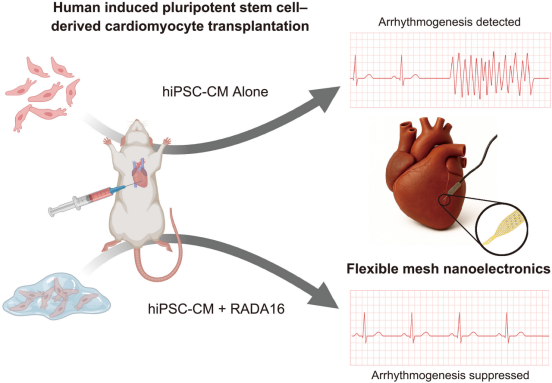
更关键的是柔性纳米电子的监测结果:单独移植 hiPSC-CMs 的对照组,80 天后仍存在明显的心律失常样自动放电——这些细胞以自身节律无序跳动,与原生心肌信号冲突;而 RADA16 处理组的自动放电现象大幅减少,135 天后几乎完全消失,电信号与原生心脏节律高度同步。功率谱密度分析显示,RADA16 组移植区域的电信号特征,已与原生心肌无显著差异,证实移植细胞真正融入了心脏电网络。
进一步机制研究表明,RADA16 的优势源于其 “生物支架 + 信号调控” 双重作用:它不仅为 hiPSC-CMs 提供物理支撑,还能通过与细胞表面整合素结合,调控基因表达——抑制起搏细胞相关的 HCN4 通道,上调钾通道 KCNJ2,减少异常自动起搏;同时促进抑制性神经元周围神经周网形成,稳定电信号微环境。而柔性纳米电子技术则解决了 “监测盲区”,让研究人员能精准追踪每一个时间节点的细胞状态,为优化方案提供直接依据。
“安全性是心脏细胞疗法进入临床的最大障碍,”Richard T. Lee 强调,“我们的研究不仅找到了解决心律失常的方案,更建立了一套治疗+监测一体化体系。” 值得一提的是,RADA16 已获批临床使用,安全性有充分保障,无需漫长的临床前毒性验证,为快速转化奠定了基础。此外,该平台还可推广至其他再生疗法——无论是肝脏、神经还是皮肤移植,只要涉及细胞整合与功能同步,都能通过嵌入式纳米电子实现精准监测。
这项研究的意义远超技术突破:它让心脏再生从 “盲目补细胞” 迈向 “精准修心脏”,既解决了 hiPSC-CMs 成熟慢、整合差的核心难题,又通过实时监测确保治疗安全,为心梗、心衰患者带来了 “补新 + 保安全” 的双重希望。未来,随着技术优化,有望实现 “个性化移植”——提取患者自身干细胞,经 RADA16 预处理后移植,再通过纳米电子实时监测疗效,调整治疗方案,真正实现心脏再生的精准化、安全化。对于全球数千万心脏病患者而言,这一突破让 “心脏重生” 不再是遥远梦想,而是即将到来的临床现实。
参考文献:
Aoyama J, Liu R, Zhang X, Zhu AY, Luanpaisanon P, Velayutham N, Garbern JC, Cao F, Barrera I, Fandl H, Sokol M, Dasariraju S, Gil ES, Aleksi E, Amanuma T, Saucerman JJ, Chen F, Liu J, Lee RT. Flexible nanoelectronics reveal arrhythmogenesis in transplanted human cardiomyocytes. Science. 2025 Nov 13;390(6774):eadw4612. doi: 10.1126/science.adw4612. Epub 2025 Nov 13. PMID: 41100583.
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。




