10年来首个新一类降糖药!美国FDA批准礼来GIP/GLP-1受体激动剂Mounjaro:显著降低血糖和体重!
来源:生物谷原创 2022-05-14 13:56
Mounjaro将2种促胰岛素的作用整合至一个单分子中,代表了治疗2型糖尿病的一类新型药物。

2022年05月13日讯 /生物谷BIOON/ --礼来(Eli Lilly)近日宣布,美国食品和药物管理局(FDA)已批准Mounjaro(tirzepatide)注射液,该药是一种新的、每周一次的GIP和GLP-1受体激动剂,辅助饮食和运动,用于改善2型糖尿病(T2D)成人患者的血糖控制。Mounjaro尚未在有胰腺炎病史的患者中进行研究,且不适用于1型糖尿病(T1D)患者。需要注意的是,Mounjaro的药物标签中含有一则关于甲状腺C细胞肿瘤的黑框警告。Mounjaro禁用于有甲状腺髓样癌个人或家族史、或患有多发性内分泌腺瘤综合征(MEN)2型的患者。
值得一提的是,Mounjaro是美国FDA批准的第一个也是唯一一个GIP/GLP-1受体激动剂,该药同时代表着近十年来获批上市的首个新一类降糖药物。根据去年10月发布的三季度财报所披露的,礼来向FDA递交了一张优先审查凭证(PRV)来加速tirzepatide审查,该PRV可将审查周期缩短4个月。目前,tirzepatide也正在接受欧盟、日本和其他几个市场的监管审查。
Mounjaro(tirzepatide)是由礼来开发的一种新型每周一次的葡萄糖依赖性促胰岛素多肽(GIP,又名:胃抑制多肽)受体和胰高血糖素样肽-1(GLP-1)受体双重激动剂。tirzepatide是一种单一分子,可激活人体的GIP和GLP-1受体。GIP和GLP-1均为天然的肠促胰岛素激素,能够促进胰岛素分泌。tirzepatide将2种促胰岛素的作用整合至一个单分子中,代表了治疗2型糖尿病的一类新型药物。
在3期SURPASS临床试验中,与所有对照相比,tirzepatide提供了卓越且一致的血糖(A1C)降低。此外,在关键次要终点方面,与所有对照相比,tirzepatide治疗组表现出显著更大程度的体重减轻。
Mounjaro预计将在未来几周内在美国上市,该产品将有6种剂量强度(2.5mg,5mg,7.5mg,10mg,12.5mg,15mg),并将采用礼来成熟的自动注射笔进行注射治疗。
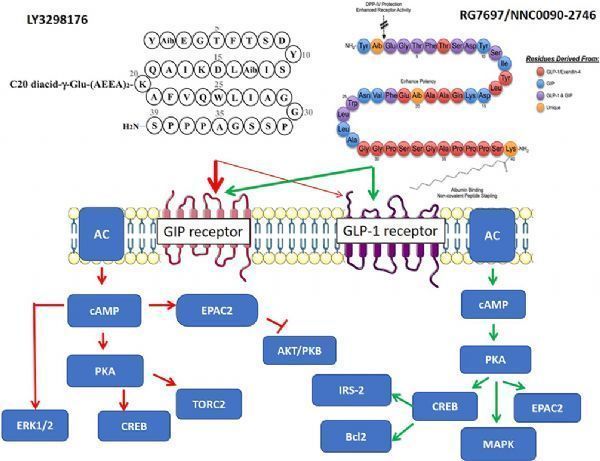
tirzepatide(LY3298176,图片来源于文献:PMID-31686879)
此次批准,基于SURPASS 3期全球临床开发项目的数据。该项目于2018年底启动,包括5项全球注册3期试验,纳入的阳性对照药物包括semaglutide 1mg注射液、甘精胰岛素、德谷胰岛素。对Mounjaro 5mg、10mg、15mg单药治疗或联合常用降糖药(包括二甲双胍、SGLT2抑制剂、磺脲类、甘精胰岛素)进行了疗效评估。
数据显示,接受Mounjaro 5mg治疗的患者实现平均血糖(A1C)水平降低1.8%至2.1%;Mounjaro 10mg和15mg治疗的患者实现平均血糖(A1C)水平降低1.7%至2.4%。此外,所有SURPASS研究的关键次要终点——体重减轻方面,接受Mounjaro治疗的患者平均体重减轻12磅(剂量5mg)至25磅(剂量15mg)。
安全性方面,SURPASS项目中,Mounjaro治疗的患者中发生率≥5%的不良事件包括恶心、腹泻、食欲下降、呕吐、便秘、消化不良和胃(腹)痛。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


