压力为什么会让人 emo?Nat Commun:剑桥团队揪出致郁关键,原来是脑膜里的免疫细胞在“搞事情”!
来源:生物谷原创 2025-09-05 14:04
本文研究不仅揭示了慢性压力如何通过影响大脑的免疫环境来促成抑郁,还为开发新的治疗方法提供了可能的靶点。
在快节奏的现代生活里,“压力大” 成了很多人的口头禅,但你可能没意识到,那些日积月累的慢性压力,正通过一种隐蔽的免疫机制悄悄影响情绪——甚至诱发抑郁和焦虑。
近日,英国剑桥大学与美国国立精神卫生研究院(NIH)的团队在《Nature Communications》发表研究,终于揭开了这层神秘面纱:慢性压力会促使颅骨骨髓中的中性粒细胞通过血管通道 “迁移” 到脑膜(包裹大脑和脊髓的保护膜),这些免疫细胞在脑膜聚集后,会激活I 型干扰素(IFN-I)信号通路,最终引发抑郁样行为。这一发现不仅填补了 “慢性炎症致郁” 的机制空白,更给三分之一对现有抗抑郁药无效的患者带来了新的治疗希望。

世界卫生组织(WHO)数据显示,全球约 10 亿人在一生中会遭遇抑郁、焦虑等情绪障碍,这些疾病不仅拉低生活质量,还造成沉重的社会负担。尽管现有抗抑郁药能缓解部分症状,但约 30% 患者属于 “难治性抑郁”,根本原因在于我们对 “压力-炎症-抑郁”的具体链条知之甚少。近年来,越来越多研究提示慢性炎症是重要推手——当免疫系统长期处于 “过度活跃” 状态,会悄悄破坏包括大脑在内的器官功能,而这次研究首次锁定了 “脑膜中性粒细胞” 这个关键角色。
研究团队用 “慢性社会失败压力(CSD)” 模型模拟人类长期心理压力:将雄性 C57BL/6J 小鼠(“入侵者”)每天与攻击性 CD-1 小鼠(“居民”)接触 5 分钟,持续 14 天,期间小鼠可通过穿孔屏障相互感知(视觉、嗅觉、听觉),但避免严重伤害。
结果显示,约 70% 小鼠会表现出 “易感” 特征——在尿液气味标记(USM)测试中对雌性尿液的兴趣降低(性快感缺失),社交互动(SI)测试中主动接近其他小鼠的次数减少,同时在开放场(OF)和明暗箱(LD)测试中表现出明显焦虑(更少进入中心区域、更少穿越到光亮侧);另有 30% 小鼠属于 “抗压型”,SI 指数≥2,基本不受压力影响,这与人类面对压力的个体差异高度相似。
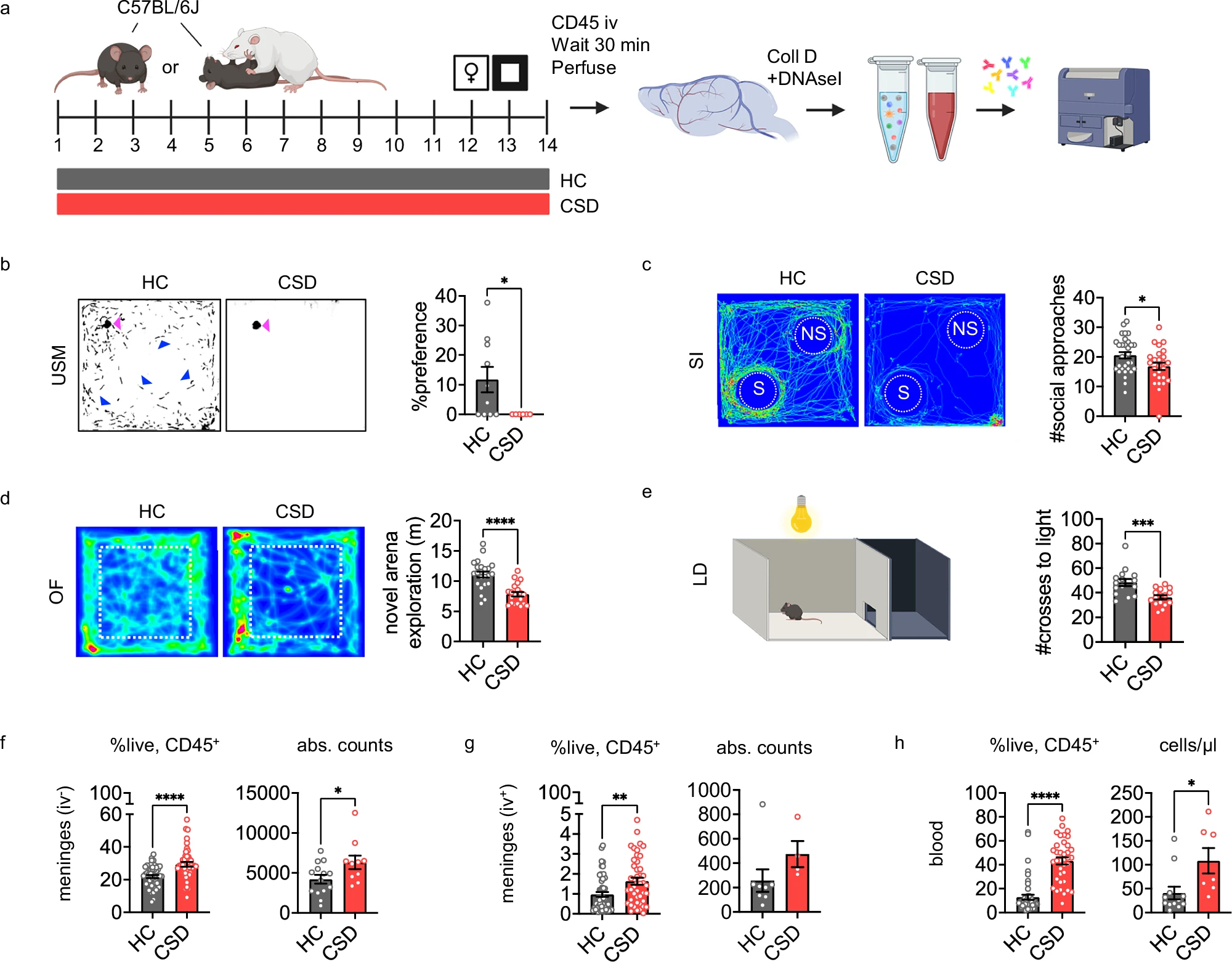
脑膜中中性粒细胞在慢性社会失败(CSD)压力后会升高 这就会导致类似抑郁症样的行为改变
深入观察发现,“易感” 小鼠的脑膜中,中性粒细胞数量显著升高 —— 非血管区域(iv-)的中性粒细胞增加 1.3 倍,血管接触区域(iv+)增加 1.7 倍,而血液中中性粒细胞更是暴增 5.6 倍。更特别的是,这些中性粒细胞并非来自血液循环,而是直接源于颅骨骨髓:通过组织透明化技术(CUBIC)观察 LysM-GFP + 小鼠(中性粒细胞呈绿色荧光),研究人员清晰看到,CSD 小鼠颅骨与脑膜相连的血管通道中,绿色荧光细胞数量比对照组多 30%,且脑膜中性粒细胞的基因表达模式与颅骨骨髓中性粒细胞高度相似(Pearson 相关系数 0.83),与胫骨骨髓或血液中性粒细胞关联甚微。这意味着,颅骨骨髓是脑膜中性粒细胞的 “专属储备库”,慢性压力会直接触发它们 “迁移” 到脑膜。
更关键的是,这些聚集在脑膜的中性粒细胞会 “激活警报”——单细胞 RNA 测序(scRNA-seq)显示,它们中Ifitm2和Ifitm3基因(I 型干扰素信号通路的核心基因)表达显著升高,且 MHCII 分子(负责抗原呈递的关键蛋白)表达降低 2.3 倍。I 型干扰素通路早已被证实与抑郁相关:比如治疗丙肝的 I 型干扰素药物,常会诱发患者抑郁症状。
研究团队进一步用 IFNAR(I 型干扰素受体)阻断抗体处理小鼠,发现奇迹发生了:CSD 小鼠脑膜中的中性粒细胞数量显著减少,USM 测试中对雌性尿液的标记行为恢复到与健康小鼠(HC)无差异,开放场测试中穿越到中心区域的次数增加 40%,焦虑和快感缺失症状明显缓解。
值得注意的是,脑膜中的炎症状态比血液更 “持久”:压力停止后,血液中性粒细胞 8 小时就恢复正常,而脑膜中性粒细胞要 24 小时后才开始下降,7 天才能回到基线水平。研究还发现,CSD 小鼠的脑膜中性粒细胞多为 “未成熟型”——细胞体积更大(比正常大 3 倍)、颗粒含量更多,这种未成熟细胞不仅促炎性更强,还可能因刚性增加 “卡在” 脑血管中,进一步加重局部炎症。此外,脑膜中 B 细胞数量会因 CSD 减少 30%,而 B 细胞的缺失会间接增强 I 型干扰素信号,形成 “中性粒细胞聚集 - B 细胞减少 - 炎症加剧” 的恶性循环。
“我们早就知道压力会改变中性粒细胞行为,但不知道它们去了哪里、做了什么。” 研究共同第一作者 Mary-Ellen Lynall 博士说,“这次发现这些‘免疫急救员’会从颅骨骨髓直接跑到脑膜,在这里搅乱情绪,就像感冒时免疫系统让你没力气、不想社交一样,长期的脑膜炎症会把‘暂时不适’变成‘持续抑郁’。”
这一发现还能解释为何抑郁常伴随中风、阿尔茨海默病等神经疾病——这些疾病都会导致脑损伤,而损伤会像慢性压力一样,触发颅骨骨髓释放中性粒细胞,进而激活 I 型干扰素通路,形成 “损伤 - 炎症 - 抑郁” 的连锁反应。未来,通过阻断 I 型干扰素信号通路、靶向清除脑膜中性粒细胞,或许能为 “难治性抑郁” 患者提供新疗法——毕竟,比起调节大脑化学物质,调控外周免疫通路可能更精准、副作用更少。
目前,研究团队正计划在雌性小鼠中验证这一机制(女性抑郁发病率更高,可能存在性别差异),同时探索颅骨骨髓中性粒细胞的 “迁移开关”。或许不久的将来,我们能通过简单的免疫调控,让大脑摆脱 “压力炎症” 的困扰,真正实现 “解压不 emo”。(生物谷Bioon.com)
参考文献:
Kigar, S.L., Lynall, ME., DePuyt, A.E. et al. Chronic social defeat stress induces meningeal neutrophilia via type I interferon signaling in male mice. Nat Commun 16, 8153 (2025). doi:10.1038/s41467-025-62840-5
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


