NEJM、ASCO双重磅:新型抗体偶联药物关键研究成功,将打破HER2阴阳二分僵局
来源:奇点糕 2022-06-13 10:40
在不考虑HR状态的情况下,与医生选择的化疗相比,曲妥珠单抗-deruxtecan显著延长了HER2低表达乳腺癌患者的无进展生存期和总生存期,有望改善超过半数HER2阴性乳腺癌患者的治疗结果。
刚刚落幕的2022年美国临床肿瘤学会(ASCO)年会,可谓群星荟萃,神仙打架!要知道,天下苦癌久矣!ASCO陆续发布的一系列重磅研究成果,不仅极大地鼓舞了患者和研发人员的积极性,也是对癌症治疗局势的精辟分析,有益于癌症治疗重新排兵布阵。
针对HER2低表达乳腺癌的治疗,美国纪念斯隆-凯特琳癌症中心的Shanu Modi教授报告了抗体偶联药物曲妥珠单抗-deruxtecan(又称T-DXd/DS-8201)的III期临床试验结果,这项名为DESTINY-Breast04的研究成果同步发表于《新英格兰医学杂志》。
研究显示,曲妥珠单抗-deruxtecan能够显著改善HER2低表达乳腺癌患者的无进展生存期和总生存期,将疾病进展或死亡风险降低近一半(HR=0.51,p< 0.001),死亡风险显著降低36%(HR=0.64,p=0.003)[1]。这也标志着HER2低表达晚期乳腺癌患者,很有希望迎来靶向治疗的全新时代!

论文首页
根据肿瘤细胞表达的受体类型,乳腺癌通常主要分为以下三类:人表皮生长因子受体2(HER2)阳性,激素受体(HR)阳性/HER2阴性和三阴性乳腺癌(即HR阴性/HER2阴性)。
然而,多项研究表明,约60%的HER2阴性转移性乳腺癌,实际上属于HER2低表达亚型,即免疫组化(IHC)评分为1+,或IHC评分为2+且原位杂交(ISH)为阴性[2-3]。
HER2低表达患者是一个存在异质性的群体,其中包括HR阳性和HR阴性两种亚型患者,但这两种亚型的患者,均未能从目前可用的HER2靶向疗法中获益[4-5],而且在初次治疗发生进展后,她们的治疗选择也非常有限,以姑息化疗为主[6]。而破解这部分患者缺少靶向治疗药物困局的,就是抗体偶联药物。
抗体偶联药物(ADC)是抗癌界的“导弹”担当,通常由三个元件构成。拿本次报告中的曲妥珠单抗-deruxtecan来说,人源化抗HER2曲妥珠单抗就是精准识别乳腺癌细胞的“定位仪”;拓扑异构酶I抑制剂deruxtecan则是杀伤癌细胞的“弹头”;而四肽基可切割的连接子相当于“弹体”,用于连接定位仪与弹头[7-9]。
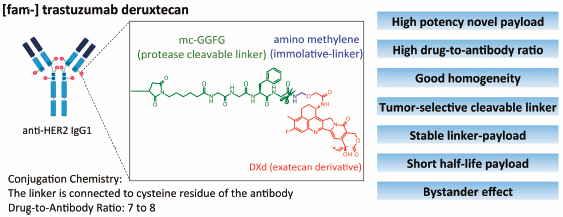
曲妥珠单抗-deruxtecan的结构示意图[7]
此前, 1期和2期临床试验结果已经表明,曲妥珠单抗-deruxtecan对HER2低表达的转移性乳腺癌患者具有显著的治疗效果,总缓解率约为37.0%-37.5%,中位无进展生存期约为6.3-11.1个月[10-12]。
为进一步评估曲妥珠单抗-deruxtecan与医师选择的化疗方案在HER2低表达的转移性乳腺癌患者中的疗效和安全性,就有了随机、两组、开放标签的3期临床研究DESTINY-Breast04。
DESTINY-Breast04研究纳入了557例接受过1-2线化疗的HER2低表达转移性乳腺癌患者,其中,494例(88.7%)为HR阳性,63例(11.3%)为HR阴性。所有患者按2 : 1随机分配成两组,并分别接受曲妥珠单抗-deruxtecan或医师选择的化疗方案。
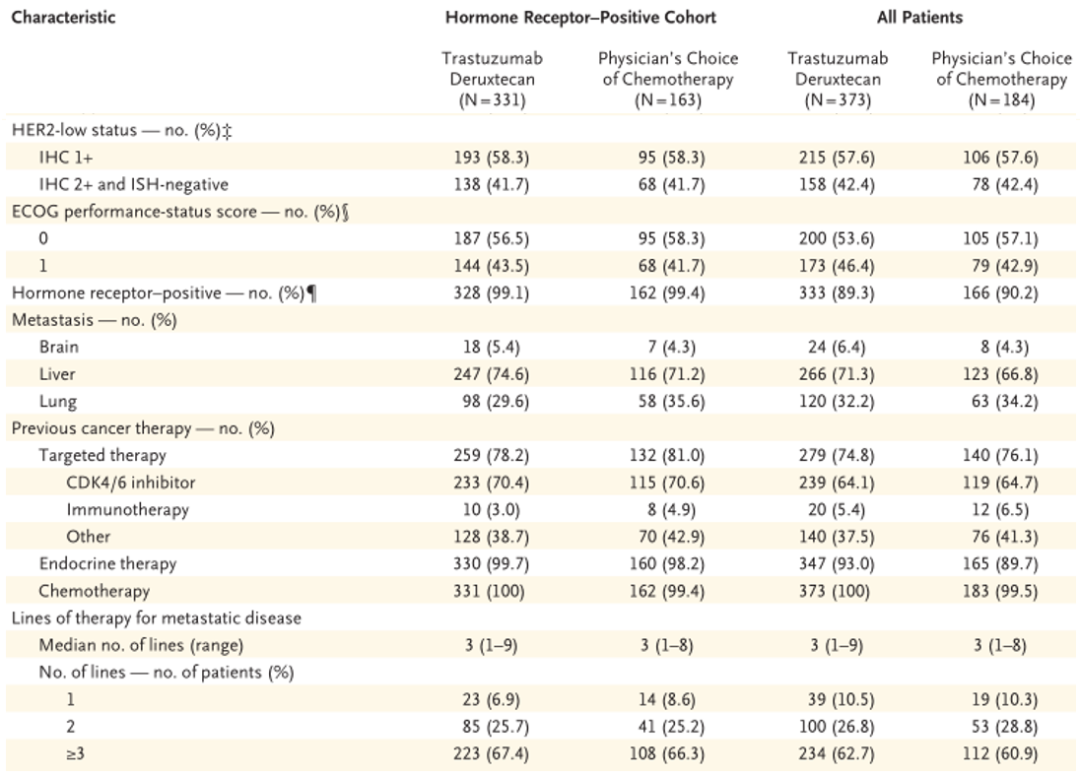
HR阳性队列及所有患者基线时的临床特征
在HR阳性队列中,曲妥珠单抗-deruxtecan组患者的中位无进展生存期为10.1个月,而化疗组患者的中位无进展生存期为5.4个月。与医师选择的化疗方案相比,曲妥珠单抗-deruxtecan将疾病进展或死亡风险降低了49%(HR = 0.51,p < 0.001)。
此外,两组患者的中位总生存期分别为23.9个月和17.5个月,缓解率分别为52.6%和16.3%。与医师选择的化疗方案相比,曲妥珠单抗-deruxtecan可将死亡风险降低36%(HR = 0.64,p = 0.003)。
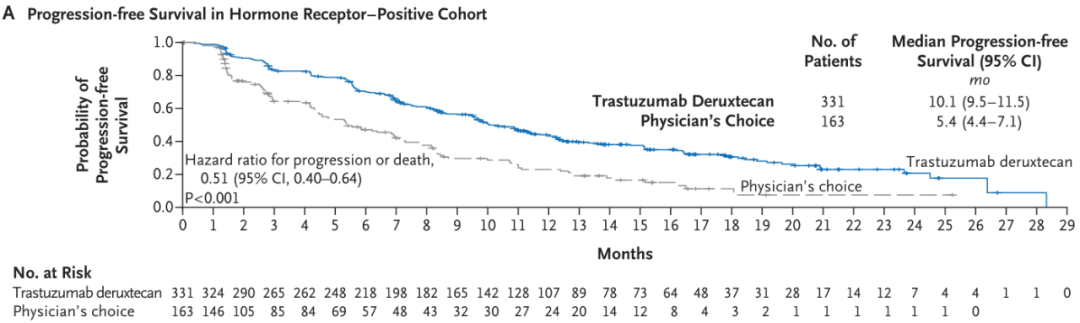
HR阳性队列中,曲妥珠单抗-deruxtecan组与化疗组患者无进展生存期的Kaplan-Meier曲线
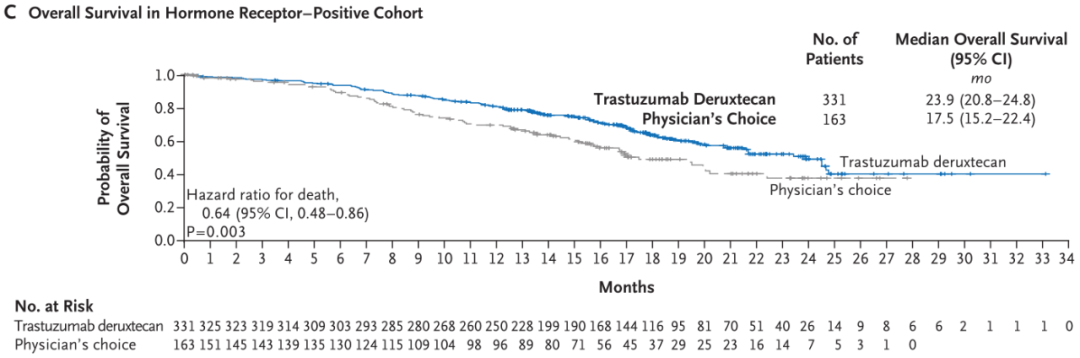
HR阳性队列中,曲妥珠单抗-deruxtecan与化疗组患者总生存期的Kaplan-Meier曲线
在所有HER2低表达乳腺癌患者队列中,曲妥珠单抗-deruxtecan组与化疗组患者的中位无进展生存期分别为9.9个月和5.1个月。与医师选择的化疗方案相比,曲妥珠单抗-deruxtecan可将疾病进展或死亡风险降低一半(HR = 0.50,p < 0.001)。
同样在整体队列中,曲妥珠单抗-deruxtecan组与化疗组患者的中位总生存期分别为23.4个月和16.8个月,相较于医师选择的化疗方案,曲妥珠单抗-deruxtecan可将死亡风险降低36%(HR = 0.64,p = 0.003)。
在HR阴性队列中,曲妥珠单抗-deruxtecan组与化疗组患者的中位无进展生存期分别为8.5个月和2.9个月,总缓解率分别为50%和16.7%,中位总生存期分别为18.2个月和8.3个月,与医师选择的化疗方案相比,曲妥珠单抗-deruxtecan将死亡风险降低了54%(HR = 0.46)。
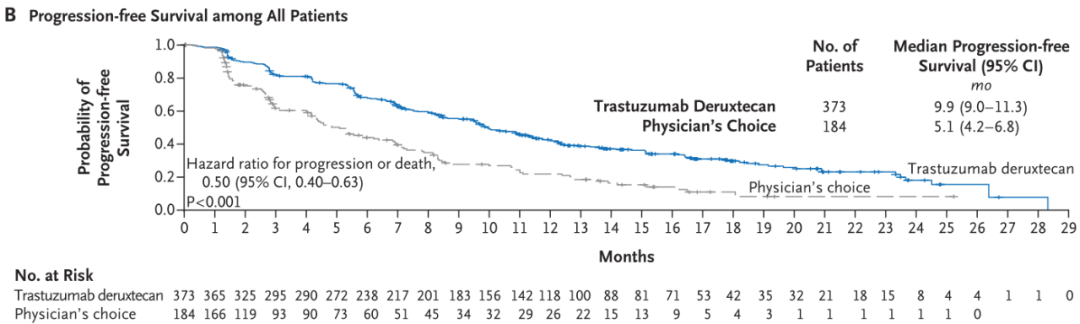
整体队列中,曲妥珠单抗-deruxtecan与化疗组患者无进展生存期的Kaplan-Meier曲线
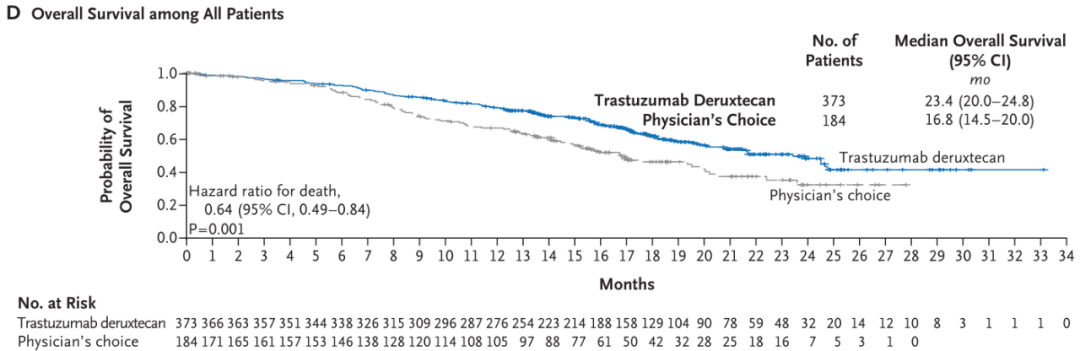
整体队列中,曲妥珠单抗-deruxtecan与化疗组患者总生存期的Kaplan-Meier曲线
上述结果表明,对于HER2低表达的转移性乳腺癌患者,曲妥珠单抗-deruxtecan比化疗的治疗效果更佳,能显著改善患者的总生存期和无进展生存期,并降低一半死亡风险。
安全高效,安全高效,这绝不是喊口号,新药的安全性评价可马虎不得!
DESTINY-Breast04研究结果显示,曲妥珠单抗-deruxtecan组与化疗组患者发生3级或以上不良事件的比例分别为52.6%和67.4%。曲妥珠单抗-deruxtecan常见的药物相关不良事件主要包括恶心(73.0%)、疲劳(47.7%)、脱发(37.7%),其中,45例患者(12.1%)发生了药物相关的间质性肺病或肺炎,死亡3例(0.8%)。
曲妥珠单抗-deruxtecan组与化疗组的不良事件发生率相似,两组最常见的3级或以上不良事件均为中性粒细胞减少,但发热性中性粒细胞减少的发生率较低。此外,药物相关的间质性肺疾病或肺炎多为轻度或中度,总体发生率与既往研究基本一致。
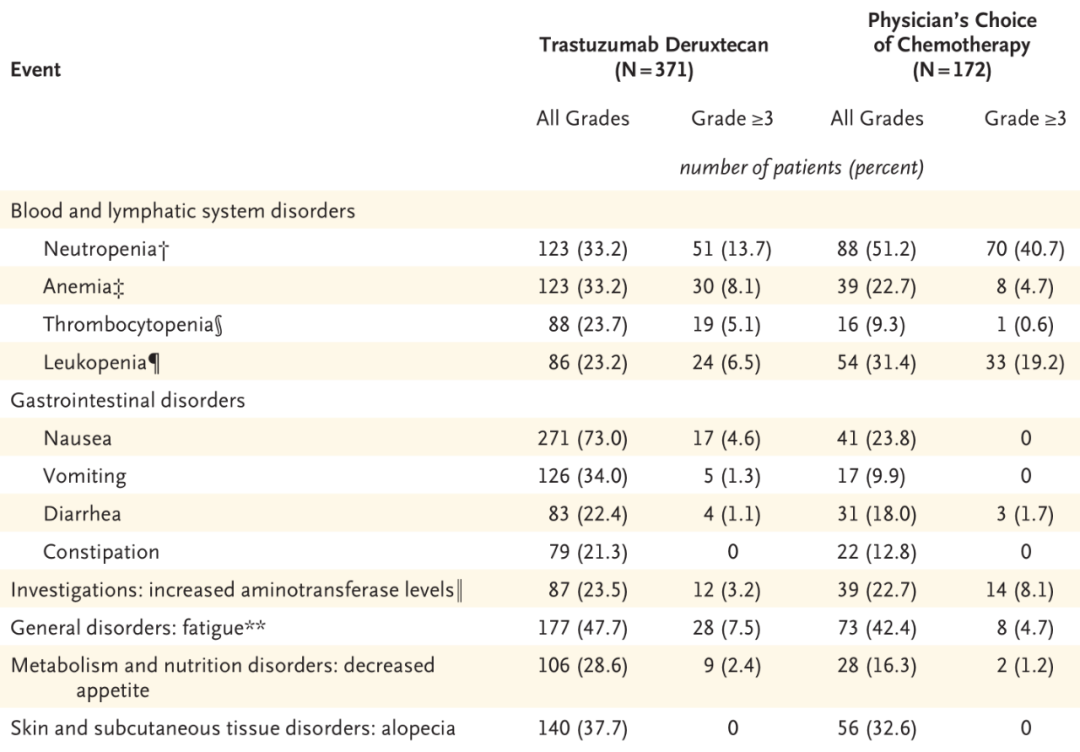
患者发生的药物相关不良事件
总的来说,在不考虑HR状态的情况下,与医生选择的化疗相比,曲妥珠单抗-deruxtecan显著延长了HER2低表达乳腺癌患者的无进展生存期和总生存期,有望改善超过半数HER2阴性乳腺癌患者的治疗结果。这项研究结果无疑是振奋人心的,因为这不仅意味着传统上难治性乳腺癌患者有药可用,也从根本上改变了我们对HER2表达及转移性乳腺癌分类的看法。
参考文献:
1.Modi S, Jacot W, Yamashita T, et al. Trastuzumab Deruxtecan in Previously Treated HER2-Low Advanced Breast Cancer. N Engl J Med. 2022;10.1056/NEJMoa2203690.
2.Schettini F, Chic N, Brasó-Maristany F, et al. Clinical, pathological, and PAM50 gene expression features of HER2-low breast cancer. NPJ Breast Cancer. 2021;7(1):1.
3.Tarantino P, Hamilton E, Tolaney SM, et al. HER2-low breast cancer: pathological and clinical landscape. J Clin Oncol. 2020; 38: 1951-62.
4.Fehrenbacher L, Cecchini RS, Geyer CE Jr, et al. NSABP B-47/NRG oncology phase III randomized trial comparing adjuvant chemotherapy with or without trastuzumab in high-risk invasive breast cancer negative for HER2 by FISH and with IHC 1+ or 2. J Clin Oncol. 2020; 38: 444-53.
5.Burris HA 3rd, Rugo HS, Vukelja SJ, et al. Phase II study of the antibody drug conjugate trastuzumab-DM1 for the treatment of human epidermal growth factor receptor 2 (HER2)-positive breast cancer after prior HER2-directed therapy. J Clin Oncol. 2011;29(4):398-405.
6.Harbeck N, Penault-Llorca F, Cortes J, et al. Breast cancer. Nat Rev Dis Primers. 2019;5(1):66.
7.Nakada T, Sugihara K, Jikoh T, Abe Y, Agatsuma T. The Latest Research and Development into the Antibody-Drug Conjugate, [fam-] Trastuzumab Deruxtecan (DS-8201a), for HER2 Cancer Therapy. Chem Pharm Bull (Tokyo). 2019;67(3):173-185.
8.Ogitani Y, Aida T, Hagihara K, et al. DS-8201a, A Novel HER2-Targeting ADC with a Novel DNA Topoisomerase I Inhibitor, Demonstrates a Promising Antitumor Efficacy with Differentiation from T-DM1. Clin Cancer Res. 2016;22(20):5097-5108.
9.Modi S, Park H, Murthy RK, et al. Antitumor Activity and Safety of Trastuzumab Deruxtecan in Patients With HER2-Low-Expressing Advanced Breast Cancer: Results From a Phase Ib Study. J Clin Oncol. 2020;38(17):1887-1896.
10.Diéras V, Deluche E, Lusque A, et al. Trastuzumab deruxtecan (T-DXd) for advanced breast cancer patients (ABC), regardless HER2 status: a phase II study with biomarkers analysis (DAISY). Cancer Res 2022; 82: PD8-02. abstract.
11.Hamilton E, Shapiro CL, Petrylak D, et al. Trastuzumab deruxtecan (T-DXd; DS-8201) with nivolumab in patients with HER2-expressing, advanced breast cancer: a 2-part, phase 1b, multicenter, open-label study. Cancer Res 2021; 81: PD3-07. abstract.
12.Aogi K, Iwata H, Masuda N, et al. A phase II study of eribulin in Japanese patients with heavily pretreated metastatic breast cancer. Ann Oncol. 2012;23(6):1441-1448.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


