TMEM147在肝细胞癌中的机制被揭示
肝细胞癌(HCC)是肝细胞的原发性恶性肿瘤,是最常见的肝脏恶性肿瘤。尽管存在多种治疗方式,但手术切除已被发现对早期HCC最有效。然而,HCC患者的预后仍然很差。
2023-12-06
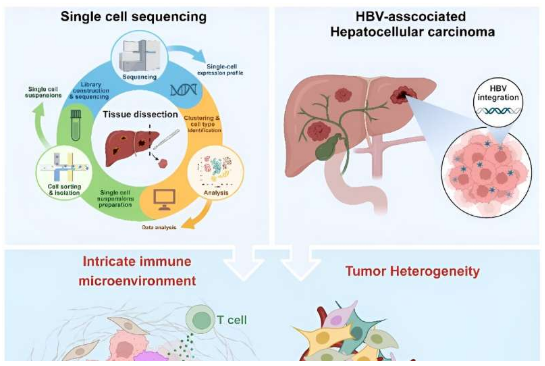
MedComm—Oncol:基于单细胞测序技术揭示HBV所致人类肝细胞癌的新见解
来自四川大学等机构的科学家们概述了科学家们通过单细胞RNA测序分析在肝细胞癌研究领域取得的进展。
2023-12-19
Mol Cancer:cfDNA甲基化检测可用于肝细胞癌(HCC)液体活检
为了对抗肝细胞癌(HCC)发病率的上升,需要改进检测方法。在目前的监测技术中,超声常与血清甲胎蛋白(AFP)水平联合使用。
2023-11-23
细胞外囊泡衍生物作为早期肝细胞癌的无创诊断生物标志物
据报道,肝癌是2020年全球第六大最常诊断的癌症。虽然各种研究加深了我们对HCC癌变的认识,但在乙型肝炎、丙型肝炎和肝硬化(LC)高危人群中,HCC的监测主要依靠腹部超声检查和血甲胎蛋白(AFP)的测
2023-12-06
Acta Pharm Sin B:Gal1沉默在肝细胞癌治疗中具有很好的潜力
本研究表明Gal1不仅是HCC的生物标志物;它还能预测HCC患者的生存结果。靶向Gal1在预防和治疗HCC方面是有效的,并且具有转化潜力,作用机制可以有很多。
2024-03-28
Hepatology:识别出能指示机体患肝细胞癌风险的特殊肿瘤生物标志物
本文研究结果表明,丙肝相关的肝细胞癌的发生对于自然杀伤性细胞的印记会产生深远的影响,TIM-3和CD38在自然杀伤性细胞中的持续共表达或许能作为丙肝相关肝细胞癌发生的早期指标。
2024-03-15
研究发现促进肝细胞癌远处转移的新机制
针对这一问题,研究人员系统性阐明了CD51作为肿瘤转移关键分子,存在一种潜在的作用机制“逃逸”了西仑吉肽的抑制作用。具体而言,CD51可接受γ-分泌酶(γ-secretase)介导的跨膜切割并产生游离
2023-09-11
Theranostics: 维生素D结合蛋白(VDBP)结合Twist1抑制肝细胞癌血管生成模拟
该研究揭示了VDBP是HCC患者重要的预后生物标志物,并发现它是增强免疫治疗疗效的治疗靶点。
2024-01-31