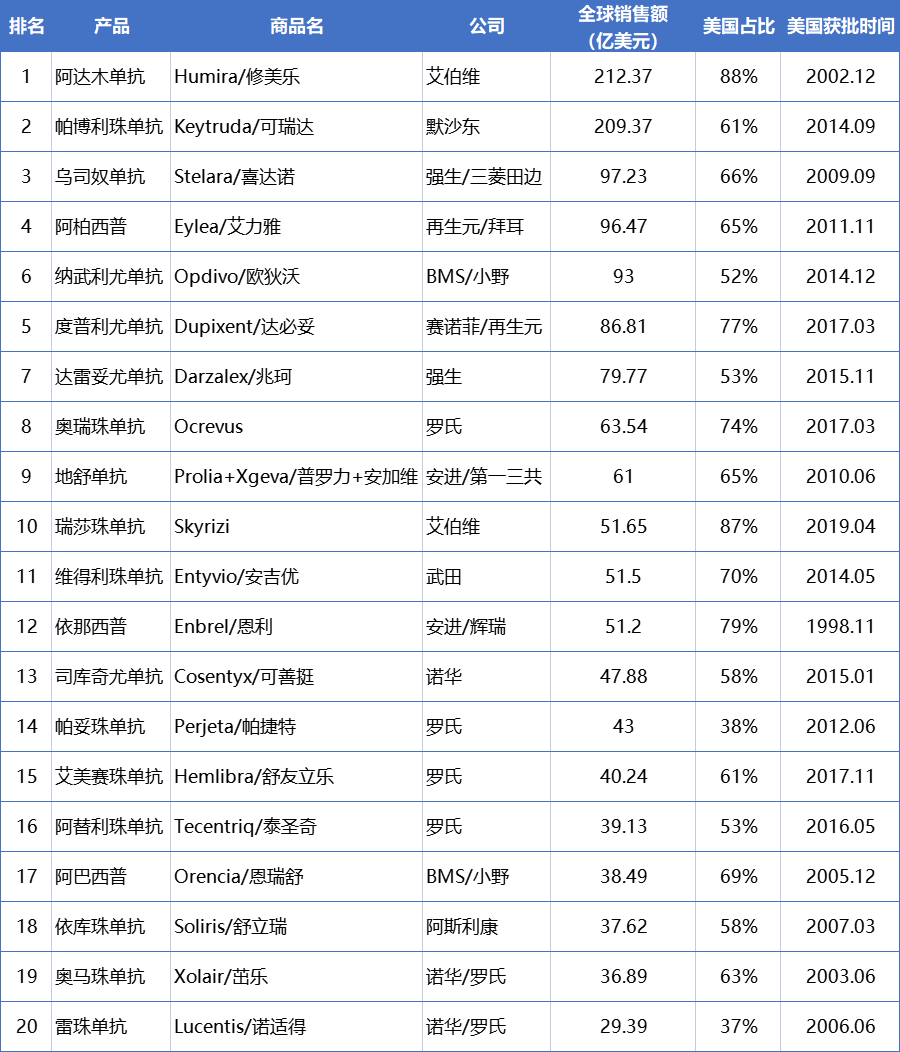
美国生物类似药市场2022概览
在政策方面,拜登政府在生物类似药领域降低药价、打击不正当竞争、专利诉讼和推动自动替换实施等方面的一系列举措极大的推动了生物类似药冲破重重阻碍的快速发展,极大的节省了政府在医药领域的巨额开支,政策层面的
2023-03-17
中小生物药企的出海之路,缘何从新发展?
新加坡凭借其独特的政策和市场选择机制,已成功吸引了越来越多的企业与人才驻足;政策、资金、产业、创新、人才在这里相互衔接,所形成的“新”式生物医药产业创新生态系统,也定将助力在“新”企业大放异彩。
2024-03-14
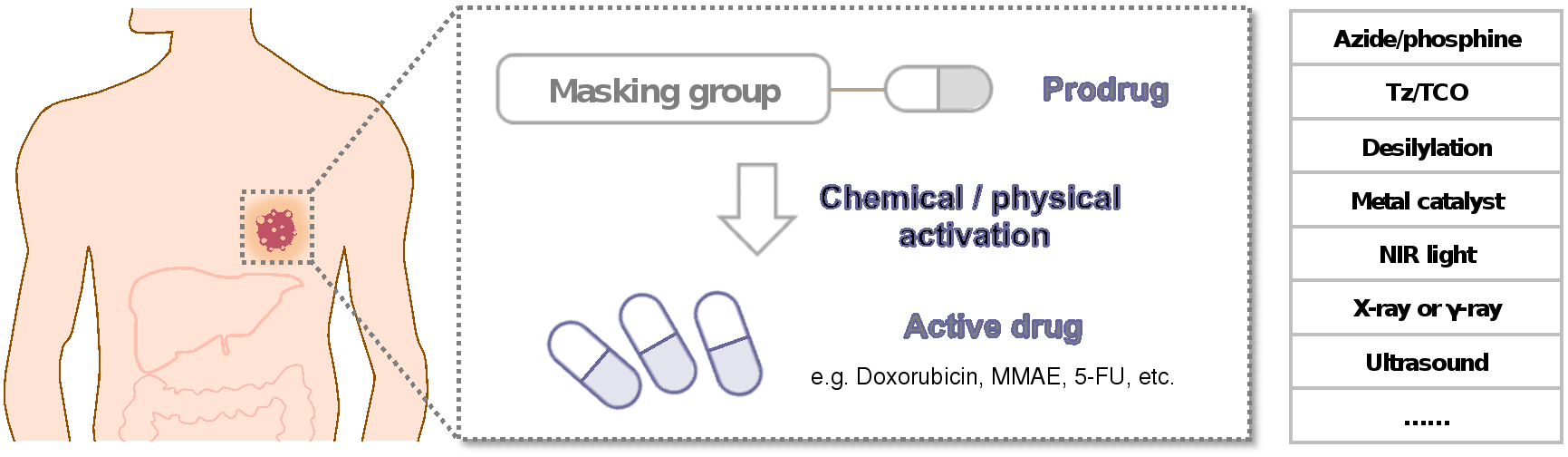
Chemical Society Reviews发表生物正交化学用于体内前药激活的综述
如何使用化学工具应对肿瘤治疗的难题,是生物正交反应领域研究的重要方向之一。传统的肿瘤治疗药物常常伴随严重的副作用,前药策略是解决上述问题的常用手段。
2023-12-25
研究阐述肠道微生物在抗抑郁药治疗中的作用
研究揭示了肠道微生物群在艾司西酞普兰治疗抑郁症患者的疗效机制中发挥了重要作用,有助于优化针对肠道微生物群和血液代谢组的抗抑郁治疗策略,为抗抑郁治疗提供了一个全新的视角。
2024-03-12
Microbiome:发文阐述肠道微生物在抗抑郁药治疗中的作用
该研究揭示了肠道微生物群在艾司西酞普兰治疗抑郁症患者的疗效机制中发挥了重要作用,有助于优化针对肠道微生物群和血液代谢组的抗抑郁治疗策略,为抗抑郁治疗提供了一个全新的视角。
2024-03-18
股价腰斩:硕迪生物发布口服GLP-1类减肥药中期临床数据
在安全性方面,GSBR-1290的几乎所有参与者都出现了治疗相关紧急不良事件,但大多数是中等严重程度。一名受试者因不良事件退出,一名参与者在研究期间被诊断为脂肪肝病,其肝酶升高,但胆红素未升高。
2023-12-20
士泽生物成功实施临床级iPS衍生细胞移植治疗帕金森病给药
士泽生物的治疗成本不及美国同类治疗成本的三十分之一,对追求个性化治疗帕金森病有实质需求的中国及全球帕金森病患者更加经济可及,具有明确的市场化竞争优势。
2024-02-11
减肥药最新进展:中国生物制药GMA106申请Ib/II期临床试验获受理
GMA106计划在中国通过Ib期试验研究进一步确认更高剂量在超重和肥胖人群中多次给药的安全性和耐受性。II期研究将在不同队列中探索不同剂量和给药频率治疗24周和36周后的初步疗效。
2023-10-17