神经变性疾病研究领域重要研究成果解读!
来源:本站原创 2021-07-30 17:47
本文中,小编整理了多篇重要研究成果,共同聚焦科学家们在人类神经退行性疾病研究领域取得的新成果,分享给大家!利用具有时空分辨率的邻近标记和定量蛋白质组学筛选STING转运辅助因子。图片来源:Nature, 2021, doi:10.1038/s41586-021-03762-2。【1】Nature:C型尼曼-匹克病竟与免疫蛋白STING有关,抑制STING或可
本文中,小编整理了多篇重要研究成果,共同聚焦科学家们在人类神经退行性疾病研究领域取得的新成果,分享给大家!

利用具有时空分辨率的邻近标记和定量蛋白质组学筛选STING转运辅助因子。
图片来源:Nature, 2021, doi:10.1038/s41586-021-03762-2。
【1】Nature:C型尼曼-匹克病竟与免疫蛋白STING有关,抑制STING或可治疗这种罕见的神经退行性疾病
doi:10.1038/s41586-021-03762-2
C型尼曼-匹克病(Niemann-Pick disease type C)是一种罕见的神经退行性疾病。这种疾病在一个多世纪前就被发现,但仍然缺乏有效的治疗。C型尼曼-皮克病在全世界的发病率大约为15万分之一,长期以来一直被认为是一种胆固醇代谢和分布的疾病。在一项新的研究中,来自美国德克萨斯大学西南医学中心的研究人员发现了一种与C型尼曼-匹克病有关的免疫蛋白。这一发现是在小鼠模型中发现的,可能为C型尼曼-匹克病提供一个强大的新治疗靶标。相关研究结果于2021年7月21日在线发表在Nature期刊上,论文标题为“Tonic prime-boost of STING signalling mediates Niemann–Pick disease type C”。
研究者Nan Yan博士表示,“C型尼曼-匹克病从未被认为是一种免疫性疾病。这些发现使它有了一个全新的视角。”当Npc1基因发生突变时,胆固醇不会被送到细胞中需要的地方,导致运动和智力能力逐渐下降,这是尼曼-皮克病的特点。Yan实验室并不研究胆固醇代谢,是在研究一种称为STING的免疫蛋白时偶然取得这一发现。STING是人体防御病毒的一个关键部分,通常依靠另一种称为环状GMP-AMP合酶(cGAS)的蛋白质来感知DNA并开启免疫基因以击退病毒入侵者。
【2】Nat Commun:一种预测神经退行性疾病的血液检测指标
doi:10.1038/s41467-021-23620-z
神经退行性疾病也称为神经系统变性病,神经轴索变性或损伤是其主要特征,会导致不可逆转的神经损伤。在既往的研究中,脑脊液中的淀粉样蛋白-β(Aβ42)、总tau(T-tau)蛋白和磷酸化tau(P-tau)蛋白等生物标志物可以用来协助诊断一些神经退行性疾病,比如阿尔茨海默症、帕金森病等。在神经退行性疾病患者中,机体为了应对神经轴索变性或损伤,脑脊液中神经纤维丝轻链(NfL)会被释放到细胞外,从而在脑脊液中可以检测到NfL的升高,这也是目前公认的神经退行性疾病的生物标志物,但是,获取脑脊液需要通过腰椎穿刺术等一些侵入性的检查手段进行,这对临床常规的评估工作造成困难。
近日,来自伦敦国王学院的研究团队通过测定伦敦国王学院和瑞典隆德斯坎恩大学医院招募的神经退行性疾病患者的血液发现,受试者血液中NfL的升高可以对阿尔茨海默症、帕金森病、运动神经元病等神经退行性疾病进行早期预测,并且初步总结出了年龄相关的NfL参考值,这些参考值在对65岁以上年龄段的神经退行性疾病检测准确率高达90%。这项研究近日发表在《Nature Communications》杂志上,题为A multicentre validation study of the diagnostic value of plasma neurofifilament light。
【3】Science子刊论文详解!开发出可穿过血脑屏障将药物递送到大脑的纳米颗粒,有望治疗一系列神经退行性疾病
doi:10.1126/sciadv.abd6889
在过去的几十年里,科学家们已经确定了导致神经退行性疾病的生物途径,并开发了针对这些途径的有前途的分子制剂。然而,将这些发现转化为临床批准的治疗方法的进展速度要慢得多,部分原因是人们在将治疗药物穿过血脑屏障(blood-brain barrier, BBB)并送入大脑方面所面临的挑战。为了促进治疗药物成功地递送到大脑,来自美国布莱根妇女医院和波士顿儿童医院的研究人员在一项新的研究中,构建出一种纳米颗粒平台,它在小鼠中可以促进将封装的药物有效地递送到物理上被破坏或完整的BBB中。在创伤性脑损伤(TBI)的小鼠模型中,他们观察到这种递送系统在大脑中的累积量是传统递送方法的三倍,而且治疗效果也很好,这可能为治疗众多神经系统疾病提供了可能性。相关研究结果发表在2021年1月1日的Science Advances期刊上,论文标题为“BBB pathophysiology–independent delivery of siRNAin traumatic brain injury”。
以前开发的将治疗药物递送到TBI发生后的大脑中的方法依赖于头部物理损伤后的短暂时间窗口,此时BBB暂时被破坏。然而,在被破坏的BBB在几周内受到修复后,医生缺乏有效的药物递送工具。研究者Nitin Joshi表示,无论大分子还是小分子治疗剂都很难穿过BBB。我们的解决方案是将治疗剂封装到具有精确工程化表面特性的生物相容性纳米颗粒中,使得它们在治疗上有效地递送到大脑中,与BBB的状态无关。
图片来源:Science, 2020, doi:10.1126/science.aay3302。
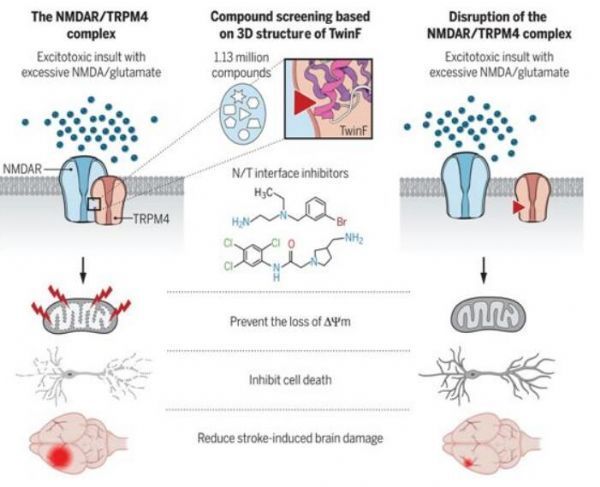
【4】Science:重大突破!一类新型抑制剂可高效阻止神经变性,有望治疗一系列神经退行性疾病
doi:10.1126/science.aay3302
在一项新的研究中,来自德国海德堡大学的研究人员发现了一种位于神经连接(即突触)处的通常会激活一种保护性遗传程序的特殊受体当位于突触外时如何导致神经细胞死亡。这种在神经退行性过程方面的重要发现使得他们对治疗药物产生了全新的认识。在对小鼠模型的实验中,他们发现了一类新的保护神经细胞的高效抑制剂。正如Hilmar Bading教授指出的那样,这类新型药物首次在对抗目前无法治疗的神经系统疾病方面开辟了前景。相关研究结果发表在Science期刊上,论文标题为“Coupling of NMDA receptors and TRPM4 guides discovery of unconventional neuroprotectants”。
Bading教授和他的团队着重关注是这种称为N-甲基-D-天门冬氨酸(NMDA)受体的受体。这种受体是一种可被生化信使分子---神经递质谷氨酸---激活的离子通道蛋白。它允许钙流入细胞。钙信号在突触中启动可塑性过程,但也会传送到细胞核中,在那里激活一种保护性遗传程序。位于神经细胞连接处的可被谷氨酸激活的NMDA受体在大脑中具有关键功能,有助于学习和记忆过程以及神经保护。但是,这种受体也存在于突触外。这些位于突触外的NMDA受体构成了威胁,这是因为它们的激活会导致细胞死亡。然而,正常情况下,高效的细胞谷氨酸摄取系统可以确保这种受体不被激活,从而确保神经细胞不受损伤。
doi:10.1073/pnas.2001563117
最近一项研究中,海德堡大学的研究人员研究了治疗神经退行性疾病的新方法。神经生物学家通过对小鼠模型的研究证明了保护神经细胞树突的损失可以减少中风后的脑损伤风险。Hilmar Bading教授与Daniela Mauceri教授领导的团队基于这一发现,正在开发治疗神经退行性疾病的新方法,相关研究结果发表在PNAS杂志上。
脑神经细胞拥有许多树突结构,可以与其他神经元建立联系。这些高度复杂的分支结构是其与其他神经细胞连接的重要先决条件,以使大脑能够正常运行。在早期的研究中,海德堡大学的研究人员发现信号分子VEGF-D是维持和恢复神经元结构的关键。基于这些发现,研究人员探究了是否可以通过恢复VEGF-D水平来预防中风后神经元树突结构的减少的问题。
【6】Nat Commun:新研究有助于治疗大脑感染以及神经退行性疾病
doi:10.1038/s41467-020-17491-z
超过3000万美国人被受污染的肉类所传播的脑部寄生虫感染,但大多数人永远不会表现出症状。来自弗吉尼亚大学医学院的一项新发现解释了其中的原因,这一发现可能对脑部感染,神经退行性疾病和自身免疫性疾病具有重要意义。
研究者表示,弓形虫会被大脑小胶质细胞控制。这些小胶质细胞释放出独特的免疫分子IL-1α,该分子从血液中募集免疫细胞来控制大脑中的寄生虫。这一新发现揭示了他们在需要时如何寻求帮助,这一发现可以应用于任何具有免疫学成分的脑部疾病,包括脑损伤,神经退行性疾病,中风,多发性硬化等。
文章中,研究人员利用小胶质细胞的长寿特性来了解它们在脑部感染中的作用。她和她的同事发现,感染导致小胶质细胞以炎性方式死亡,而密切相关的免疫细胞则不会。
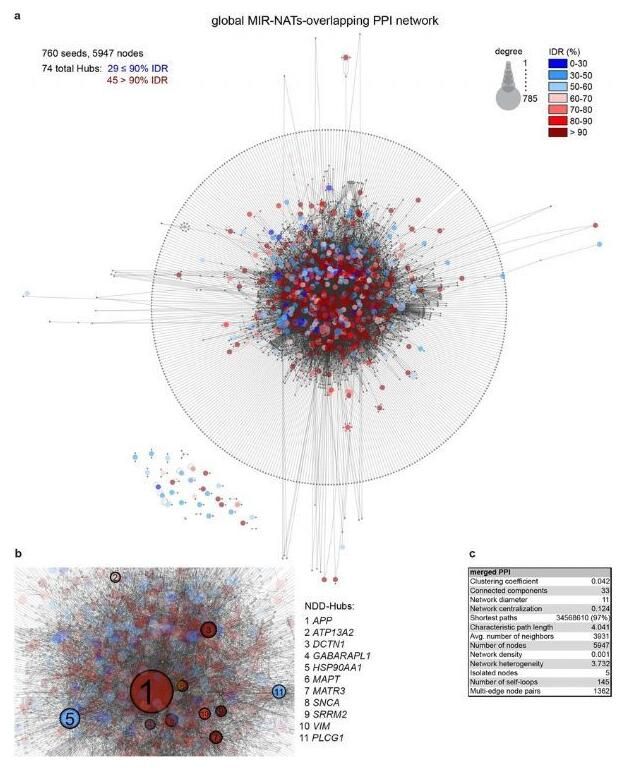
在神经退行性变中MIR-NATs抑制MAPT的转译和促进蛋白质稳态。
图片来源:Simone, R., et al. Nature (2021). doi:10.1038/s41586-021-03556-6
【7】Nature:揭秘神经变性疾病发生过程中tau蛋白产生的分子机制 或有望帮助开发相应的新型疗法
doi:10.1038/s41586-021-03556-6
人类基因组能表达数千种天然翻译转录物(NAT,natural antisense transcripts),从而调节其重叠基因的表观遗传状态、转录、RNA稳定性或翻译。日前,一篇刊登在国际杂志Nature上题为“MIR-NATs repress MAPT translation and aid proteostasis in neurodegeneration”的研究报告中,来自伦敦大学学院等机构的科学家们通过研究首次揭示了参与控制tau蛋白产生的一层遗传物质,tau蛋白是一种在诸如帕金森疾病和阿尔兹海默病等严重神经变性疾病发生过程中扮演关键角色的特殊蛋白。
文章中,研究人员通过对小鼠和细胞进行研究后揭示,这种遗传物质或许是一种较大的非编码基因家族的一部分,该基因家族控制并调节其它相类似的大脑蛋白,比如与阿尔兹海默病发生相关的β-淀粉样蛋白和参与帕金森疾病和路易体痴呆症的α-突触核蛋白等。相关研究结果或为研究人员阐明与神经性疾病相关的蛋白质产生和被控制的机制提供了新的认识,并有望帮助开发新型疗法来治疗一系列痴呆症相关的疾病。
研究者Roberto Simone博士说道,tau蛋白在脑细胞内部发挥着重要作用,其有助于稳定并维持细胞骨架结构,从而促进不同的物质被运输到机体所需的地方。我们都知道,过多的tau蛋白是有害的,过量且未使用的tau蛋白会转化成为有毒物质,从而负责损伤细胞并驱动退行性疾病的传播和扩展;然而,尽管tau蛋白已经被研究了超过30年了,但目前研究人员还并不清楚tau蛋白的产生是如何被控制的。
【8】Cell Rep:一种参与神经变性疾病的特殊蛋白或能阻断诱发细胞死亡的特殊信号
doi:10.1016/j.celrep.2021.108976
RIG-I样受体(RLRs)会通过识别双链RNA(dsRNA)参与到对自身和非自身的识别过程中去,目前有研究表明,免疫刺激性dsRNAs是普遍表达的,但其却会被细胞RNA结合蛋白(RBPs)所破坏或隔绝起来,TDP-43就是一种与多种神经性障碍相关的RBP,其对于细胞的活力至关重要。
近日,一篇发表在国际杂志Cell Reports上题为“TDP-43 prevents endogenous RNAs from triggering a lethal RIG-I-dependent interferon response”的研究报告中,来自范德堡大学等机构的科学家们通过研究发现,一种参与神经变性疾病(比如ALS,肌萎缩性侧索硬化症等)发生的特殊蛋白或能阻断引发细胞死亡的先天性免疫反应的激活。
这种被称之为TDP-43的特殊蛋白能够调节双链RNA的积累,双链RNA是一种存在于病原体和机体自身细胞中的遗传物质;相关研究结果揭示了先天性免疫反应和基因表达控制之间的复杂关联。研究者Karijolich表示,我们非常感兴趣阐明细胞是如何有效区分自我与非自我,以及被激活的信号通路是否能保护机体抵御病原体的侵入。每天我们都会接触到病毒和细菌,而机体自身还要确保并不会让这些病原体在机体中建立感染。
图片来源:CC0 Public Domain
【9】PLoS Biol:科学家发现在多种人类神经变性疾病发生过程中扮演关键角色的关键细胞压力酶类!
doi:10.1371/journal.pbio.3001096. eCollection
近日,一篇发表在国际杂志PLoS Biology上题为“MARK2 Phosphorylates eIF2α in Response to Proteotoxic Stress”的研究报告中,来自约翰霍普金斯大学布鲁姆博格公共健康学院等机构的科学家们通过研究发现,名为MARK2的酶类或能作为细胞中的一种关键压力反应开关,这类压力反应的过度激活是诱发神经变性疾病患者大脑细胞损伤的一种可能性原因,包括阿尔兹海默病、帕金森疾病和肌萎缩性侧索硬化症,这一研究发现或能帮助研究人员阐明MARK2酶在多种疾病发生过程中扮演的关键角色,同时其或有望成为研究人员开发治疗神经变性疾病新型疗法的潜在靶点。
除了与神经变性疾病相关的潜在相关性外,这一研究发现对于科学家们理解基础的细胞生物学机制也有着非常重要的意义。文章中,研究人员重点研究了应对蛋白质毒性压力(即细胞主要部分内受损或聚集的蛋白质的积累,这是神经变性疾病发生的核心特征)的细胞反应,众所周知,细胞能通过减少新蛋白质的产生来对这类压力产生反应,而一种特殊的信号酶类似乎会介导这种反应,在排除了其它信号酶类后,研究人员发现,信号酶MARK2或许就扮演着关键的角色。
【10】基于癸酸的膳食策略或有望治疗包括癌症、癫痫症和神经变性疾病在内的一系列人类疾病
新闻阅读:Research finds new dietary approach could manage a range of diseases
近日,来自皇家霍洛威大学的科学家们通过研究发现了一类名为癸酸(decanoic acid)的特殊脂肪酸或许与生酮饮食的健康效应密切相关,其或有望作为一种关键组分来帮助机体细胞抵御癌症、癫痫症和神经变性疾病的发生。
研究者Robin SB Williams表示,癸酸能够逆转包括癌症、癫痫症和神经变性疾病等多种疾病患者机体中的细胞改变,并能改善患者的疾病症状;生酮饮食,即一种高脂、低碳水化合物的特殊饮食模式,其被广泛认为是通过生成名为酮类的化学物质来发挥作用,并能降低机体的葡萄糖和胰岛素信号,进而保护机体抵御多种疾病下的细胞改变。
研究人员采用了一种创新性的方法来揭示了癸酸的作用机制,此前研究人员对一种名为盘基网柄菌(Dictyostelium)的单细胞生物进行研究时首次发现了癸酸,而在大约10亿年前盘基网柄菌与人类有着共同的祖先。随后研究者证实,癸酸在哺乳动物大脑、人类脑细胞及患有结节性硬化症患者中能以相同的方式发挥作用,结节性硬化症是一种机体的神经发育障碍。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。