白血病告别化疗!艾伯维Imbruvica+Venclexta固定疗程一线治疗CLL:完全缓解率56%!
来源:本站原创 2021-06-08 11:25
该方案是一种全口服、每日一次、无化疗、稳定疗程方案,2年生存率98%。
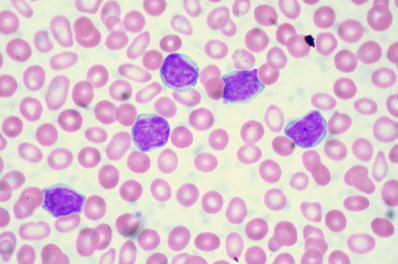
慢性淋巴细胞白血病(CLL,图片来源:dxline.info)
2021年06月08日讯 /生物谷BIOON/ --艾伯维(AbbVie)近日公布了2期CAPTIVATE(PCYC-1142)研究的新数据。该研究在年龄18-70岁、先前没有接受过治疗(naive,初治)的慢性淋巴细胞白血病(CLL)或小细胞淋巴瘤(SLL)患者中开展,正在评估Imbruvica(中文商品名:亿珂®,通用名:ibrutinib,伊布替尼)联合Venclexta(中文商品名:唯可来®,通用名:venetoclax,维奈克拉)作为一种全口服、每日一次、无化疗、稳定疗程(fixed-duration,FD)方案,用于一线治疗的疗效和安全性。
FD队列中,159例患者接受3个周期ibrutinib导入治疗,随后接受12个周期的ibrutinib+venetoclax(Ibr 420mg/天,Ven递增至400mg/天)方案治疗。在完成12个周期ibrutinib+venetoclax治疗后,经确认为无法检测到微小残留病(uMRD,即MRD阴性)的患者(定义为:外周血[PB]和骨髓[BM]uMRD连续超过3个周期),以1:1的比例随机分配,接受安慰剂或ibrutinib双盲治疗。不符合uMRD的患者,以1:1的比例随机分配至ibrutinib或ibrutinib+venetoclax开放标签治疗。uMRD(MRD阴性)意味着治疗后使用一种特殊且高度敏感的检测方法检测不到癌细胞,其定义为每10000个白细胞中癌细胞数量<1个。
结果显示,FD队列达到了主要终点:中位随访27.9个月,在无del(17p)、70岁或以下的患者中,完全缓解率(CR)为56%(95%CI:48-64),这一比率远高于研究假设的37%最低有意义比率(p<0.0001)。在整个研究人群中,CR为55%,并且在所有高危亚组中是一致的。此外,24个月无进展生存率(PFS)和总生存率(OS)分别为95%和98%。此外,77%的患者在外周血(PB)、60%的患者在骨髓(BM)中实现了无法检测到的微小残留病(uMRD,即MRD阴性)。
这一数据建立在先前在ASH2020年会上报道的MRD队列结果的基础上:超过三分之二的患者在ibrutinib+venetoclax治疗12个周期后实现不可检测的uMRD,30个月的PFS率为≥95%,与随后的随机治疗无关。
研究中,最常见的3/4级不良反应(AE)为中性粒细胞减少(33%)、高血压(6%)和中性粒细胞计数下降(5%)。不良事件导致4%的患者停药ibrutinib,2%的患者停药venetoclax。联合用药的安全性与每种药物已知的AE基本一致,未发现新的安全信号。
CAPTIVATE指导委员会成员及研究调查员Paolo Ghia博士表示:“我们对这些有希望的结果感到鼓舞,这表明ibrutinib+venetoclax有潜力作为CLL患者的一种重要的无化疗、稳定疗程治疗选择。”
ibrutinib(伊布替尼)是全球首款上市的BTK抑制剂,于2013年11月首次获批。该药由艾伯维旗下公司Pharmacyclics与强生旗下杨森制药联合开发和商业化,艾伯维拥有美国市场的权利,强生拥有美国以外市场的权利。BTK是B细胞生存所必需的一种激酶。通过阻断BTK,ibrutinib有助于迫使恶性B细胞离开其生长增殖的环境,如淋巴结,并阻止它们返回。ibrutinib的作用,联合阻断BTK的其他效应,降低了恶性B细胞的生存能力。
ibrutinib已在100多个国家获得批准,迄今为止已治疗全球23万多名患者。ibrutinib是唯一一个在3项CLL临床试验中显示总生存期(OS)获益的BTK抑制剂,缓解持久长达8年,70%的患者在5年后仍然存活且无疾病进展。此外,ibrutinib是唯一被证明能调节短期和长期免疫恢复的BTK抑制剂。
在中国,ibrutinib(亿珂®,伊布替尼)于2017年8月首次获批,作为一种单药疗法,用于治疗:(1)既往至少接受过一种治疗的慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)患者;(2)既往至少接受过一种治疗的套细胞淋巴瘤(MCL)患者。2018年11月,Imbruvica获批新适应症:(1)作为单药疗法,用于既往至少接受过一种治疗的华氏巨球蛋白血症(WM)患者,或者不适合接受化学免疫治疗的患者的一线治疗;(2)与利妥昔单抗联用,用于WM患者的治疗。
venetoclax(维奈克拉)是一种首创、口服、选择性B细胞淋巴瘤因子-2(BCL-2)抑制剂,由艾伯维与罗氏合作开发,双方共同负责美国市场的商业化(商品名:Venclexta),艾伯维则负责美国以外市场的商业化(商品名:Venclyxto)。BCL-2蛋白在细胞凋亡(程序性细胞死亡)中发挥重要作用,可阻止一些细胞(包括淋巴细胞)的凋亡,并且在某些类型癌症中过度表达,与耐药性的形成相关。venetoclax旨在选择性抑制BCL-2的功能,恢复细胞的通讯系统,让癌细胞自我毁灭,达到治疗肿瘤的目的。
venetoclax已在全球80多个国家获得批准,用于治疗慢性淋巴细胞白血病(CLL)、小细胞淋巴瘤(SLL)、急性髓性白血病(AML)。在美国,venetoclax已获FDA授予5个突破性药物资格(BTD),一个用于一线治疗CLL、2个用于复发或难治CLL、2个用于一线治疗急性髓性白血病(AML)。
在中国,venetoclax(唯可来®,维奈克拉)于2020年12月获批,与阿扎胞苷联合用于治疗因合并症不适合接受强诱导化疗,或者年龄75岁及以上的新诊断的成人急性髓系白血病(AML)患者。venetoclax(唯可来®,维奈克拉)是中国首个获批的B细胞淋巴瘤因子-2(BCL-2)抑制剂,标志着中国AML领域进入了靶向治疗时代。(生物谷Bioon.com)
原文出处:CAPTIVATE Study Shows an IMBRUVICA® (ibrutinib) Plus VENCLEXTA®/VENCLYXTO® (venetoclax) Chemotherapy-Free Combination Has Potential to Provide Remission After Fixed-Duration Treatment for Chronic Lymphocytic Leukemia (CLL)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->