Nat Commun:新型免疫疗法或有望彻底根治乙肝
来源:本站原创 2021-05-16 15:17
2021年5月16日 讯 /生物谷BIOON/ --确定T细胞的不同代谢需求以及其为何无法对抗病毒和肿瘤或有望提供新的治疗检查点,抑制酰基-CoA:胆固醇酰基转移酶(ACAT)或具有直接的抗癌活性。日前,一篇刊登在国际杂志Nature Communications上题为“Targeting human Acyl-CoA:cholesterol acyltra
2021年5月16日 讯 /生物谷BIOON/ --确定T细胞的不同代谢需求以及其为何无法对抗病毒和肿瘤或有望提供新的治疗检查点,抑制酰基-CoA:胆固醇酰基转移酶(ACAT)或具有直接的抗癌活性。日前,一篇刊登在国际杂志Nature Communications上题为“Targeting human Acyl-CoA:cholesterol acyltransferase as a dual viral and T cell metabolic checkpoint”的研究报告中,来自英国伦敦大学学院等机构的科学家们通过研究识别出了一种新型免疫疗法来抵御乙肝病毒(HBV),乙肝病毒是引发全球人群患肝癌最常见的原因。在全球范围内,每年慢性HBV都会导致大约88万人死于肝硬化或肝细胞癌。
图片来源:https://www.nature.com/articles/s41467-021-22967-7
在这项开创性研究中,研究人员利用直接分离自病人肝脏和肿瘤组织中的免疫细胞进行研究,结果表明,靶向作用ACAT酶或能有效增强机体的免疫反应,ACAT是一种能帮助管理细胞中胆固醇水平的特殊酶类。研究者指出,利用ACAT抑制剂阻断ACAT的活性或能增强特殊免疫细胞的功能,从而帮助抵御病毒及其相关癌变的肿瘤,这或许就阐明了ACAT抑制剂作为免疫疗法的有效性,抑制ACAT也能阻碍HBV自身的复制,从而就能发挥直接的抗病毒作用,诸如阿伐麦布(avasimibe) 等口服的ACAT抑制剂此前已经被证明作为人类的降胆固醇药物具有良好的耐受性。
研究者Mala Maini教授表示,慢性乙肝病毒感染是目前影响全球人群健康的一大重要问题,也是引发人群患肝癌的最常见原因。开发新型疗法对于改善患者的护理至关重要,诸如T细胞等免疫细胞对于抵御病毒和肿瘤是非常必要的,但其往往会因为功能严重失调而无法有效控制这些疾病,当前的标准治疗手段往往也不能消除病毒,亦不能预防癌症发展和挽救免疫细胞。
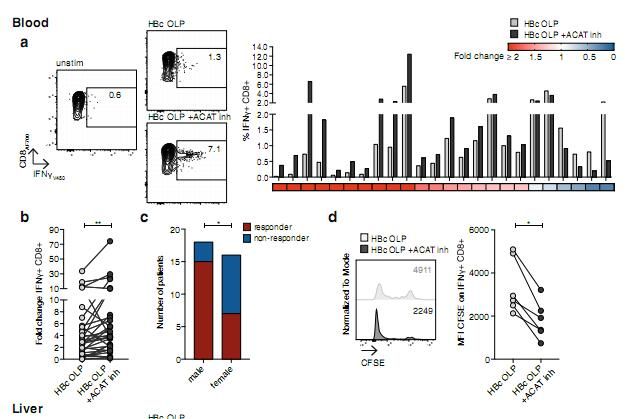
ATAT的抑制或能增强外周和肝脏内HBV特异性的CD8+ T细胞的活性。
图片来源:Schmidt, N.M., et al. Nat Commun 12, 2814 (2021). doi:10.1038/s41467-021-22967-7
这篇研究报告中,研究人员旨在识别出新型疗法靶点来直接抑制病毒的功能,并增强宿主机体抵御病毒感染的能力。胆固醇是机体每天就能从食物中获得的一种脂质,其能在机体的不同细胞中发挥多种功能,HBV能感染肝脏,而肝脏则是一种富含胆固醇的的器官,同时其还以限制机体局部免疫反应而闻名。通过在体外对来自人类肝脏疾病组织进行研究后,研究人员发现,ACAT抑制剂能增强人类抗病毒T细胞清除病毒的能力,这种反应与当前可用的治疗方法形成了鲜明的对比;免疫增强效应在HBV感染的肝脏和肝癌中所发现的T细胞中尤为显著,其能克服对免疫细胞功能的局部限制,从而促进T细胞靶向作用病毒和癌变细胞。
研究者指出,ACAT抑制剂能以一种异于其它抗病毒药物的作用方式来阻断HBV的生命周期,因此这些药物或具有独特的抗病毒和免疫疗法效应的特殊组合。研究者Nathalie Schmidt表示,如今我们已经找到了一种高效的新型靶点,其或有望未来帮助开发治疗慢性乙肝病毒感染和肝癌的新型疗法。利用ACAT抑制剂来调节胆固醇代谢或许具有直接靶向作用病毒和肿瘤的独特功能,同时还能增强T细胞的功能,这就能够使得研究人员同时从多个方向来解决这一疾病。
ATAT的抑制或能增强外周和肝脏内HBV特异性的CD8+ T细胞的活性。
图片来源:Schmidt, N.M., et al. Nat Commun 12, 2814 (2021). doi:10.1038/s41467-021-22967-7
如今科学家们已经知道调节胆固醇的药物在人类机体中使用是安全的,而且研究者希望本文研究或能指导当前将胆固醇调节和其它免疫疗法相结合的临床试验。综上,ATAT抑制剂或能提供一种代谢检查点的范例,从而来抑制病毒和肿瘤进展,但能挽救耗竭的T细胞,从而就能提供一种具有吸引力的治疗性靶点来帮助开发HBV及其相关肝细胞癌的新型疗法;总之,本文研究结果为发现或开发慢性病毒感染和癌症的新型疗法提供了新的可能性。(生物谷Bioon.com)
原始出处:
Schmidt, N.M., Wing, P.A.C., Diniz, M.O. et al. Targeting human Acyl-CoA:cholesterol acyltransferase as a dual viral and T cell metabolic checkpoint. Nat Commun 12, 2814 (2021). doi:10.1038/s41467-021-22967-7
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。




