基因魔剪!CRISPR/Cas9基因编辑造血干细胞疗法CTX001获欧盟优先药物资格(PRIME):治疗2种血红蛋白病!
来源:本站原创 2021-04-29 22:13
CTX001将造血干细胞进行改造,使红血球产生高水平的胎儿血红蛋白(HbF),单次输注可快速持久提高血红蛋白水平!

2021年04月29日讯 /生物谷BIOON/ --Vertex制药公司与合作伙伴基因编辑公司CRISPR Therapeutics近日联合宣布,欧洲药品管理局(EMA)已授予CTX001优先药物资格(PRIME),该药是一种自体、体外CRISPR/Cas9基因编辑疗法,用于治疗输血依赖性地中海贫血(TDT)。2020年9月,EMA还授予了CTX001治疗重度镰状细胞病(SCD)的PRIME。
值得一提的是,CTX001是治疗TDT和SCD方面临床推进最快的基因编辑方法,同时也是第一个在临床上已被证明概念正确的CRISPR/Cas9治疗方法。(CTX001临床疗效数据详见:Creating transformative gene-based medicines for serious diseases)
PRIME是EMA在2016年3月推出的一个快速审批项目,与美国FDA的突破性药物资格(BTD)项目相似,旨在加速医药短缺领域重点药品的审评进程,尽早使患者受益。入围PRIME的实验性药物,将在临床试验及药品开发方面获得EMA的大力支持,以加速真正创新药物的开发及审批,来满足对有前景新药的医疗需求。获得PRIME资格的药物,必须有初步临床证据和非临床证据表明该药与现有治疗药物相比能够实质性改善病情。
CTX001是一种在研的、自体、体外CRISPR/Cas9基因编辑疗法,目前正在评估用于治疗TDT和重度SCD。在这种疗法中,患者的造血干细胞被改造成在红血球中产生高水平的胎儿血红蛋白(HbF;血红蛋白F)。HbF是一种携带氧气的血红蛋白,在出生时自然存在,然后转换为成人形式的血红蛋白。CTX001升高HbF有潜力减轻TDT患者的输血需求、减少SCD患者痛苦且使人虚弱的镰状细胞危象。
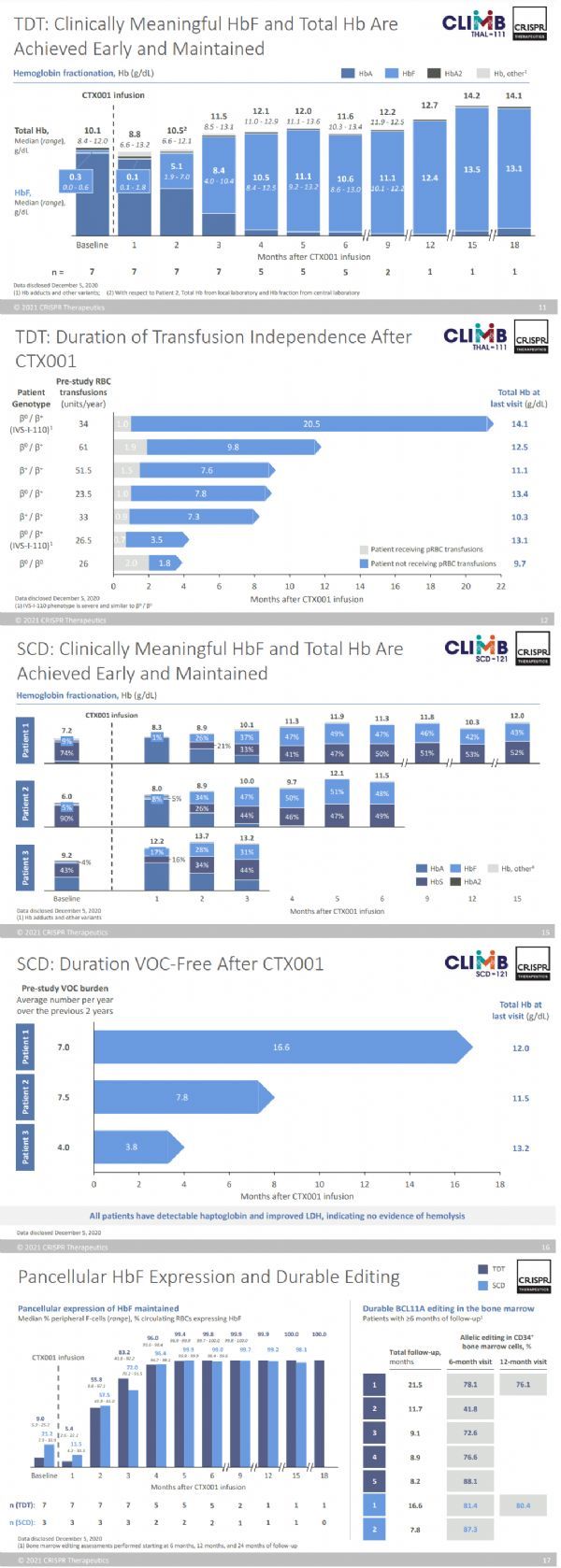
此次PRIME的授予是基于CRISPR和Vertex正在开展的一项评估CTX001治疗TDT患者的1/2期临床试验的数据。数据显示,接受单剂量输注CTX001的TDT患者,快速实现了强劲、持久、泛细胞HbF高水平表达,同时减轻了输血需求。在治疗重度SCD患者的1/2期临床试验中,接受单剂量输注CTX001的重度SCD患者,快速实现了强劲、持久、泛细胞HbF高水平表达,同时减少了痛苦和使人衰弱的镰状危象。
CRISPR-Cas9基因编辑(图片来源:CRISPR Therapeutics)
CTX001是根据CRISPR Therapeutics和Vertex之间的共同开发和共同商业化协议开发,用于治疗TDT和SCD。根据该项目迄今为止的进展,CTX001治疗TDT和SCD已获得美国FDA授予再生医学高级治疗产品(RMA)、快速通道资格(FTD)、孤儿药资格(ODD)、罕见儿科疾病资格(RPDD)。此外,CTX001也被欧盟EMA授予了治疗TDT和SCD的孤儿药资格(ODD)。
目前,CTX001正在2项正在进行的临床试验中进行研究,作为TDT患者和重度SCD患者的一种潜在一次性疗法。这些试验中,已有30多例患者接受了CTX001治疗,最长的随访时间已超过2年。2项试验预计在今年将完成患者入组。
CLIMB-111(CLIMB-Thal-111)和CLIMB-121(CLIMB-SCD-121)均为正在进行的1/2期开放标签试验,旨在分别评估单剂量CTX001在12-35岁TDT患者、12-35岁重度SCD患者中的安全性和有效性。每项试验将招募多达45例患者,在CTX001输注后,将对患者进行大约2年的随访。每例患者都将被要求参与一项长期随访试验(CLIMB-131),这项试验旨在CTX001输注后对患者进行长达15年的随访。
CTX001治疗TDT和SCD临床数据(点击图片,查看大图)
CRISPR Therapeutics与Vertex于2015年达成了一项战略研究合作,重点是利用CRISPR/Cas9发现和开发针对人类疾病内在遗传原因的潜在新疗法。CTX001是联合研究计划中出现的第一种治疗方法。CRISPR Therapeutics和Vertex将共同开发和商业化CTX001,并平等分担全球所有研发成本和利润。
2021年4月20日,Vertex与CRISPR Therapeutics宣布,双方已修订了上述合作协议。根据修订后的协议,Vertex将领导CTX001的全球开发、制造和商业化;双方在研发成本和利润的分配比例,将由之前的5:5修订为Vertex占60%、CRISPR占40%。此外,CRISPR将收到9亿美元的预付款,在CTX001获得监管部门批准后,还将收到2亿美元的里程碑付款。
Vertex将部署其在制造、开发、监管和商业化方面的广泛全球能力和成熟经验,以最大限度地发挥CTX001改变美国、欧洲和其他国家成千上万患者生活的潜力。(生物谷Bioon.com)
原文出处:Vertex and CRISPR Therapeutics Announce Priority Medicines (PRIME) Designation Granted by the European Medicines Agency to CTX001? for Transfusion-Dependent Beta Thalassemia
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->