PD-L1阳性三阴性乳腺癌(TNBC)免疫治疗!美国FDA咨询委员会:支持维持罗氏Tecentriq+化疗加速批准!
来源:本站原创 2021-04-29 17:48
Tecentriq(泰圣奇)+化疗(Abraxane)方案已在多个国家获批治疗PD-L1阳性转移性TNBC,但在验证性试验中未能达到主要终点。

2021年04月29日讯 /生物谷BIOON/ --罗氏(Roche)近日宣布,美国食品和药物管理局(FDA)肿瘤药物咨询委员会(ODAC)以7票赞同、2票反对的投票结果,支持维持抗PD-L1疗法Tecentriq(泰圣奇,通用名:atezolizumab,阿替利珠单抗)治疗PD-L1阳性三阴性乳腺癌(TNBC)的一项加速批准,具体为:Tecentriq联合化疗(Abraxane,白蛋白结合型紫杉醇[nab-紫杉醇]),用于治疗经FDA批准的检测方法证实为肿瘤表达PD-L1、不可切除性、局部晚期或转移性TNBC患者。
此次ODAC会议,是FDA针对肿瘤学药物加速批准进行全行业审查的一部分,所涉及的肿瘤药物在验证性试验中未能达到主要终点且尚未获得常规批准。咨询委员会向FDA提供来自外部医学专家的独立意见和建议,尽管这些建议没有法定约束力。目前,FDA还没有宣布何时对Tecentriq的这一适应症做出最终决定。
罗氏首席医疗官兼全球产品开发主管Levi Garraway医学博士表示:“三阴性乳腺癌患者几乎没有治疗选择,这就是为什么今天咨询委员会做出认可Tecentriq联合疗法重要性决定的重大意义。我们感谢FDA和ODAC的公开对话,并期待继续合作,改善乳腺癌患者的生活。”
1992年,FDA设立“加速批准项目(Accelerated approval Program)”,该项目允许有条件地批准一种药物上市,以解决严重疾病领域的显著未满足医疗需求,并有特定的上市后要求(PMR),来确认药物的临床益处并转换为常规批准。作为新药研发与审评的一种加速通道,该项目的推出,在很大程度上加快了一些新药上市的步伐。
Tecentriq于2019年3月获得美国FDA加速批准,用于治疗PD-L1阳性、不可切除性、局部晚期或转移性TNBC成人患者。该批准基于Passion130研究的阳性无进展生存期(PFS)结果。是否继续批准该适应症取决于IMpassion131研究的结果,该研究是这项mTNBC适应症的上市后要求(PMR)。
然而,结果显示,在初始(一线)治疗PD-L1阳性mTNBC患者方面,IMpassion131研究没有达到改善PFS的主要终点。由于在Passion130研究中显示的具有临床意义的益处仍然存在,罗氏期待着继续与FDA合作,以确定该适应症中关于Tecentriq的下一步措施。
罗氏仍然致力于跟踪科学,以更好地了解癌症,包括哪些患者可能受益于免疫治疗。Tecentriq已经证明了它在高医疗需求领域的变革性作用,是同类药物中第一个被批准治疗某些特别难以治疗的癌症类型。
Tecentriq的广泛开发项目包括多个正在进行和已计划的3期研究,涵盖肺癌、泌尿生殖道癌、皮肤癌、乳腺癌、胃肠道癌、妇科癌和头颈癌等多个癌种。这包括单独或与其他药物联合使用评价Tecentriq的研究,以及在转移性、辅助治疗、新辅助治疗的研究。
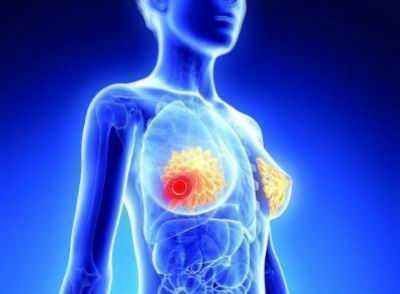
乳腺癌是女性最常见的癌症类型,全球每年确诊超过200万例。TNBC约占15%,与其他类型相比,TNBC在50岁以下女性中更常见。TNBC特指雌激素受体(ER)、孕激素受体(PR)及人表皮生长因子受体2(HER-2)三者均为阴性表达的乳腺癌,进展迅速,预后极差,5年生存率不到15%。TNBC对激素疗法和HER2靶向疗法(如赫赛汀)均无效,治疗选择非常有限,主要依靠化疗。转移性TNBC是最具侵袭性、最难治疗的乳腺癌之一,与其他亚型乳腺癌相比,转移性TNBC进展迅速,生存期更短。
过去30多年来,罗氏一直在推进乳腺癌研究,目标是帮助尽可能多的乳腺癌患者。该公司靶向药物Herceptin、Perjeta、Phesgo、Kadcyla、Tecentriq正在继续改变早期和晚期HER2阳性乳腺癌和TNBC的治疗格局。通过临床开发项目,罗氏希望为乳腺癌患者带来新的治疗组合,最终改善预后。
Tecentriq属于PD-(L)1肿瘤免疫疗法,靶向结合肿瘤细胞和肿瘤浸润免疫细胞上表达的PD-L1蛋白,阻断其与PD-1和B7.1受体的相互作用。通过抑制PD-L1,Tecentriq可以激活T细胞。
截至目前,Tecentriq已获多个国家批准作为单药疗法及联合靶向疗法和/或化疗,治疗多种类型癌症,包括:非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)、某些类型的转移性尿路上皮癌(mUC)、PD-L1阳性三阴性乳腺癌(TNBC)、肝细胞癌(HCC)、黑色素瘤等。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


