Nat Med:缩短抗原结合结构域的接头可提高CD22 CAR-T细胞的疗效
来源:本站原创 2021-04-30 10:27
2021年4月30日讯/生物谷BIOON/---尽管靶向CD19的嵌合抗原受体(CAR)T细胞(CAR-T)能够在B细胞急性淋巴细胞白血病(B-ALL)患者中诱导病情缓解,但是较大的一部分患者会因CD19丢失发生疾病复发。与CD19一样,CD22在B系细胞中广泛表达,因此可作为B-ALL免疫治疗的替代靶点。在一项新的研究中,来自美国宾夕法尼亚大学佩雷尔曼医学
2021年4月30日讯/生物谷BIOON/---尽管靶向CD19的嵌合抗原受体(CAR)T细胞(CAR-T)能够在B细胞急性淋巴细胞白血病(B-ALL)患者中诱导病情缓解,但是较大的一部分患者会因CD19丢失发生疾病复发。与CD19一样,CD22在B系细胞中广泛表达,因此可作为B-ALL免疫治疗的替代靶点。
在一项新的研究中,来自美国宾夕法尼亚大学佩雷尔曼医学院的研究人员发现很多B-ALL患者在接受靶向CD22的CAR-T细胞治疗后没有反应,于是试图探究其中的原因。他们发现,当涉及到将CAR的抗原结合结构域中可变重链区和可变轻链区连接在一起的接头(linker)的长度时,少即是多(less is more),其中抗原结合结构域使得CAR-T细胞能够结合肿瘤细胞并攻击它们。相关研究结果于2021年4月22日在线发表在Nature Medicine期刊上,论文标题为“Antigen-independent activation enhances the efficacy of 4-1BB-costimulated CD22 CAR T cells”。

这些作者指出,几个氨基酸的微小差异就能给患者带来巨大的变化;在他们从接头上移除15个氨基酸后,将CAR的抗原结合结构域中的可变重链区和可变轻链区连接在一起,并预先激活CAR-T细胞。
宾夕法尼亚大学佩雷尔曼医学院与诺华公司合作开发的抗CD19 CAR-T细胞(Kymriah)目前已被美国食品药品管理局(FDA)批准用于治疗患上复发/难治性B-ALL的儿童和年轻成人;然而,长期随访显示,相当一部分获得缓解的患者最终会复发,通常是当白血病细胞失去CD19抗原的表达并逃避新的免疫系统时复发。这些作者已经为这组患者开发了第二种方法:靶向CD22抗原的CAR-T细胞(下称CAR-22 T细胞),CD22也是在B细胞表面上发现的。
宾夕法尼亚大学和费城儿童医院用CAR-22 T细胞疗法对6名儿童和3名成年难治/复发性B-ALL患者进行的两项临床试验(NCT02588456和NCT02650414)研究显示,总体上临床反应不佳。令人震惊的是,这些发现与美国国家癌症研究所(NCI)的一项类似试验的积极结果不一致。因此,这些作者开展进一步调查,发现这两种治疗方法之间的唯一区别是单链可变片段的长度。美国国家癌症研究所临床试验中的CAR的单链可变片段的接头是5个氨基酸的长度,而宾夕法尼亚大学/费城儿童医院临床试验中的接头是20个氨基酸的长度。
宾夕法尼亚大学的研究小组与诺华公司合作,随后构建出一种新的基于41BB的具有较短接头长度的CAR-22 T细胞,并在小鼠和人类细胞研究中将它与之前的CAR进行比较。相比于CD28,41BB是一种不同的共刺激信号,是CAR-T细胞激活和生存所需要的。这些作者发现,事实上,CAR构建体上的较短接头更成功地预激活了CAR-T细胞,使其对B细胞的反应和随后的抗肿瘤活性得到改善。科学家们通常认为,当T细胞在看到它们的靶标之前被预先激活时,它们会变得很容易遭受功能衰竭。
这些作者认为这一发现真正颠覆了当前的教条。如今大多数CAR具有两个内置强化系统之一:CD28或41BB。事实证实这个假设仅对CD28刺激的CAR是正确的,而对更常用的41BB刺激的CAR则不是。他们在这项新的研究中证实情形刚好相反。最令人兴奋的是,这些数据揭示了一条以前隐藏的路径,它以一种有条不紊的方式改善CAR-T细胞的功能。
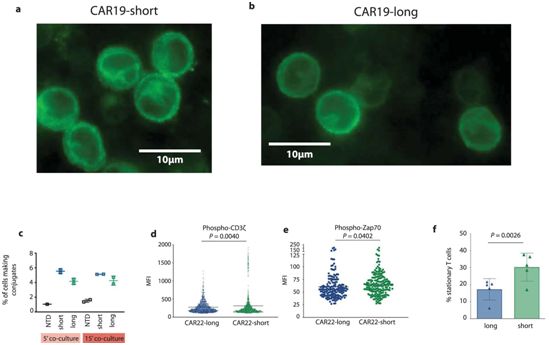
图片来自Nature Medicine, 2021, doi:10.1038/s41591-021-01326-5。
这些研究结果导致宾夕法尼亚大学、费城儿童医院与诺华公司合作,对患有难治/复发性B-ALL的成人和儿童患者进行一项新的、正在进行的临床试验,旨在研究具有较短接头长度的CAR。其他研究正在进行中,以确定接头的长度在其他CAR-T细胞中是否重要。
综上所述,这些作者发现,缩短连接CAR抗原结合结构域中可变重链和可变轻链的氨基酸接头,推动了受体同源二聚体化和抗原非依赖性信号转导。与基于CD28的CAR相比,基于4-1BB的自主信号转导的CAR表现出增强的免疫突触形成、促炎症基因激活和卓越的效应功能。他们在几种CAR构建体中证实了自主信号转导和增强功能之间的这种联系,并在这些观察的基础上,设计了一种新的短接头CD22单链可变区片段用于临床评估。他们的研究结果表明,基于4-1BB的抗原非依赖性信号转导(tonic signaling)有利于CAR的功能,并展示在CAR-T细胞疗法的设计和实施中,从病床边到实验室再到病床边的转化是有实用性的。(生物谷 Bioon.com)
参考资料:
Nathan Singh et al. Antigen-independent activation enhances the efficacy of 4-1BB-costimulated CD22 CAR T cells. Nature Medicine, 2021, doi:10.1038/s41591-021-01326-5.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


