多发性骨髓瘤新药!赛诺菲CD38靶向抗体Sarclisa第二种组合疗法获欧盟批准!
来源:本站原创 2021-04-20 10:05
Sarclisa是强生重磅CD38抗体Darzalex的第一个直接竞争对手,后者上市第5年,销售额达到42亿美元!

2021年04月20日讯 /生物谷BIOON/ --赛诺菲(Sanofi)近日宣布,欧盟委员会(EC)已批准CD38靶向抗体药物Sarclisa(isatuximab),联合卡非佐米(carfilzomib,Kyprolis®)和地塞米松方案(Kd),用于治疗既往已接受过至少一种疗法的复发性多发性骨髓瘤(MM)成人患者。在美国监管方面,Sarclisa+Kd方案于2021年3月获得了FDA批准。
值得一提的是,此次是Sarclisa在欧盟获批治疗复发性MM的第2个适应症,也是在不到一年时间里欧盟第2次批准Sarclisa联合标准治疗方案治疗复发性或难治性MM。2020年6月,Sarclisa在欧盟首次获批,联合泊马度胺和地塞米松方案(pom-dex),用于治疗既往已接受过至少2种疗法(包括来那度胺和蛋白酶体抑制剂)并在最后一种治疗中被证实疾病进展的复发性和难治性MM成人患者。
此次最新批准,基于III期IKEMA临床试验的结果。数据显示,在既往接受过1-3种疗法病情复发的MM患者中,与卡非佐米+地塞米松方案(Kd)相比,Sarclisa+卡非佐米+地塞米松(S-Kd)方案治疗将无进展生存期(PFS)在统计学上显著延长、将疾病进展或死亡风险显著降低47%、并显示出临床意义的深度缓解(微小残留病[MRD]阴性率:29.6% vs 13%)。
法国南特大学医院血液科Philippe Moreau医学博士表示:“由于多发性骨髓瘤没有治愈的方法,而且患者经常出现疾病复发,我们必须坚持寻求额外的治疗方案。近30%接受Sarclisa方案治疗的患者实现了深度缓解。这种新的治疗方案有潜力成为复发性多发性骨髓瘤患者的标准治疗方案,使患者在疾病进展的早期有了另一种治疗选择。”
赛诺菲肿瘤和儿科创新全球开发负责人Peter Adamson表示:“欧盟批准Sarclisa与卡非佐米和地塞米松(Kd)方案联合治疗,意味着欧洲的多发性骨髓瘤患者现在可以接受Sarclisa与2种标准治疗方案联合治疗结合。卡非佐米和地塞米松联合用药方案(Kd)代表着一个重要的标准护理。3期IKEMA试验的结果表明,在该方案中加入Sarclisa可将疾病进展或死亡风险降低近一半,这一发现为此次重要的欧盟批准奠定了基础。”
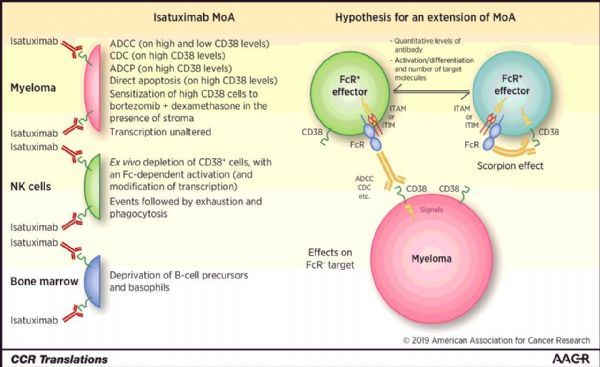
isatuximab作用机制(图片来源:aacrjournals.org)
IKEMA(NCT03275285)是一项随机、多中心、开放标签III期临床试验,在16个国家的69个临床中心入组了302例复发和/或难治性多发性骨髓瘤(MM)患者,这些患者先前接受过1-3种抗骨髓瘤疗法。试验期间,Sarclisa通过静脉输注,剂量为10mg/kg,每周一次持续四周,之后每隔一周输注一次,卡非佐米剂量为20/56mg/m2每周两次,治疗期间使用标准剂量的地塞米松。IKEMA试验的主要终点是无进展生存期(PFS)。次要终点包括总缓解率(ORR)、很好的部分反应或更好反应(≥VGPR)、微小残留病(MRD)、完全缓解率(CR)、总生存期(OS)和安全性。
结果显示,该研究达到了主要终点:与Kd组(n=123)相比,S-Kd组(n=179)疾病进展或死亡风险降低47%(HR=0.531,99%CI:0.318-0.889,p=0.0007)、PFS显著延长(中位PFS:未达到 vs 19.15个月)。与Kd相比,S-Kd方案在多个亚组中均显示出一致的治疗效果。
次要终点方面:S-Kd组与Kd组在ORR方面没有统计学显著差异(86.6% vs 82.9%;p=0.1930)。S-Kd组完全缓解率(CR)为39.7%、Kd组为27.6%。S-Kd组VGPR为72.6%、Kd组为56.1%。S-Kd组MRD阴性完全缓解率为29.6%、Kd组为13%,表明S-Kd组有近30%的患者采用下一代测序在1/100000敏感度下检测不到多发性骨髓瘤细胞。在中期分析时,总生存期(OS)数据尚不成熟。
该研究中,Sarclisa的安全性和耐受性与在其他临床试验中观察到的Sarclisa的安全性特征一致,没有观察到新的安全信号。
多发性骨髓瘤(MM)是第二常见的血液癌症,全世界每年新诊断病例超过13万例。在欧洲,每年确诊约3.9万例;在美国,每年确诊约3.2万例。尽管有可用的治疗方法,MM仍然是一种无法治愈的恶性肿瘤,与患者的严重负担相关。由于MM无法治愈,大多数患者最终都会复发,对目前可用的疗法不再有治疗应答。复发性MM是指癌症在治疗或缓解期后复发。难治性MM是指癌症对治疗没有反应或不再有反应。
Sarclisa的活性药物成分isatuximab是一种IgG1嵌合单克隆抗体,靶向浆细胞CD38受体的特定表位,能够触发多种独特的作用机制,包括促进程序性肿瘤细胞死亡(凋亡)和免疫调节活性。CD38在多发性骨髓瘤(MM)细胞上呈高水平表达,是MM和其他恶性肿瘤中抗体治疗的细胞表面受体靶标。在美国和欧盟,isatuximab均被授予了治疗复发或难治性多发性骨髓瘤(R/R MM)的孤儿药资格。目前,赛诺菲也正在评估isatuximab治疗其他血液系统恶性肿瘤和实体瘤的潜力。
2020年3月,Sarclisa获得美国FDA批准,联合泊马度胺和地塞米松(pom-dex),用于既往已接受过至少2种疗法(包括来那度胺和蛋白酶体抑制剂)的RRMM成人患者。2020年6月初,Sarclisa联合pom-dex方案也获得了欧盟委员会(EC)的批准。
Sarclisa是强生重磅CD38靶向药物Darzalex的第一个直接竞争对手,后者于2015年上市,适应症涵盖1-4线用药,已成为临床基石疗法,2020年全球销售额达到41.9亿美元,较上一年增幅达39.8%。华尔街投资银行Jefferies分析师预计,Sarclisa上市后的年销售峰值将突破10亿美元。
当前,赛诺菲正在推进多项III期临床研究,评估isatuximab联合目前可用的标准疗法,用于治疗RRMM患者或新诊断的MM患者。MM是第二种最常见的血液系统恶性肿瘤,在全球范围内,每年患病人数超过138万。对于大多数患者而言,MM仍然无法治愈,因此该领域存在着显著的未满足医疗需求。(生物谷Bioon.com)
原文出处:European Commission approves second indication of Sarclisa® (isatuximab) for relapsed multiple myeloma
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->