PNAS:肿瘤内部STING信号影响其对免疫治疗的耐受性
来源:本站原创 2021-04-15 22:36
肿瘤抗原性的缺乏或丧失是其具备免疫逃逸能力以及对T细胞免疫疗法产生抗性的关键。有证据表明,肿瘤细胞中干扰素基因(STING)信号刺激物的激活可以通过触发I型IFN介导的自分泌和旁分泌增强其抗原性。尽管已经发现在黑色素瘤和其他肿瘤类型中抑制该途径具有治疗益处,但是其内在机制仍不清楚。对此,来自Moffitt 癌症中心的James J. Mulé团队试图研究ST
2021年4月15日讯/生物谷BIOON/---肿瘤抗原性的缺乏或丧失是其具备免疫逃逸能力以及对T细胞免疫疗法产生抗性的关键。有证据表明,肿瘤细胞中干扰素基因(STING)信号刺激物的激活可以通过触发I型IFN介导的自分泌和旁分泌增强其抗原性。尽管已经发现在黑色素瘤和其他肿瘤类型中抑制该途径具有治疗益处,但是其内在机制仍不清楚。对此,来自Moffitt 癌症中心的James J. Mulé团队试图研究STING的抑制作用是否部分受到表观遗传调控,以及其是否影响了黑色素瘤对T细胞免疫疗法的抗药性。相关结果发表在最近的《PNAS》杂志上。
(图片来源:www.pixabay.com)
以前研究发现,在大量的人类黑素瘤细胞系中,STING和cGAS蛋白的表达存在不同程度的下调(STING为约50%,cGAS为约35%)。为了确定DNA甲基化在黑色素瘤STING和cGAS沉默中的作用,作者使用Illumina MethylationEPIC BeadChip微阵列平台对16个人类黑色素瘤细胞系进行了全基因组DNA甲基化分析,并且评估了STING的18个CpG探针中的甲基化变化情况。同时,作者对每个细胞系进行了免疫印迹分析,并进行了定量化的处理,确定了每种探针中的β值与STING蛋白表达之间的相关程度。研究证实:STING的超甲基化与蛋白质表达量之间呈负相关(Pearson r = -0.51)。此外,这些CpG探针的β值热图根据其STING蛋白表达识别出三个不同的亚类。在缺乏STING的细胞系WM266-4,WM239A,WM2032和888-MEL中,出现了高度甲基化,WM1361A的两个CpG探针(cg16983159和cg08321103)中也发现了高度甲基化(β值> 0.7)。上述结果表明,STING的丧失可能是由遗传和/或表观遗传改变(例如组蛋白修饰或涉及微小RNA的因素)介导发生的。

(图1,黑色素瘤中STING表观遗传学修饰与其表达量呈负相关趋势)
为了评估DNA去甲基化是否可以恢复STING表达和功能,作者接下来用6种STING缺失的黑色素细胞系(STING启动子甲基化过高):WM1361A,WM2032,WM239A,WM266-4、888-MEL和SBCL-2进行研究。并且加入DNA甲基转移酶(DNMT)抑制剂5-氮杂2'-脱氧胞苷(5AZADC)对细胞进行处理。 免疫印迹分析结果显示, 5AZADC处理后所有细胞系中STING表达发生上调,尽管程度不同。 此外,细胞接受吹之后 DNMT1,DNMT3A和DNMT3B明显减少。 同样,使用 siRNA对DNMT1和DNMT3B进行抑制也得到了相似的结果。
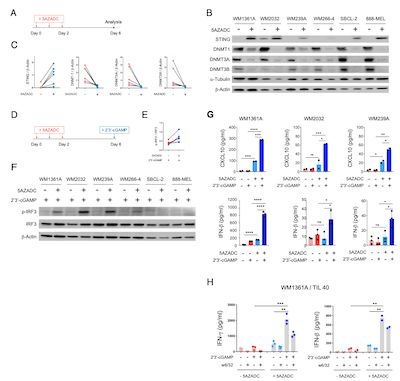
(图2,DNA去甲基化处理恢复STING的表达水平以及信号活性)
进一步研究证明,在STING缺陷型黑素瘤细胞系中,去甲基化介导的STING信号转导的恢复可以通过上调HLA的表达来改善其抗原性MHC I类分子的表达与功能,从而增强了它们对细胞毒性T细胞的识别和杀伤力。这些发现不仅阐明了表观遗传过程的作用,特别是阐明了DNA甲基化在黑色素瘤固有STING信号转导障碍中的作用,而且还突出了它们在肿瘤免疫逃逸和对T细胞的免疫疗法的产生耐受性中的功能。(生物谷 Bioon.com)
原始出处:Rana Falahat, Anders Berglund, Ryan M. Putney et al., Epigenetic reprogramming of tumor cell–intrinsic STING function sculpts antigenicity and T cell recognition of melanoma. Proceedings of the National Academy of Sciences Apr 2021, 118 (15) e2013598118; DOI: 10.1073/pnas.2013598118
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


