2021年3月Cell期刊不得不看的亮点研究
来源:本站原创 2021-03-31 23:47
2021年3月31日讯/生物谷BIOON/---2021年3月份即将结束了,3月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Cell:新研究表明新冠病毒变种B.1.351和P.1逃避中和抗体doi:10.1016/j.cell.2021.03.036检测和疫苗接种是人类试图控制SARS-CoV-2冠状病毒大流行的支柱。虽然耗
2021年3月31日讯/生物谷BIOON/---2021年3月份即将结束了,3月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:新研究表明新冠病毒变种B.1.351和P.1逃避中和抗体
doi:10.1016/j.cell.2021.03.036
检测和疫苗接种是人类试图控制SARS-CoV-2冠状病毒大流行的支柱。虽然耗时比很多人预想的要长,但相信大家接种疫苗从而得到保护只是时间问题。然而,时间也在对这种病毒起作用,该病毒现已发生多次变异,其中来自英国的B.1.1.7变种、来自南非的B.1.351变种和来自巴西的P.1变种迅速传播。这些病毒变种在所谓的刺突蛋白上发生了突变,其中刺突蛋白是这种病毒表面上的一种结构,负责附着在宿主细胞上。与此同时,刺突蛋白也是免疫反应的主要靶标。在SARS-CoV-2感染或接种疫苗时产生的抗体会与刺突蛋白结合,从而阻断这种病毒。
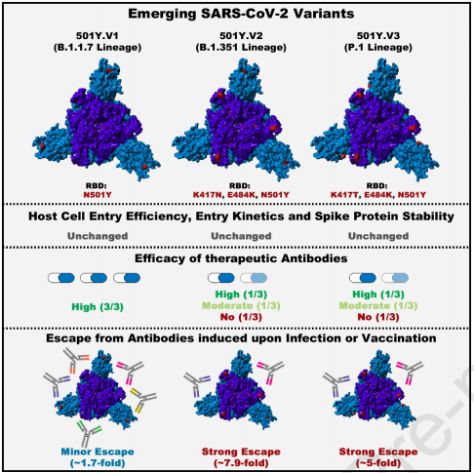
图片来自Cell, 2021, doi:10.1016/j.cell.2021.03.036。
2.Cell:人类和猩猩大脑 “无缝切换”,只需改变一个分子开关
doi:10.1016/j.cell.2021.02.050
作为一个物种,人类最独特的特征之一就是大脑的扩大。与小鼠相比,人脑的神经元总数增加了1,000倍,是所有灵长类动物中最多的,比我们的近亲黑猩猩和大猩猩高出三倍多。自从人类脱离了其他大猿之后,人类的大脑就经历了快速的扩张,但是这种人类特有的扩张机制仍然未知。而且尽管我们已经了解了许多有关控制灵长类动物与啮齿类动物进化差异的机制的知识,但与其他猿类相比,人类特异性的变化却鲜为人知。
基于此,来自英国剑桥大学医学研究理事会分子生物学实验室的Madeline A Lancaster 教授带领团队,通过使用衍生自人类、大猩猩和黑猩猩细胞的大脑类器官来研究驱动进化性大脑扩张的发育机制。发现神经上皮分化是猿类中的一个长期持续的过程,涉及以细胞形状改变为特征的先前无法识别的过渡状态。并通过比较RNA测序(RNA-seq)揭示了细胞形态发生因子,包含一种已知的上皮-间质转化调节剂(ZEB2),在表达动力学上的差异。相关研究成果以“An early cell shape transition drives evolutionary expansion of the human forebrain ”为题,于近期在线发表在《Cell》 杂志上。
3.Cell:工程化免疫细胞能够靶向抑制癌细胞转移
doi:10.1016/j.cell.2021.02.048
在最近一项研究中,科学家通过对免疫细胞进行遗传改造,从而使其能够精确地传递抗癌信号到可能扩散癌症的器官。在小鼠模型中,研究者们发现用工程化的细胞治疗可以有效缩小肿瘤,并防止癌症扩散到身体的其他部位。该研究由美国国立卫生研究院(NIH)旗下的美国国家癌症研究所(NCI)的科学家领导,并于2021年3月24日发表在《Cell》杂志上。
图片来源:Www.pixabay.com。
4.Cell解读!科学家有望利用人类机体的肠道微生物组来开发治疗神经系统疾病的新型靶向性疗法!
doi:10.1016/j.cell.2021.02.009
当我们想到诱发神经系统疾病的原因以及如何治疗时,我们通常会想到针对大脑来进行研究;但这到底是不是最佳的方法或者唯一的方向呢?日前,一篇发表在国际杂志Cell上题为“Dissecting the contribution of host genetics and the microbiome in complex behaviors”的研究报告中,来自美国贝勒医学院等机构的科学家们通过研究发现,肠道中的微生物或许会诱发与复杂神经系统疾病相关的某些疾病症状,因此基于微生物的疗法未来或有望帮助治疗人类的神经系统疾病。
研究者Mauro Costa-Mattioli说道,机体不同的异常行为或许是由宿主的基因和其机体的微生物组进行相互依存调节的,具体而言,在神经发育障碍小鼠模型中,其多动行为是由宿主机体的遗传特性所空的,而社会行为缺陷则是由肠道微生物组所介导的。更重要的是,从治疗学的角度来讲,利用促进肠道中生物喋呤家族中特定化合物产生的特定微生物进行治疗,或者利用一种代谢活性的生物喋呤分子进行治疗,就能够改善机体的社会行为,但并不能改善机体的运动活性。
5.Cell:新研究揭示胚胎组织经历了相变
doi:10.1016/j.cell.2021.02.017
当奥地利科学技术研究所的研究人员观察发育中的斑马鱼胚胎时,他们观察到了一个突如其来的巨大变化:在短短几分钟内,固体状的胚胎组织变成了液体状。是什么原因会导致这种变化,它在胚胎的进一步发育过程中起什么作用?在一项新的多学科研究中,他们找到了答案,这可能会改变我们对发育和疾病中关键过程(比如肿瘤转移)的看法。相关研究结果于2021年3月16日在线发表在Cell期刊上,论文标题为“Rigidity percolation uncovers a structural basis for embryonic tissue phase transitions”。
要想更多地了解一束微小的细胞是如何发育成复杂的系统,如鱼、人类或像大象一样大的动物,许多科学家转向斑马鱼(Danio rerio)。它有几个优点,使它成为像Nicoletta Petridou这样的发育生物学家最喜欢的模型生物之一。首先,这种小型的有条纹的鱼在短短几天内就发育完毕,胚胎在母体外进行发育,而且是透明的---可以看到它发育时的每一种器官。在观察受精后几小时的斑马鱼胚胎时,Petridou和她的同事们在之前的一项研究中已发现,胚胎组织的粘度突然发生了变化---这是衡量一种组织抗变形能力的标准。Petridou解释说,“在这个早期阶段,形成胚胎的组织是非常僵硬的,但突然间,粘度下降了十倍,这种组织流动得非常快--它液体化了。”
6.Cell:科学家有望开发出治疗过敏症和自身免疫性疾病的新型疗法!
doi:10.1016/j.cell.2021.02.027
近日,一项刊登在国际杂志Cell上的研究报告中,来自澳洲国立大学等机构的科学家们通过研究发现,免疫系统中的一种特殊功能或有望帮助治疗诸如哮喘症等过敏性疾病,并能帮助阻断危及生命的过敏反应。文章中,研究者揭示了一种能帮助预防机体患自身免疫性疾病和过敏症的天然方法,这一过程是由机体中一种名为神经突蛋白(neuritin)的特殊蛋白质所驱动的。
研究者Carola Vinuesa教授说道,如今我们在人类机体中发现了一种非常有趣的机制,其能帮助阻断诱发自身免疫性疾病或过敏症的“流氓”抗体的产生。长期以来我们一直知道,神经突蛋白在大脑和机体神经系统中扮演着关键角色,但如今我们在免疫系统发现了丰富的神经突蛋白及其作用机制,而这在此前生物学研究中并未描述过。
7.Cell:单基因突变为何会让某些人群更易患分枝杆菌病?
doi:10.1016/j.cell.2020.10.046
近日,一篇发表在国际杂志Cell上题为“Human T-bet Governs Innate and Innate-like Adaptive IFN-γ Immunity against Mycobacteria”的研究报告中,来自洛克菲勒大学等机构的科学家们通过研究揭示了患者机体的罕见突变如何帮助解释关于分枝杆菌的奥秘。仅仅因为我们暴露于病原体或许并不意味着我们会患病;有意思的是,研究人员已经发现,在决定引起一系列疾病的病原体是否最终会导致严重疾病的过程中,遗传因素扮演着关键角色,比如流感、疣和COVID-19。
研究者Jean-Laurent Casanova等人花费了25年时间来研究人类基因和分枝杆菌病(mycobacterial disease)之间相互作用的分子机制,以及继续深入分析遗传缺陷并将严重感染性疾病患者与暴露于分枝杆菌后仍然无疾病症状的患者区分开来,这项研究中,研究人员报道了对一位来自摩洛哥患有严重分支杆菌病的患者的研究结果。
8.Cell:多种新冠病毒变体竟可抵抗辉瑞和Moderna新冠疫苗诱导的中和抗体
doi:10.1016/j.cell.2021.03.013
造成COVID-19的SARS-CoV-2冠状病毒在整个大流行期间发生了突变。这种病毒的新变种在世界各地出现,包括可能具有更强的传播能力或逃避免疫系统的变种。美国加利福尼亚州、丹麦、英国、南非和巴西/日本都发现了此类变种。了解COVID-19疫苗对这些变种的作用如何,对于阻止全球COVID-19流行病的努力至关重要,这也是来自美国拉根研究所和麻省总医院的一项新研究的课题。

图片来自Cell, 2021, doi:10.1016/j.cell.2021.03.013。
9.Cell:环境污染物危害身体的八种方式
doi:10.1016/j.cell.2021.01.043
一篇针对现有证据的新综述论文提出了环境暴露的八种特征,这些特征描绘了污染物导致疾病的生物途径:氧化应激和炎症、基因组改变和突变、表观遗传改变、线粒体功能障碍、内分泌紊乱、细胞间通信改变、微生物组群落改变和神经系统功能受损。这篇综述论文近期发表在Cell期刊上,论文标题为“Hallmarks of environmental insults”。
论文高级作者、美国哥伦比亚大学梅尔曼公共卫生学院环境健康科学主席Andrea Baccarelli博士说,“每天我们都会更多了解关于暴露于空气、水、土壤和食物中的污染物如何危害人类健康。然而,不太了解的是这些化学物对我们身体造成损害的具体生物途径。在这篇综述论文中,我们提供了一个框架来理解为什么复杂的环境暴露混合物即使在相对适度的浓度下也会带来严重的疾病。”
10.Cell:新研究揭示动脉粥样硬化加速克隆性造血产生
doi:10.1016/j.cell.2021.01.049
在一项新的研究中,来自美国麻省总医院(MGH)和哈佛医学院的研究人员如今提出了一种不同的、额外的可能性:动脉粥样硬化导致克隆性造血。动脉粥样硬化患者遭受高脂血症和炎症,这两种症状会长期增强造血干细胞分裂率。他们证实这种增加的分裂会加速克隆性造血的产生。相关研究结果于2021年2月25日在线发表在Cell期刊上,论文标题为“Increased stem cell proliferation in atherosclerosis accelerates clonal hematopoiesis”。
论文通讯作者、MGH系统生物学中心首席研究员Kamila Naxerova博士说,“动脉粥样硬化患者基本上经历了‘时间加速’。这是因为基因改变出现并在造血系统中传播的速度是由干细胞分裂的基本速度决定的。从遗传学的角度来看,你可以说动脉粥样硬化加速了血液的老化。鉴于克隆性造血是一种与年龄相关的疾病,因此动脉粥样硬化患者比健康人容易更早发病。”(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


