聚焦ASH 2020:ROR1 ADC赛道有何看点?
来源:生物谷 2020-12-08 08:50
12月5日至8日,第62届美国血液学会(ASH)年会将以线上形式举行,一年一届的ASH年会是全球血液学工作者的盛会,每届年会都会公布和发表全球最新血液学进展。两款靶向受体酪氨酸激酶样孤儿受体1( ROR1)药物在本届ASH年会上公布了最新数据,这其中包括ROR1单抗(Cirmtuzumab)和ROR1 ADC(VLS101),数据显示两款药物都具有可控的安全
12月5日至8日,第62届美国血液学会(ASH)年会将以线上形式举行,一年一届的ASH年会是全球血液学工作者的盛会,每届年会都会公布和发表全球最新血液学进展。两款靶向受体酪氨酸激酶样孤儿受体1( ROR1)药物在本届ASH年会上公布了最新数据,这其中包括ROR1单抗(Cirmtuzumab)和ROR1 ADC(VLS101),数据显示两款药物都具有可控的安全性和积极的抗肿瘤活性。
来源:ASH官网
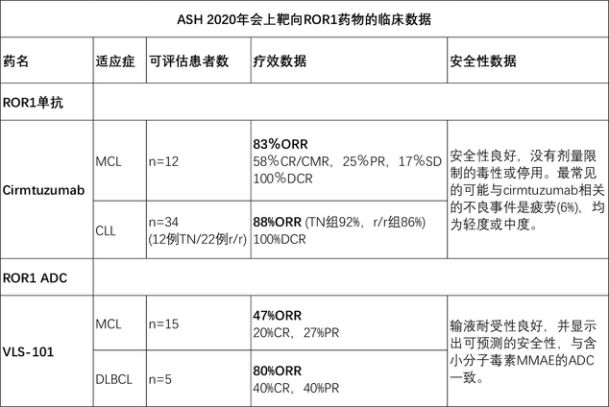
(如上图)ROR1单抗Cirmtuzumab与Ibrutinib(伊布替尼)联合用于复发/难治性(r/r)套细胞淋巴瘤(MCL)或初治(TN)或r / r慢性淋巴细胞性白血病(CLL)的患者,这种联合策略在正在进行的1/2期临床研究中获得积极数据。
此次公布的结果显示,MCL患者的总体缓解率(ORR)为83% (n=10/12),包括7名(58%)完全缓解(CR)、3名部分缓解(PR)和2名疾病稳定(SD),这意味着疾病控制率(DCR)为100%。中位随访8.3个月,中位无进展生存期(PFS)为17.5个月。CLL患者的ORR为88% (n=30/34),其中初次治疗(TN)组为92%, r/r组为86%,1名CR。4名SD,也意味着DCR为100%。中位随访12.8个月,所有患者无进展,82%仍在研究中。安全性良好,没有剂量限制的毒性或停用。
ASH 2020上,VelosBio公司公布的ROR1 ADC药物VLS-101的1期临床试验数据显示:在MCL的患者中(n=15),VLS-101的ORR(包括3例CR)达到47%(7/15);在弥漫性大B细胞淋巴瘤(DLBCL)患者中,ORR达到80%(4/5)。这些患者均经过大量的既往疗法治疗失败或治疗后复发,VLS-101输液耐受性良好,并显示出可预测的安全性,这表明了靶向ROR1药物有望满足更多患者的治疗需求。
基石药业与默沙东先后两大交易,ROR1到底有什么魔力?
就在ASH官网披露摘要当天,Cirmtuzumab所有者Oncternal Therapeutics的股价随即上涨了78%。而VLS101所有者VelosBio则凭借亮眼数据,在更早之前成功吸引到了默沙东的青睐,默沙东在11月5日宣布将以27.5亿美元买下VelosBio公司,彻底点燃了ROR1 ADC的市场行情。
这里不得不说,国内基石药业可谓是“慧眼识英雄”,在10月29日,早于默沙东布局,以1000万美元的首付款拿下了LegoChem Biosciences(简称LCB)旗下ROR1 ADC(LCB71)在韩国以外的全球地区的独家开发和商业化授权,可以说是最好的时间点。
ASH上的亮眼数据以及近期资本市场上的两大交易,让我们注意到ROR1。先是基石药业,后是默沙东,ROR1到底有什么魔力?
据了解,ROR1即受体酪氨酸激酶样孤儿受体1(receptor tyrosine kinase-like orphan receptor 1),在肿瘤特异性表达并在肿瘤增殖、转移和耐药等方面发挥重要作用,使其成为一个潜在的有吸引力的癌症治疗靶点。ROR1是一类癌胚细胞表面蛋白,参与了非经典的Wnt5a信号通路。在早期胚胎发育阶段表达,对神经、骨骼和血管器官生成起着重要作用,在胎儿发育过程中,ROR1的表达减少,正常成人组织中除了罕见的B淋巴细胞前体细胞外,缺乏ROR1的表面表达。
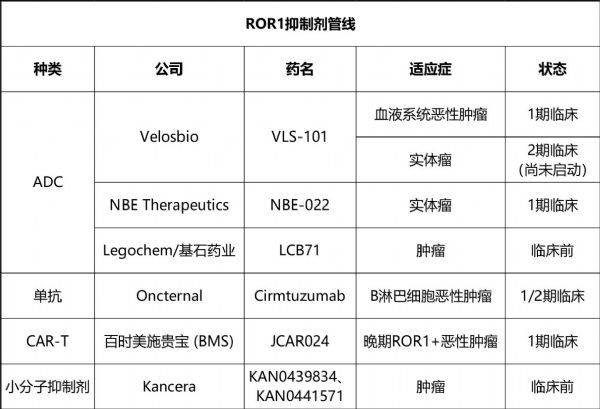
随着对ROR1分子结构、组织表达、信号通路及作用机制的深入研究,靶向ROR1的多种形式药物正在开发中,包括抗体药物偶联物(ADC)、单克隆抗体、嵌合抗原受体(CAR)T细胞疗法和小分子抑制剂。
来源:EvaluatePharma & clinicaltrials.gov.
国内基石药业领跑,全球ROR1 ADC仅两款进入临床
纵观全球,只有为数不多的公司正在开发以ROR1为靶点的ADC,仅两款进入临床阶段。包括VelosBio公司(已被默沙东收购)的VLS-101,目前正处于2期临床试验,以及NBE-Therapeutics公司的NBE-002,目前正处于1/2期临床试验。基石药业引进的LCB71目前处于临床前阶段,是进展近乎全球第三的ROR1 ADC。
相关进展:
· 如上所述,在早期临床试验中,VLS-101单药治疗血癌表现出可控的安全性和抗肿瘤活性的早期迹象。这项1期临床试验的患者已接受其他抗癌药物的大量预处理,并且他们的癌症在最初对这些其他抗癌药物产生反应后仍未反应或复发。不久前,ROR1 ADC药物VLS-101的2期临床研究首例患者完成给药。该公司计划在今年晚些时候开始评估它作为实体瘤的潜在治疗方法。
· 另一款进入临床的ROR1 ADC药物NBE-002已经于今年10月开始了首次人体研究,该项目用于三阴性乳腺癌(TNBC)和其他实体肿瘤。
· 韩国LCB公司专注于利用其专有的药物发现技术LegoChemistry,以及其ADC平台技术ConjuAllTM来开发下一代新疗法,LCB公司一直致力于研究开发基于专有平台技术的ADC、抗生素、抗凝血剂和抗癌疗法等。作为ADC平台技术开发商,LCB公司迄今已签署了9项技术许可协议,总价值超过9亿美元,这也证明了该公司在全球市场中的技术竞争力。随着ADC赛道异常火爆,该公司仅在今年就达成了四笔交易,最新交易是在12月2日,其与Pyxis Oncology签署了价值3亿美元的DLK-1 ADC候选技术许可协议。
基于专有的ADC平台,LCB公司开发的ROR1 ADC(LCB71)具有特殊设计,携带有肿瘤激活的吡咯并苯二氮卓(PBD)前药毒素,可有效地解决与传统PBD载荷有关的典型毒性问题,有更大的安全窗口。目前处于临床前阶段的LCB71已在几种临床前癌症模型中证明具有完全的肿瘤抑制作用,并展示出良好的血清半衰期及药代动力学特性,这些都将会转化为多种实体和血液恶性肿瘤的广泛治疗指标。此外,LCB71利用定向偶联技术获得精准的药物抗体比率(DAR),便于实现均质及大规模生产。
另外,值得一提的是,国内尚未见有其他公司管线正在参与ROR1 ADC药物的开发。基石药业引进的这款LCB71有可能成为潜在同类最优(best-in-class)的候选药物,用于针对一系列癌症适应症的单药治疗或联合疗法。
据相关资料显示,该公司已经开发了多种候选药物,靶点包括当前肿瘤免疫领域的三个骨架产品,即PD-1、PD-L1和CTLA-4抗体药物。目前的肿瘤免疫治疗领域仍然存在着一些挑战,例如缺乏针对无T细胞免疫或者“冷”肿瘤的治疗手段、不友善的肿瘤免疫微环境是免疫检查点抑制剂治疗的主要耐药机制。LCB71是基石药业研发管线里的第一款ADC,不但可以加强基石药业不断扩大的肿瘤免疫治疗管线,还可以与公司现有的管线互为补充,用于潜在的联合治疗策略,以更好地应对该领域的挑战。
小结
ADC来源于将化疗药物和抗体药结合在一起的设想,其由单抗、细胞毒性药物以及将两者连接起来的连接头(linker)组成,由于抗体具有靶向性(可识别癌细胞表面抗原),因此可将细胞毒性分子选择性地直接“运送”到肿瘤细胞中,在发挥抗癌作用的同时,又避免对健康细胞产生影响。当前,在国内形成了以荣昌生物、百奥泰为首的ADC竞争格局,但仔细研究后发现,靶点赛道拥挤,大多集中在CD22、CD30、CD33、HER2、Trop2等。各大公司通过自主研发或者license-in,获得差异化的竞争优势将是突破当前瓶颈的重要方向。这其中包括开发新靶点,或对已有靶点开发差异化的临床适应症;基于先进的技术平台,研发出同靶点、同适应症中具最佳有效性或安全性的药物。
在新靶点ADC的研发中,尽管ROR1 ADC的临床数据有限,但是就目前来看,安全性和有效性都值得期待,并且相对于CD22、HER2等已经拥挤的赛道具有不错的投资潜力。ROR1 ADC在短短时间内达成了两项交易,就是此类创新ADC药物在市场上炙手可热的缩影。
新药研发就是大浪淘沙的过程,聪明的公司可以在早期发现优质项目,加快新药上市所需的一系列步骤。我们期待着有关ROR1 ADC的最新两项交易以及更多药企的努力可以充分发挥ADC药物的潜力,并将其带给世界各地的患者。与此同时,我们相信多种形式靶向ROR1的药物将突破现有瓶颈,推动下一代肿瘤免疫治疗领域的发展。(生物谷 Bioon.com)
参考出处:
1. 张瑶.ROR1靶向疗法的研究进展[J].中药与临床,2020,11(04):63-66.
2. Balakrishnan A, Goodpaster T, Randolph-Habecker J, et al. Analysis of ROR1 Protein Expression in Human Cancer and Normal Tissues. Clin Cancer Res. 2017;23(12):3061-3071. doi:10.1158/1078-0432.CCR-16-2083
3. http://www.koreatimes.co.kr/www/tech/2020/10/694_298439.html
4. https://pipelinereview.com/index.php/2020020673738/DNA-RNA-and-Cells/Oncternal-Therapeutics-Announces-Presentation-of-ROR1-CAR-T-Preclinical-Data-at-2020-ASCO-SITC-Clinical-Immuno-Oncology-Symposium.html
5.https://seekingalpha.com/news/3632323-new-data-on-lead-drug-propels-oncternal-therapeutics-up-78
6. https://ash.confex.com/ash/2020/webprogram/Paper136373.html
7.https://ash.confex.com/ash/2020/webprogram/Paper141917.html?source=content_type%3Areact%7Cfirst_level_url%3Anews%7Csection%3Amain_content%7Cbutton%3Abody_link
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->