中性粒细胞的“安全网”或能促进癌细胞转移并不断增殖
来源:本站原创 2020-06-23 15:14
2020年6月23日 讯 /生物谷BIOON/ --中性粒细胞是一种特殊的免疫细胞,其能为机体抵御感染提供第一道免疫防线,然而,在很多情况下,其都有能力促进癌症发生转移,即让癌细胞从原发性位点迁移并在机体其它部位生长,日前一项刊登在国际杂志Nature上的研究报告中,研究者Yang等人就揭示了中性粒细胞促进这一致命过程的分子机制。图片来源:Emma Nola
2020年6月23日 讯 /生物谷BIOON/ --中性粒细胞是一种特殊的免疫细胞,其能为机体抵御感染提供第一道免疫防线,然而,在很多情况下,其都有能力促进癌症发生转移,即让癌细胞从原发性位点迁移并在机体其它部位生长,日前一项刊登在国际杂志Nature上的研究报告中,研究者Yang等人就揭示了中性粒细胞促进这一致命过程的分子机制。
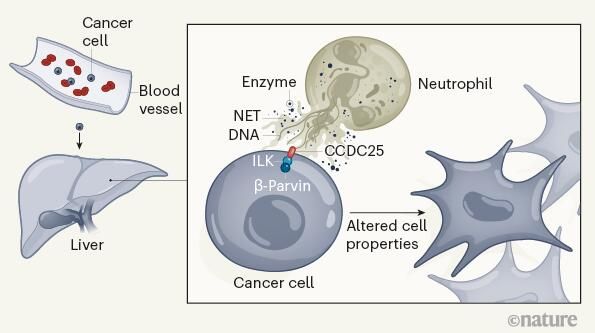
图片来源:Emma Nolan et al. Nature (2020) doi:10.1038/d41586-020-01672-3
中性粒细胞的一个关键特征就是能将一种名为中性粒细胞胞外陷阱(NET,neutrophil extracellular trap)的特殊结构挤压到周围环境中,其优覆盖对微生物有毒的特殊酶类的DNA网所组成,其能够捕获并杀灭入侵的微生物,在肺部中,NETs能被炎症所诱导,而其抗肿瘤活性也与NET相关的酶类有关,如今越来越多的研究证据表明,NETs能介导癌细胞侵袭特性的发生及进展,然而研究人员并不清楚NETs如何增强癌症的转移,此外,此前也并没有研究报道促进癌细胞感知NETs的分子机制,研究者Yang等人就通过研究深入揭示了这些NETs促进肿瘤形成的分子机制。
首先研究人员评估了544名乳腺癌患者的原发性和转移性肿瘤中NETs的状况,NETs在原发性肿瘤位点很少见,但在肝脏(乳腺癌扩散常见的位点)中水平却很高,研究者发现,早期乳腺癌患者血液中高水平的NET DNA与癌症随后扩散到肝脏中直接相关,这就表明,监测血液样本中的NET DNA或能作为评估癌症患者疾病预后的一种新方法。为了在体内研究NETs与癌细胞之间的关联,研究人员将人或小鼠来源的乳腺癌细胞转移到小鼠体内并分析转移的肿瘤细胞,结果发现,NETs会在所检测小鼠模型的肝脏中积累,这一研究发现与研究者对癌症患者机体肿瘤分析的结果一致。
研究者Yang等人通过对小鼠模型进行研究后发现,在转移性癌细胞被检测到之前NETs就会在肝脏中被诱导产生,而癌细胞转移到肝脏中的效率取决于NETs,因为小鼠体内的癌症转移会在去除NETs后被大大损伤,无论是通过DNA降解酶DNase I或通过对小鼠遗传工程化修饰使其缺少NET形成所需的关键酶类。此前研究中,研究者表示,NET依赖性的肝脏转移是通过NETs对癌细胞物理捕获的间接机制所引发的,Yang等人发现,在体外测试中,NET DNA能直接刺激人类乳腺癌细胞的迁移和吸附。
随后研究人员想通过研究阐明这种迁移行为被诱导的分子机制,通过在NET DNA上添加标记并以其为诱饵来捕获并识别与其相互作用的特殊蛋白,研究人员发现了一种能与NET DNA相结合的名为CCDC25的受体,其存在于癌细胞表面,能与较高的特异性和亲和力与NET DNA结合,从而促进癌细胞对NET的感知,此外,研究者还识别出了能与NET DNA结合的CCDC25的特殊胞外部分。研究者证实,NET接到的爱细胞迁移的刺激是通过CCDC25所驱动的,这就表明,在体外通过剔除人类乳腺癌细胞或患者原发性乳腺肿瘤细胞样本中的CCDC25就能明显降低癌细胞的迁移(体外测试);相比CCDC25存在而言,从小鼠癌细胞表面剔除CCDC25就能明显减轻LPS炎性诱导疗法后癌细胞向肝脏的转移;此前研究人员揭示了LPS在诱发与NETs相关的肺部转移过程中所扮演的关键角色,这项研究中,研究者表示,如果使用缺失CCDC25的小鼠来模拟自发乳腺癌小鼠(MMTV-PyMT小鼠),当进行LPS治疗时,肺部的癌细胞转移也会有类似的减少,有趣的是,CCDC25与NET DNA之间的相互作用在支持肺部转移中的角色或许会在感染的状况下发生,而其对肝脏转移的效应则是自发发生的。
研究者揭示了肿瘤细胞如何从与NETs的相互作用中获益,利用CCDC25作为诱饵的生化技术来捞出癌细胞中与CCDC25相互作用的蛋白,从而研究者就能识别出一种名为整联蛋白相关激酶(ILK),其能调节诸如细胞迁移和增殖等过程,当ILK被移除或其下游信号伴侣—β-parvin蛋白被失活时,体外癌细胞的生长和运动就会明显受损,同时小鼠机体中癌细胞向肝脏的转移也会减弱。相关研究结果表明,NET DNA与CCDC25之间的结合或能通过激活ILK介导的级联信号反应来增强恶性的癌细胞行为。
研究者Yang等人表示,NET DNA促进肝脏癌转移的能力并非乳腺癌细胞所特有的,在结肠癌患者的肝脏转移和注射了人类结肠癌细胞的小鼠肝脏中研究人员也观察到了NTEs,如果人类乳腺和结肠癌细胞能被工程化改造来增加CCDC25的水平,这或许就能促进给予此类细胞小鼠机体发生癌症转移,重要的是,研究者还在多种癌症类型患者机体中发现,原发性肿瘤中高水平的CCDC25与患者生存期较短之间存在一定关联,这就表明,监测CCDC25的表达或许能用作癌症预防的目的。
未来研究人员还需要进行研究来评估靶向CCDC25的抗癌疗法的可行性,研究人员还需要分析CCDC25在不同细胞类型中的表达情况及其在正常细胞中的可能性功能,如今研究者已经识别出了CCDC25与NET DNA相互作用的精确胞外部分,这或许就能帮助开发特殊的抑制剂来阻断其二者之间的相互作用,这种靶向性疗法或能有助于保存能帮助对抗感染的NETs的其它功能优势。相比其它转移位点,目前研究人员并不清楚为何肝脏中容易发生NET的积累,在哺乳动物患肠癌的情况下,中性粒细胞中NETs的释放或与补体C3a的上调有关,C3a主要在肝脏中产生,其能与中性粒细胞上的受体相结合。在肝脏转移发生之前,补体通路的激活就发生在哺乳动物肝脏中,因此研究者推测这或许是一种补体依赖性的NET形成的刺激,但具体的机制研究者并不清楚。
研究者Yang等人的研究结果代表了癌症扩散研究领域中一项非常有意义的进展,其或能帮助研究人员开发新型策略来抑制NET对癌症转移的促进作用,此外,相关研究数据还为研究人员提供了一种可能性的方法来通过监测血液中NET DNA的水平预测癌症的转移状况。(生物谷Bioon.com)
参考资料:
Emma Nolan & Ilaria Malanchi. Neutrophil ‘safety net’ causes cancer cells to metastasize and proliferate, Nature (2020) doi:10.1038/d41586-020-01672-3
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


