镰状细胞病自体干细胞基因疗法!Aruvant胎儿血红蛋白基因疗法ARU-1801获美国FDA孤儿药资格!
来源:本站原创 2020-01-23 14:01
2020年01月23日讯 /生物谷BIOON/ --Roivant Sciences旗下公司Aruvant Sciences是一家临床阶段的生物制药公司,专注于开发和商业化变革性疗法,用于严重血液疾病的治疗。近日,该公司宣布,美国食品和药物管理局(FDA)已授予ARU-1801治疗镰状细胞病(SCD)的孤儿药资格(ODD)。之前,FDA还授予了ARU-180

2020年01月23日讯 /生物谷BIOON/ --Roivant Sciences旗下公司Aruvant Sciences是一家临床阶段的生物制药公司,专注于开发和商业化变革性疗法,用于严重血液疾病的治疗。近日,该公司宣布,美国食品和药物管理局(FDA)已授予ARU-1801治疗镰状细胞病(SCD)的孤儿药资格(ODD)。之前,FDA还授予了ARU-1801治疗SCD的罕见儿科疾病资格认定(RPD)。
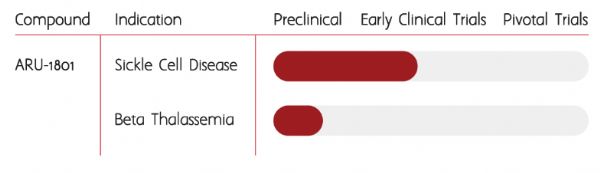
ARU-1801是一种改良的胎儿血红蛋白(fetal hemoglobin)基因疗法,开发用于治疗镰状细胞病(SCD)和β地中海贫血。该疗法利用了专有技术,通过慢病毒载体将经过修饰的胎儿血红蛋白基因插入自体干细胞,以增加功能性红细胞。研究表明,胎儿血红蛋白水平升高的镰状细胞患者较少发生血管阻塞性危象和住院,部分原因是胎儿血红蛋白相对于成人血红蛋白(adult hemoglobin)的特性有所改善。
ARU-1801是目前已知的唯一一种递送胎儿血红蛋白编码基因的临床阶段基因疗法,其中的胎儿血红蛋白编码基因已被改进以优化携氧能力和抗镰刀特性。Aruvant公司正开发ARU-1801作为治疗SCD和β地中海贫血的一种潜在的一次性疗法。
ARU-1801经设计用来递送一种具有强化抗镰刀特性的高效基因负载,允许对患者采用一种减低强度预处理方案(RIC)。目前,用于镰状细胞病的其他研究性基因疗法需要使用高强度清髓预处理方案,这与长期住院和许多可能严重的并发症有关。RIC将为患者提供一种改善风险效益的治疗方案,包括降低不孕风险和减少住院天数。
Aruvant首席执行官Will Chou表示:“我们很高兴ARU-1801在之前罕见儿科疾病资格认定(RPD)的基础上又获得了FDA的孤儿院资格认定(ODD)。对于镰状细胞病患者,我们相信,基因治疗的终极潜力是一次性治愈、没有高强度清髓治疗方案的副作用。我们致力于为患者提供这一选择,并期待着在我们正在进行的I/II期研究中,随着患者继续接受治疗,我们提供更多关于减低强度预处理方案(RIC)的数据。”
孤儿药(Orphan Drug)是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称,又称“孤儿病”。在美国,罕见病是指患病人群少于20万的疾病类型,罕见病药物研发方面的激励措施包括各种临床开发激励措施,如临床试验费用相关的税收抵免、FDA用户费减免、临床试验设计中FDA的协助,以及药物上市后针对所批准适应症为期7年的市场独占期。
FDA的罕见儿科疾病资格针对的是主要影响18岁及以下且影响人群不足20万的严重、危及生命的疾病。该项目旨在鼓励开发用于预防和治疗罕见儿科疾病的新药和生物制剂。如果ARU-1801的生物制品许可申请(BLA)获得批准,Aruvant公司将有资格获得优先审评券(PRV),该券可以兑换以获得任何后续新药申请的优先审查,并且可以出售或转让。
镰状细胞病(SCD)是一种逐渐衰弱和危及生命的遗传性红细胞疾病,导致患者携氧细胞异常不灵活和镰刀形。这种遗传缺陷导致这些红血球血红蛋白蛋白质的携氧能力降低。镰状细胞病可引起四肢发炎、细菌感染、中风、贫血和称为镰状细胞危机的疼痛发作。
β地中海贫血是一种遗传性红细胞疾病,其特征是功能性β-珠蛋白的生成减少或不存在,这是成人血红蛋白的重要组成部分。这种疾病的患者患有贫血,贫血会导致虚弱、疲劳和更严重的并发症。β地中海贫血患者发生异常血栓的风险增加。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


