Incyte强效FGFR抑制剂pemigatinib在欧洲进入审查
来源:新浪医药新闻 2020-01-12 10:19
Incyte公司近日宣布,欧洲药品管理局(EMA)已受理靶向抗癌药pemigatinib的营销授权申请(MAA),这是一种选择性成纤维细胞生长因子受体(FGFR)抑制剂,用于治疗接受过至少一种系统疗法后病情复发或难治、携带FGFR2融合或重排、局部晚期或转移性胆管癌(cholangiocarcinoma)成人患者。EMA已启动MAA的正式审查程序,如果获得批
Incyte公司近日宣布,欧洲药品管理局(EMA)已受理靶向抗癌药pemigatinib的营销授权申请(MAA),这是一种选择性成纤维细胞生长因子受体(FGFR)抑制剂,用于治疗接受过至少一种系统疗法后病情复发或难治、携带FGFR2融合或重排、局部晚期或转移性胆管癌(cholangiocarcinoma)成人患者。
EMA已启动MAA的正式审查程序,如果获得批准,pemigatinib将成为欧洲治疗胆管癌的首个靶向疗法。在美国,FDA在去年11月受理了pemigatinib的新药申请并授予了优先审查。
pemigatinib的MAA基于FIGHT-202研究(NCT02924376)的数据。这是一项开放标签、多中心II期研究,正在评估pemigatinib在先前接受过治疗的局部晚期或转移性胆管癌成人患者中的疗效和安全性。这些患者根据FGF/FGFR状态被纳入三个队列中的一个:队列A(FGFR2融合或重排)、队列B(其他FGF/FGFR基因改变)、队列C(无FGF/FGFR基因改变)。研究中,所有患者均接受pemigatinib治疗,每日口服一次13.5mg,21天为一个周期(2周服药/1周停药),直至放射学疾病进展或不可接受的毒性。
研究的主要终点是队列A的总缓解率(ORR),根据实体瘤疗效评价标准(RECIST v1.1)进行独立评估。次要终点包括:队列B、A+B、C的ORR,所有队列的无进展生存期(PFS)、总生存期(OS)、缓解持续时间(DOR)、疾病控制率(DCR)和安全性。
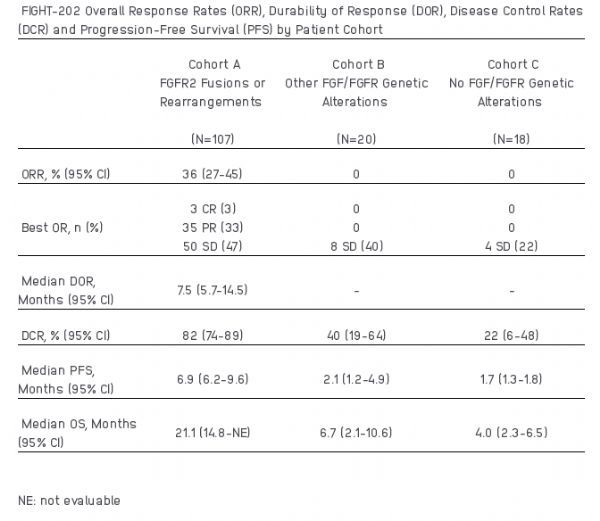
研究结果于2019年9月底在欧洲肿瘤内科学会(ESMO)会议上公布。数据显示,中位随访15个月,基于独立中心放射学审查结果,队列A的ORR为36%(95%CI:27-45),中位PFS为6.9个月(95%CI:6.2-9.6)、中位OS为21.1个月(95%CI:14.8-NE)、中位DOR为7.5个月(95%CI:5.7-14.5)、DCR为82%(95%CI:74-89)。
该研究中,pemigatinib总体上耐受性良好。最常见的治疗出现的不良事件(TEAE)是1级或2级高磷血症(60%),可通过低磷饮食、磷酸盐结合剂和利尿剂、剂量减少或中断来管理。最常见的3级TEAE是低磷血症(12%),没有一例被认为有临床意义或严重,没有一例导致剂量减少或停药。有4%的患者(≥3级,1%)出现浆液性视网膜脱离,没有一例出现临床后遗症。
pemigatinib(FGFR抑制剂,图片来源:medchemexpress.cn)
胆管癌是一种罕见的胆管癌症。肝内胆管癌(iCCA)发生于肝内胆管,肝外胆管癌发生于肝外胆管。胆管癌患者在确诊时通常已处于预后不佳的后期或晚期阶段。胆管癌的发病率因地区而异,在欧洲为0.4-1.8/100000。FGFR2融合或重排几乎只发生在iCCA中,在10-16%的患者中观察到。
成纤维细胞生长因子受体(FGFR)在肿瘤细胞增殖、存活、迁移和血管生成(新生血管的形成)中起着重要作用。FGFR中的融合、重排、易位和基因扩增与多种肿瘤的发生发展密切相关。pemigatinib是FGFR异构体1、2、3的强效、选择性、口服小分子抑制剂,在临床前研究中被证实针对FGFR基因改变的癌细胞具有选择性药理学活性。
FIGHT临床项目包括多项正在进行中的II期和III期试验,正评估pemigatinib治疗多种FGFR驱动的恶性肿瘤,包括:II期单药研究(FIGHT-202:治疗胆管癌,FIGHT-201:治疗膀胱癌;FIGHT-203:治疗骨髓增生性肿瘤;FIGHT-207:治疗FGFR改变的实体瘤)、II期组合研究(FIGHT-205:pemigatinib联合Keytruda、pemigatinib单药疗法一线治疗膀胱癌)、III期研究(FIGHT-302:pemigatinib一线治疗FGFR2融合或重排胆管癌)。
2018年12月,信达生物与Incyte公司达成战略合作和独家授权许可协议,推进3款药物(itacitinib,parsaclisib,pemigatinib)的单药或联合治疗在中国内地及香港、澳门和台湾地区的临床开发与商业化。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->