新适应症再望!辉瑞Xeljanz治疗幼年特发性关节炎III期成功
来源:新浪医药新闻 2019-11-14 18:33
日前,在亚特兰大举行的美国风湿病学会/风湿病卫生专业人员协会(ACR/ARP)2019年年会上,辉瑞公布了Xeljanz(tofacitinib)治疗2-18岁以下幼年特发性关节炎(JIA)患者关键性III期临床研究A3921104(NCT02592434)的结果。数据显示,在伴有多关节病程的JIA(pcJIA)患者中,与安慰剂相比,Xeljanz治疗显着降低了疾病耀斑发生
日前,在亚特兰大举行的美国风湿病学会/风湿病卫生专业人员协会(ACR/ARP)2019年年会上,辉瑞公布了Xeljanz(tofacitinib)治疗2-18岁以下幼年特发性关节炎(JIA)患者关键性III期临床研究A3921104(NCT02592434)的结果。
数据显示,在伴有多关节病程的JIA(pcJIA)患者中,与安慰剂相比,Xeljanz治疗显着降低了疾病耀斑发生率、推迟了耀斑发生时间、改善了疾病体征/症状和身体功能、在疾病活动度方面具有持续的临床意义的改善,安全性与治疗类风湿性关节炎(RA)成人患者中的安全性一致。基于该研究结果,辉瑞计划在2020年向美国FDA提交Xeljanz治疗pcJIA的新适应症申请。
A3921104是一项随机、双盲、安慰剂对照停药研究,包括两个部分。在导入期,所有患者接受为期18周的开放标签Xeljanz治疗。在18周导入期结束时,只有达到至少JIA ACR30缓解的患者被随机分配进入为期26周的双盲、安慰剂对照、撤出期,以1:1比例随机分配继续接受Xeljanz或停药Xeljanz并接受安慰剂治疗直至第44周研究结束。研究评估了Xeljanz作为5毫克片剂或1毫克/毫升口服溶液每日2次(BID)的疗效和安全性,给药剂量根据患者体重进行调整:体重<40公斤,2-4毫克BID;体重≥40公斤,5毫克BID。
主要终点是治疗44周的疾病耀斑发生率,关键次要终点是治疗第44周时的JIA ACR50/30/70缓解率、儿童健康评估问卷残疾指数(CHAQ-DI)相对第二阶段基线的变化。研究中,疾病耀斑定义为:JIA核心集(JIA临床试验中使用的结果评估工具)中六个变量中至少有三个变量恶化30%或更多。
在导入期,共225例患者入组并接受了Xeljanz治疗,其中包括:伴多关节病程JIA(pcJIA,n=184)、银屑病关节炎(PsA,n=20)或末端炎相关关节炎(ERA,n=21)。在治疗第18周,173/225(76.9%)患者进入第二部分(pcJIA,n=142;PsA,n=15;ERA,n=16)。
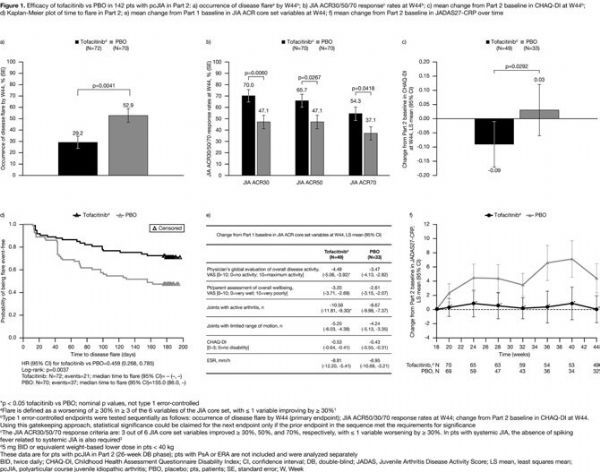
数据显示,研究达到主要终点:在pcJIA患者中,至第44周,在研究第二部分中Xeljanz治疗组疾病耀斑发生率显着低于安慰剂组(29.2% vs 52.9%;p=0.0041;图1a)。JIA ACR50/30/70缓解率(图1b)以及CHAQ-DI从第二部分基线的变化(图1c),Xeljanz治疗组均高于安慰剂组,具体数据为:JIA ACR30缓解率(70.0% vs 47.1%;p=0.0060)、JIA ACR50缓解率(65.7% vs 47.1%;p=0.0267)、JIA ACR70缓解率(54.3% vs 37.1%,p=0.0418)、CHAQ-DI(-0.09 vs +0.03;p=0.0292)。
在第二部分,Xeljanz治疗组发生疾病耀斑(发病期间疾病活动增加称为耀斑)的时间较安慰剂组推迟(p=0.0037;图1d)。在第44周,采用JIA ACR核心集变量相对第一部分基线的变化进行评估,Xeljanz与安慰剂相比在减少pcJIA体征和症状方面具有更大的疗效(图1e)。从第二部分的早期时间点开始,安慰剂组疾病活动度(采用JADAS27-CRP评估)恶化,而Xeljanz治疗组疾病活动度保持稳定(图1f)。
研究中,Xeljanz治疗患者和安慰剂患者中的安全性相似(表2),不良事件发生率分别为77.3%和74.1%,严重不良事件发生率分别为1.1%和2.4%。最常见的不良事件为上呼吸道感染、头痛、鼻咽炎、恶心、发热、病情恶化、呕吐和JIA。没有发生死亡、主要心血管不良事件(MACE)、恶性肿瘤、血栓形成、机会性感染或肺结核病例。整个研究过程中,Xeljanz治疗组发生两例带状疱疹和四例严重感染。
Xeljanz是一种口服JAK抑制剂,可选择性抑制JAK激酶,阻断JAK/STAT通路,该信号通路是近年来发现的一条由细胞因子刺激的信号转导通路,参与细胞的增殖、分化、凋亡以及免疫调节等许多重要的生物学过程。
在美国,Xeljanz于2012年获批,成为上市的首个JAK抑制剂。该药已被批准三个适应症:治疗中度至重度活动性RA成人患者;治疗活动性银屑病关节炎成人患者;治疗中度至重度溃疡性结肠炎成人患者。当前,辉瑞正在推进一个庞大的临床项目,评估Xeljanz用于多种免疫介导性炎症疾病的治疗。
科睿唯安:JAK抑制剂竞争格局
当前,Xeljanz是JAK抑制剂领域的领头羊。根据辉瑞在10月底发布的业绩报告,Xeljanz今年前9个月销售额16.34亿美元,较2018年同期增长34%,其中美国市场增长25%、国际市场增长69%。
然而,围绕Xeljanz高剂量(10mg)的安全性问题一直不断。特别是今年上半年,美国FDA和欧盟EMA因肺栓塞和死亡率不平衡均对10mg Xeljanz发布了安全警告和限制,这无疑会对Xeljanz的商业前景带来不利影响。另一方面,礼来Olumiant、艾伯维Rinvoq、吉利德预期上市的filgotinib,都将对Xeljanz施加更大的竞争压力。特别是Rinvoq和filgotinib,这2款药物在临床研究中表现出了高安全性。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。