全球埃博拉疫苗!默沙东减毒活疫苗ERVEBO(V920)年底将获欧盟批准,美国在明年3月!
来源:本站原创 2019-10-23 10:10
2019年10月23日讯 /生物谷BIOON/ --默沙东(Merck & Co)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布一项积极意见,推荐有条件批准V920扎伊尔埃博拉疫苗(rVSV∆G-ZEBOV-GP,减毒活疫苗)。现在,CHMP的意见将由欧盟委员会(EC)审查,该机构预计将在第四季度作出审查决定。如果获得批准,这款疫苗的品牌名将为ERVEB

2019年10月23日讯 /生物谷BIOON/ --默沙东(Merck & Co)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布一项积极意见,推荐有条件批准V920扎伊尔埃博拉疫苗(rVSV∆G-ZEBOV-GP,减毒活疫苗)。现在,CHMP的意见将由欧盟委员会(EC)审查,该机构预计将在第四季度作出审查决定。如果获得批准,这款疫苗的品牌名将为ERVEBO®,用于18岁及以上人群的主动免疫,以预防扎伊尔型埃博拉病毒(Ebola Zaire)引起的埃博拉病毒病(EVD)。之前,EMA已授予V920优先药物资格(PRIME)。
目前,V920也正在接受美国FDA的审查,该机构于今年9月中旬受理了V920的生物制品许可申请(BLA)并授予了优先审查,预计将在2020年3月14日作出审查决定。此前,FDA还授予了V920突破性药物资格。除了与FDA和EMA密切合作,默沙东还向世界卫生组织(WHO)提交了获得资格预审的材料,并向非洲疫苗监管论坛(AVAREF)提交了材料。
默克研究实验室总裁Roger M.Perlmutter博士表示:“CHMP的这一积极审查意见代表了在扎伊尔埃博拉病毒(Ebola Zairevirus)感染地区为民众提供一种许可疫苗方面取得的重要进展。如果没有无数人的努力,特别是来自世界卫生组织(WHO)和许多其他政府和非政府组织人士,我们的工作是不可能完成的,他们为研制这一重要疫苗作出了不懈的努力。我们的首要任务是完成我们德国ERVEBO生产基地的注册,以便获得许可生产供应,用于支持全球公共卫生准备。”
在努力推进监管审查的同时,默沙东仍继续致力于稳步扩大生产V920的试验性剂量,以帮助国际公共卫生官员和政府当局应对持续、不可预测和不断变化的疫情反应,以及在刚果民主共和国和邻国不断变化的需求。自2018年5月以来,默沙东应世界卫生组织(WHO)请求,向WHO捐赠并运送了超过24万支1.0ml试验性V920疫苗。除了已经交付的剂量外,目前还有19万多个额外的1.0ml试验性剂量可供使用,并准备应WHO的请求运送到疫情暴发地区。
此外,2019年6月,根据与美国卫生和公众服务部、WHO和全球疫苗联盟正在进行的磋商,默沙东开始执行一项更新的补充战略,以增加试验性V920埃博拉疫苗供应。该战略的目标是在未来6至18个月内,以分阶段的方式分发和提供额外的估计65万份1.0ml试验性剂量。总的来说,过去、现在和即将生产的V920的试验性剂量将超过90万份1.0ml。
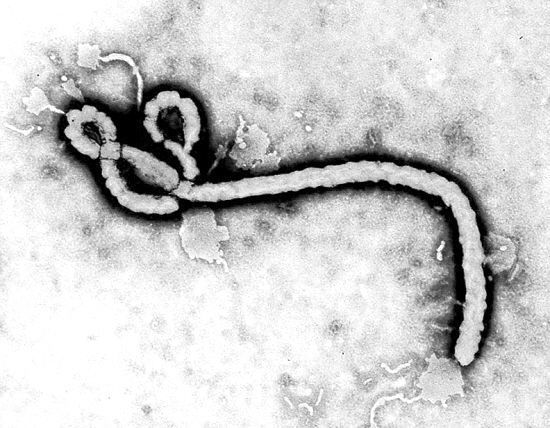
埃博拉病毒(Ebola)是导致埃博拉出血热(EHF)的元凶,该病是一种急性病毒性出血性传染病,症状包括:发烧、头痛、关节和肌肉疼痛、乏力、腹泻、呕吐、胃痛、食欲不振及异常出血。这些症状可在病毒感染后2-21天内出现,但最常见于8-10天。埃博拉病毒不是一种经水传播(water-borne)或食物传播的疾病,也不通过空气传播,该病通过直接接触受感染者体液或已被病毒污染的器具(如针头)传播。
V920采用了一种有缺陷的、能够感染家畜的水泡性口炎病毒,将病毒的一种基因用埃博拉病毒的基因替换。V920最初是由加拿大公共卫生署(PHAC)开发,之后在2010年授权给了NewLink Genetics公司。2014年底,当非洲西部埃博拉疫情达到高峰时,默沙东从NewLink公司签署了一项全球独家授权协议,获得了这款埃博拉疫苗。之后,默沙东一直与一些外部合作者密切合作,在美国政府的部分资助下,开展了一项广泛的临床开发项目,其中包括美国卫生和人类服务部的生物医学高级研究及发展管理局(BARDA)以及美国国防部威胁减少管理局(DTRA)和联合疫苗采办计划(JVAP)等。V920的试验性供给活动由BARDA根据合同号HHSO100201700012C提供部分联邦资金支持。默沙东负责V920的研究、开发、制造及监管工作,该公司已承诺与其他利益相关方密切合作,加速疫苗的持续开发、生产和分销。
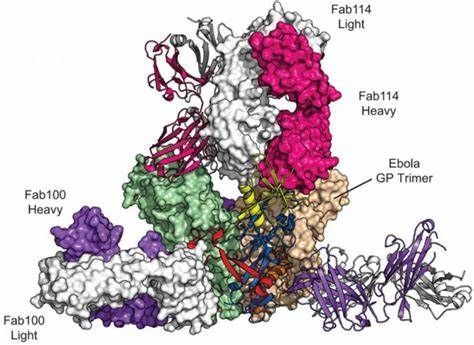
图片来自:labiotech.eu
值得一提的是,今年9月初,FDA授予了Ridgeback Biotherapeutics公司单抗药物mAb114突破性药物资格,这是一种治疗性单抗,起源于1995年刚果民主共和国基奎特市的埃博拉疫情。在那次疫情中,幸存者在感染埃博拉长达十一年后仍保留抗埃博拉抗体,研究人员从这些幸存者体内分离出了抗体,其中mAb114是最有前途的一种。
此次BTD授予,是基于Pamoja Tulinde Maisha(PALM,共同拯救生命)研究的中期数据。该研究测试了4种疗法,包括3种抗体疗法(抗体鸡尾酒ZMapp、三种单抗混合物REGN-EB3[再生元公司]、单克隆抗体mAb114)和一款抗病毒药物remdesvir(吉利德公司),其中ZMapp用作对照。
今年8月公布的来自499例受试者的初步评估结果显示:接受REGN-EB3和mAb114治疗的受试者比其他两组受试者有更大的生存机会。具体数据为:(1)remdesvir、ZMapp、mAb114、REGN-EB3治疗的感染者死亡率分别为53%、49%、34%、29%;(2)在感染后早期治疗且血液病毒水平较低的患者中,数据更强,死亡率分别为:33%、24%、11%、6%。
而目前,整个埃博拉疫情的死亡率为67%。基于上述数据,PALM研究已提前终止,并选择REGN-EB3和mAb114作为扩展期中用于所有未来患者随机治疗的药物,以进一步评估评估安全性直至获得最终临床试验结果。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


