眼科创新药!艾尔建3月一次抗VEGF疗法abicipar申请上市,治疗湿性年龄相关性黄斑变性(AMD)
来源:本站原创 2019-09-10 11:00
2019年09月10日讯 /生物谷BIOON/ --艾尔建(Allergan)与合作伙伴Molecular Partners近日联合宣布,眼科药物abicipar pegol治疗新生血管(湿性)年龄相关性黄斑变性(nAMD)的新药申请(NDA)已被美国食品和药物管理局(FDA)受理,预计在2020年年中获得审查结果。此外,该药的营销授权申请(MAA)已被欧洲药品管理局(EMA)受理,预计在2020

2019年09月10日讯 /生物谷BIOON/ --艾尔建(Allergan)与合作伙伴Molecular Partners近日联合宣布,眼科药物abicipar pegol治疗新生血管(湿性)年龄相关性黄斑变性(nAMD)的新药申请(NDA)已被美国食品和药物管理局(FDA)受理,预计在2020年年中获得审查结果。此外,该药的营销授权申请(MAA)已被欧洲药品管理局(EMA)受理,预计在2020年下半年获得审查结果。
BLA和MAA基于2项头对头III期临床研究(SEQUOIA,CEDAR)的数据,结果支持了abicipar每季度一次给药方案与罗氏/诺华Lucentis(ranibizumab,雷尼珠单抗)每月一次方案相比在第一年注射次数减少50%以上(6次 vs 13次)的情况下维持视力的非劣性疗效。
SEQUOIA研究和CEDAR研究比较了abicipar与ranibizumab在先前未接受治疗(初治)nAMD患者中的疗效和安全性。结果证实,在第52周,abicipar 8周(Q8)和12周(Q12)固定间隔治疗方案与ranibizumab 4周(RQ4)间隔给药方案在稳定视力(最佳矫正视力[BCVA]相对于基线视力损失≤15个字母)主要终点达到了非劣效性。
abicipar注射6针(Q12方案)和注射8针(Q8方案)与ranibizumab注射13针(RQ4方案)治疗一年取得了相似疗效:SEQUOIA研究中,Q8组、Q12组、RQ4组实现稳定视力的患者比例分别为94.8%、91.3%、96.0%;CEDAR研究中,Q8组、Q12组、RQ4组实现稳定视力的患者比例分别为91.7%、91.2%、95.5%。安全性方面,3个治疗组中总体不良反应相似,abicipar治疗组眼内炎症发生率较高:SEQUOIA研究,Q8组、Q12组、RQ4组中,总体治疗相关不良事件发生率分别78.3%、78%、74%,眼内炎症事件发生率分别为15.7%、15.3%、0.6%。CEDAR研究,Q8组、Q12组、RQ4组中,总体治疗相关不良事件发生率分别73.7%、81.1%、73.2%,眼内炎症事件发生率分别为15.1%、15.4%、0%。
今年4月,艾尔建公布了另一项临床研究MAPLE的顶线安全结果。该研究是一项为期28周的开放标签研究,入组了123例nAMD患者,评估了通过改进制造工艺生产的abicipar的安全性。研究中,先前未接受治疗(初治)或已接受抗血管内皮生长因子(VEGF)疗法治疗的患者,接受3次每月一次2mg剂量abicipar注射,之后接受每2月一次2mg剂量注射,直至第28周共接受5次注射。
由于制造工艺的改进,MAPLE研究中的眼内炎症(IOI)发生率为8.9%,低于之前III期研究中观察到的发生率。大多数IOI事件的严重程度为轻度到中度。严重IOI的发病率为1.6%,其中一例报告为虹膜炎,一例报告为葡萄膜炎。该研究未报告眼内炎或视网膜血管炎的病例。
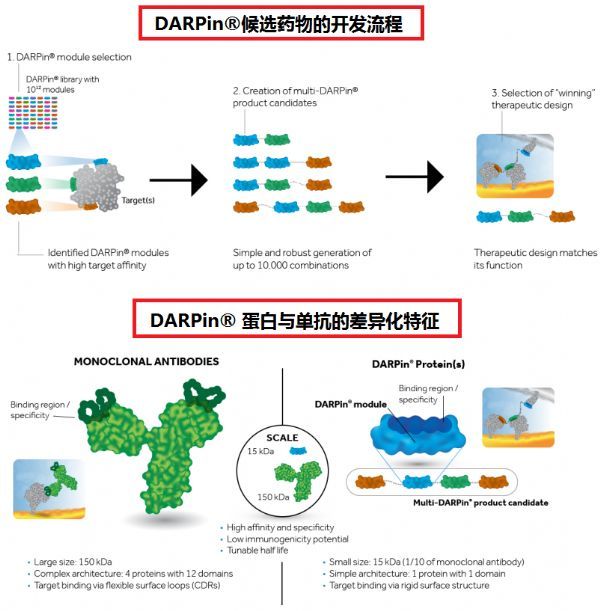
艾尔建于2011年与Molecular Partners达成眼科学战略合作,开发新型multi-DARPin产品。DARPin(设计的锚蛋白重复蛋白)是一类衍生自天然锚蛋白重复序列(ANK)的新型结合蛋白。锚蛋白是自然界最常见的一类具有结合作用的蛋白,负责各种不同的功能,如细胞信号转导和受体结合。DARPin蛋白具有分子质量小、高效力、高稳定性、高亲和力和具备柔性结构等诸多有点,在临床治疗领域有极大应用价值。
abicipar是一种基于DARPin技术的抗血管生成药物,开发用于nAMD和DME的治疗。abicipar是血管内皮生长因子A(VEGF-A)的拮抗剂,可高效抑制VEGF-A所有相关亚型。abicipar集小尺寸、高效力、玻璃体内长半衰期特性于一体,可提供较低的注射频率(与Lucentis相比,当前的标准护理疗法)和更高的视力增益。
艾尔建首席研发官David Nicholson表示:“abicipar监管文件在美国和欧盟被受理,使我们更接近于为患者和医生提供一种新的治疗方案,该方案有潜力减少患者就诊和注射,通过每季度一次给药实现和保持视力,该药将成为一款变革性的治疗药物,解决nAMD患者中的未满足医疗需求。”
Molecular Partners首席运营官Michael T. Stumpp表示:“FDA的受理标志着DARPin?技术的一个重要里程碑,因为abicipar是我们第一个获得FDA受理的DARPin候选药物,该药将成为一款真正的每季度给药一次的抗VEGF药物,将帮助nAMD患者提高视力和改善生活质量。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->