东阳光GLP-1/FGF21双重激动剂HEC88473注射液获批临床
CDE官网显示,东阳光开发的新药HEC88473注射液临床试验申请已获国家药监局默认许可,拟开展2型糖尿病和减重临床研究。HEC88473是国内首个获批临床的GLP-1/FGF21双重激动剂。HEC88473注射液是东阳光药2021年首个提交临床申请的1类新药;德谷胰岛素注射液是一种新型的、超长效应的胰岛素类似物,2019年全球销售额
苑东生物枸橼酸咖啡因注射液通过注射剂质量和疗效一致性评价
2月24日,苑东生物发公告,公司于近日收到国家药监局核准签发的化学药品“枸橼酸咖啡因注射液”的《药品补充申请批准通知书》,该品种用于治疗早产新生儿原发性呼吸暂停。枸橼酸咖啡因注射液于 1997 年 12 月 31 日在法国获准用于治疗早产新生儿原发性呼吸暂停。1998 年 9 月获得美国孤儿药资格,并于 1999 年 9 月 21 日
国家药监局发布关于修订门冬氨酸鸟氨酸注射剂说明书的公告
12月29日,国家药监局官网发布一则关于修订门冬氨酸鸟氨酸注射剂说明书的公告,对该注射剂(包括门冬氨酸鸟氨酸注射液、注射用门冬氨酸鸟氨酸)说明书【不良反应】、【注意事项】、【禁忌】、【孕妇及哺乳期妇女用药】、【儿童用药】、【老年用药】项进行修订。具体公告内容如下:国家药监局关于修订门冬氨酸鸟氨酸注射剂说明书的公告(2020年第121号)为进一步保障公众用药安
霍尼韦尔推出Aclar® Edge™创新型口服液体制剂瓶和无菌注射剂瓶 ——生物谷专访霍尼韦尔Aclar® Edge™项目的负责人
2020年7月2日,霍尼韦尔近日推出创新医药包装解决方案Aclar®Edge™(阿克拉®Edge™),用于人类健康口服液体制剂和动物健康无菌注射剂。Aclar Edge口服液体制剂瓶和注射剂瓶均采用霍尼韦尔新型多层共挤吹塑专利技术,可确保大部分液体剂型的保质期和功效,同时显着提升用户操作处理和给药过程的安全性。
国家药监局发文 化药注射剂一致性评价正式启动
5月14日,国家药监局发布《国家药监局关于开展化学药品注射剂仿制药质量和疗效一致性评价工作的公告》。相关解读如下:一、《国家药监局关于开展化学药品注射剂仿制药质量和疗效一致性评价工作的公告》出台的背景是什么?答:为贯彻落实国务院关于加快推进仿制药一致性评价的工作部署,国家药监局仿制药一致性评价办公室组织专家委员会制定了《化学药品注射剂仿制药质量和疗效一致性评
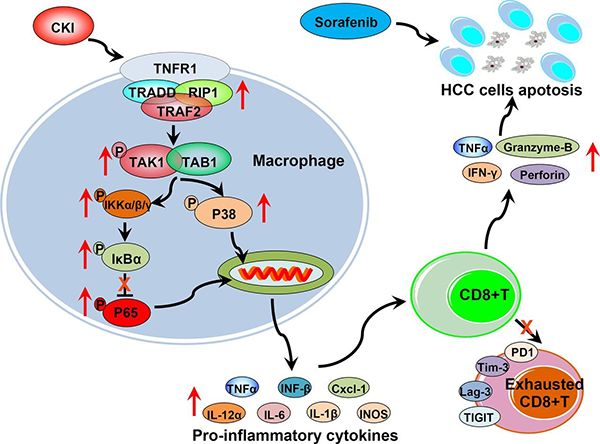
研究揭示中药复方苦参注射液增敏索拉菲尼治疗肝癌新机制
3月15日,肿瘤免疫治疗学会(The Society for Immunotherapy of Cancer, SITC)会刊Journal for ImmunoTherapy of Cancer 在线发表了中国科学院上海营养与健康研究所及上海交通大学公共卫生学院王慧研究组的研究论文“Compound kushen injection relieves tu
美国FDA批准Barhemsys(氨磺必利注射剂),用于预防/抢救性治疗!
2020年02月28日讯 /生物谷BIOON/ --Acacia制药集团近日宣布,美国食品和药物管理局(FDA)已批准Barhemsys(amisulpride injection,氨磺必利注射剂)用于成人患者,预防和治疗术后恶心呕吐(PONV)。Barhemsys的批准涵盖了已使用一种不同类别的止吐药预防性治疗PONV的手术患者或没有接受止吐药预防性治疗P
武田皮下注射剂型Entyvio治疗2种炎症性肠病在欧盟进入审查!
2020年02月29日讯 /生物谷BIOON/ --武田(Takeda)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布一份积极审查意见,建议批准皮下注射(SC)剂型的肠道选择性生物制剂Entyvio(vedolizumab),作为一种维持疗法,用于中度至重度溃疡性结肠炎(UC)或克罗恩病(CD)成人患者的治疗。该皮下制剂产品包括预充式