欧盟CHMP推荐批准辉瑞2款JAK抑制剂Cibinqo(阿布昔替尼)和XELJANZ(托法替尼)!
欧盟CHMP建议批准:Cibinqo治疗特应性皮炎,XELJANZ治疗强直性脊柱炎。
2021-10-22
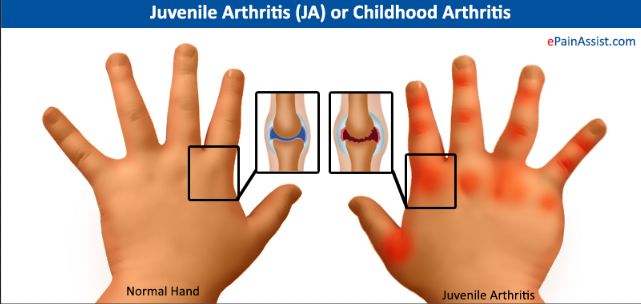
欧盟批准辉瑞JAK抑制剂XELJANZ(托法替尼):治疗2种亚型的幼年特发性关节炎(JIA)!
XELJANZ是欧洲第一个也是唯一一个治疗多关节型幼年特发性关节炎(pcJIA)和幼年型银屑病关节炎(PsA)的JAK抑制剂。
2021-08-23
辉瑞发布XELJANZ治疗RA患者上市后所需安全性研究结果
辉瑞宣布了类风湿关节炎(RA)药物XELJANZ(tofacitinib,托法替尼)最近完成的上市后安全性研究ORAL Surveillance(A3921133;NCT02092467)的共同主要终点结果,分析显示,预先指定的非劣效性标准没有得到满足。辉瑞介绍,ORAL Surveillance研究的主要目的是评估两种剂量(5毫克和
2021-02-02
用于青少年特发性关节炎 辉瑞XELJANZ在美获批第四项适应症
9月28日,辉瑞宣布,美国FDA批准XELJANZ?(tofacitinib,托法替尼)用于治疗活动性多关节病程的青少年特发性关节炎(pcJIA)2岁及以上儿童和青少年患者。此次批准了两种配方,一种是片剂,另一种是口服溶液,需要根据患者体重给药。辉瑞表示,XELJANZ口服液剂型预计在2021年第一季度末上市,而5毫克的片剂将立即上市。这项批准使得XELJA
2020-10-02
辉瑞XELJANZ XR(托法替尼缓释片)获美国FDA批准,首个每日一次的JAK抑制剂!
2019年12月13日讯 /生物谷BIOON/ --辉瑞(Pfizer)近日宣布,美国食品和药物管理局(FDA)已批准XELJANZ XR(tofacitinib,托法替尼)缓释片11毫克和22毫克,用于治疗对TNF阻滞剂应答不足或不耐受的中度至重度活动性溃疡性结肠炎(UC)成人患者。XELJANZ XR将为中重度活动性UC成人患者提供第一种也是唯一一种每日
2019-12-13