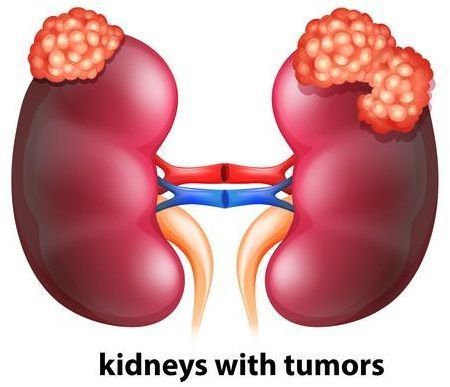
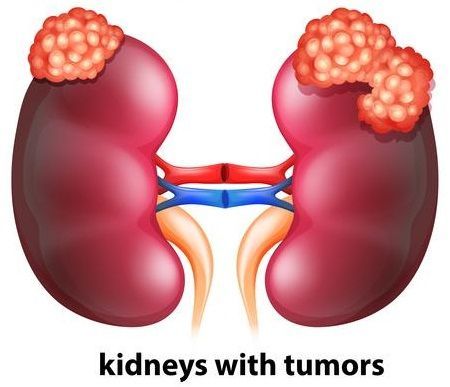
口服下一代VEGF-TKI Fotivda上市:疗效击败拜耳Nexavar(多吉美)!
Fotivda是一种口服、下一代血管内皮生长因子受体(VEGFR)酪氨酸激酶抑制剂(TKI)。
2021-03-23
拜耳肝癌药物Nexavar成功加入英国医保体系
近日,拜耳旗下药物Nexavar(索拉非尼)已获得英国国家卫生与临床技术优化研究所(NICE)推荐纳入英格兰地区医疗保障体系,用于治疗晚期肝细胞癌(HCC)患者(肝功能分级A级肝损伤以及手术失败或者不适合手术及局部区域治疗)。自2010年以来,患者可以通过癌症药物基金会获得Nexavar的治疗机会。此次,英国国家卫生与临床技术优化研究所将其纳入医保计划当中,将意味着医生和患者现在可以通
2017-08-11
拜耳多吉美(Nexavar)HER2阴性乳腺癌III期RESILIENCE研究失败
拜耳多吉美(Nexavar)HER2阴性乳腺癌III期研究(RESILIENCE)失败,该项研究未能达到无进展生存期(PFS)主要终点。
2014-07-25
拜耳多吉美(Nexavar)甲状腺癌新适应症获日本批准
拜耳多吉美(Nexavar)获日本批准,用于不可切除性分化型甲状腺癌的治疗,这是Nexavar获批的第三个适应症。此前,MHLW已授予Nexavar治疗甲状腺癌的孤儿药地位。
2014-06-20
拜耳多吉美(Nexavar)新适应症获欧盟批准
拜耳多吉美Nexavar获欧盟批准,用于用于局部晚期或转移性放射性碘(RAI)难治性分化型甲状腺癌(DCT)的治疗。此前,FDA已于去年11月批准了该药的新适应症。
2014-06-04
拜耳多吉美(Nexavar)新适应症获FDA批准
拜耳抗癌药多吉美(Nexavar)获FDA批准,用于局部晚期或转移性放射性碘(RAI)难治性分化型甲状腺癌的治疗,是FDA批准用于这一疾病的首个药物。
2013-11-25
拜耳试图阻止印度多吉美(Nexavar)仿制药举动再次遭到MSF谴责
2012年9月5日讯 /生物谷BIOON/ --德国制药巨头——拜耳(Bayer)昨日前往印度知识产权上诉委员会(Intellectual Property Appellate Board),要求推翻有关抗癌药多吉美(Nexavar)的强制许可,该许可已允许出于公共卫生利益,生产更实惠的Nexavar仿制药。
2012-09-06