又一款BTK抑制剂被FDA部分临床暂停
4月12日,德国默克(Merck KGaA)公司宣布,FDA对evobrutinib新招募患者和给药不足70天的患者实施部分临床暂停。不过,在美国正在进行的evobrutinib治疗复发性多发性硬化症
NASH新药获FDA突破性疗法认定,本季度将申报上市
4月18日,Madrigal Pharmaceuticals宣布FDA授予resmetirom治疗伴有肝纤维化的非酒精性脂肪性肝炎 (NASH) 患者的
上市12年后,FDA正式宣布早产预防药Makena撤市
4月6日,FDA宣布,撤销对Makena的上市批准。在加速审批途径下,Makena曾被批准用于降低有自发性早产史的孕妇的早产风险。从即日起,Makena及其仿制药不再被批准
全球首款TIL细胞疗法完成FDA滚动上市申报
据报道,全球每年约有32.5万新发黑色素瘤患者,其中每年约有5.7万患者因该病死亡;美国每年约有10万人被诊断出患有黑色素瘤,约有7700人死于该疾病。
K药+化疗上市申请获FDA受理,有望年底上市
4月13日,默沙东宣布,FDA已接受Keytruda(帕博利珠单抗)联合化疗一线治疗HER2阴性晚期胃癌或胃食管交界处 (GEJ) 腺癌的补充生物制剂许可申请(sBLA),PDUFA日期定为2023年
美国FDA批准荣昌生物泰它西普开展治疗重症肌无力Ⅲ期临床试验并授予快速通道资格认定
值得一提的是,此次美国FDA批准泰它西普在美国开展Ⅲ期临床试验之际,还授予其快速通道资格认定。
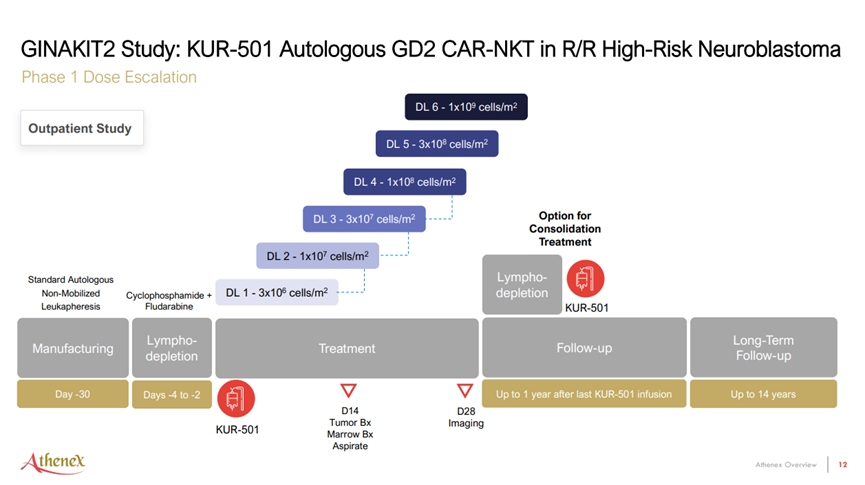
出现患者死亡,自体CAR-NKT疗法临床试验被FDA暂停
KUR-503靶向GPC3,是一款同种异体的TCR-NKT细胞疗法,用于治疗肝细胞癌(HCC)。Athenex表示将于2023年上半年启动IND。
诺维信和科汉森股东批准合并,共同打造全球领先生物解决方案企业
北京2023年4月4日 /美通社/ -- 诺维信和科汉森的拟议合并已经得到各自股东的批准,股东的大力支持使这两家生物解决方案公司向联合又迈出了一步。
FDA批准阿尔茨海默病新药,可减缓认知能力下降,但副作用引争议
去年,FDA批准了世界首个靶向Aβ的药物——aducanumab,但实际疗效缺乏证据,而且售价高昂(5.6万美元/年),以至于医生并不愿意给阿尔茨海默病患者开这种药物。
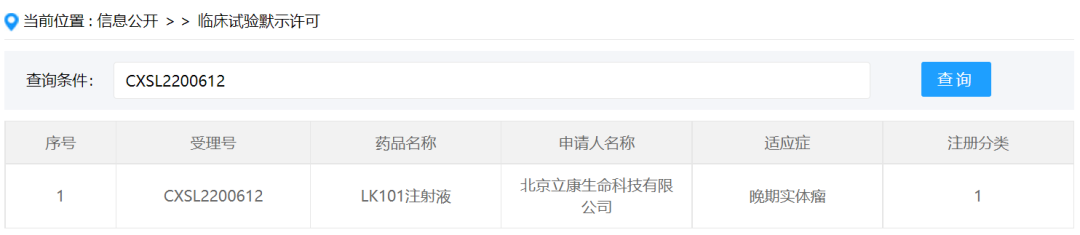
我国首款个性化肿瘤新生抗原疫苗获NMPA批准进入临床阶段
这是中国首个获得 NMPA 批准进入临床阶段的个性化肿瘤新生抗原疫苗,也是首个获批进入临床阶段的完全个性化的 mRNA 编辑产品。