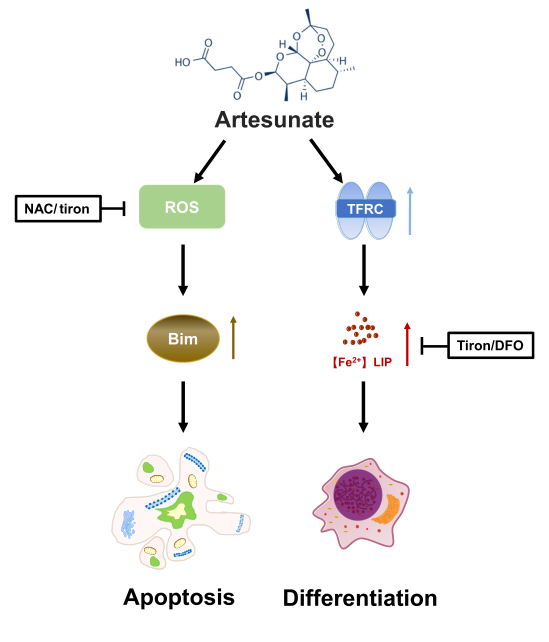
英国药理学:青蒿琥酯是一种新的抗疟疾临床药物,通过靶向ROS/Bim和TFRC/Fe2+途径显示出强大的抗AML活性
急性髓系白血病(AML)是最常见的成人急性白血病,主要由造血干细胞的恶性增殖和分化引起的一组不同的肿瘤疾病组成。基于这一特点,诱导凋亡或分化的治疗代表了靶向特定AML细胞的一种潜在的化疗方法。
2022-12-26
白血病(AML)新药!第二代FLT3抑制剂quizartinib获美国FDA优先审查:治疗新诊FLT3-ITD阳性AML!
AML是最常见的成人白血病类型之一,FLT3-ITD是最常见FLT3突变类型。3期试验中,与化疗相比,quizartinib方案将死亡风险降低22.4%,有潜力改变新诊FLT3-ITD阳性患者的治疗。
2022-10-25
白血病(AML)新药!美国FDA批准Tibsovo(艾伏尼布)一线治疗IDH1突变AML患者,已在国内上市!
基石药业拥有Tibsovo大中华区权利,该药于2022年2月获批上市,治疗复发或难治性IDH1突变AML患者。
2022-05-31
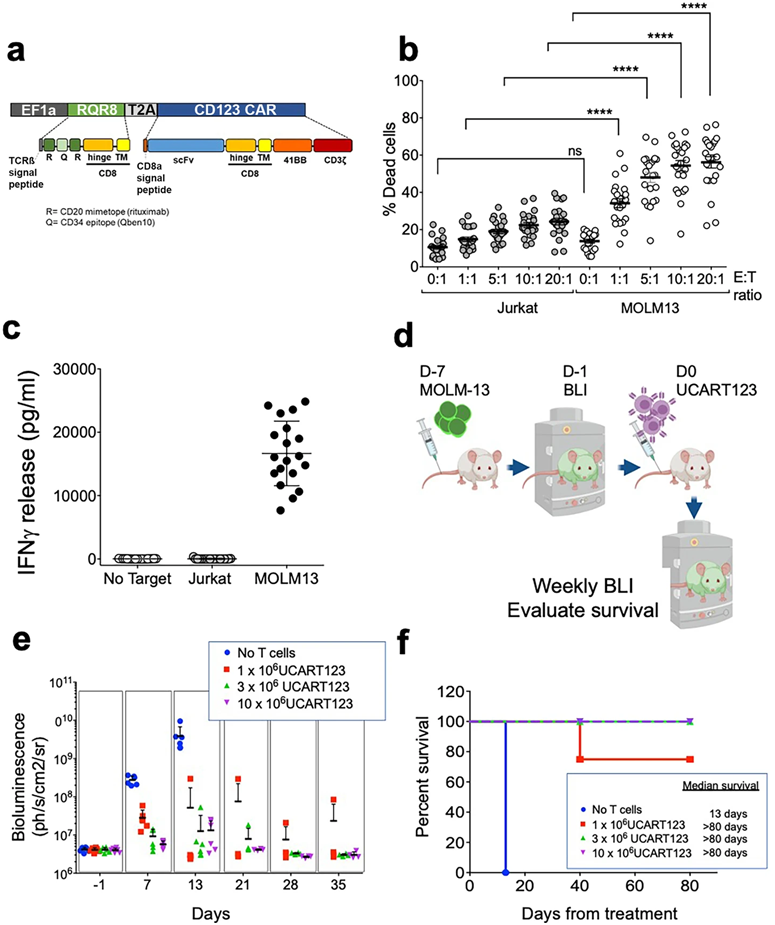
Nat Commun:靶向CD123的CAR-T细胞特异性杀死白血病干细胞,有望阻止AML白血病复发
这种新的细胞疗法目前正在进行1期临床试验,最终可能帮助AML患者保持无癌状态。
2022-06-10
基石药业拓舒沃®(艾伏尼布片)联合阿扎胞苷疗法获FDA批准用于一线治疗初治的IDH1突变AML患者
目前,拓舒沃®是全球首个获批联合阿扎胞苷用于一线治疗初治的IDH1突变AML患者的癌症代谢靶向疗法。
2022-06-02
《新英格兰医学杂志》重磅发表基石药业拓舒沃®(艾伏尼布片)联合阿扎胞苷治疗初治IDH1突变AML患者的全球AGILE III期研究数据
与阿扎胞苷联合安慰剂相比,拓舒沃®是首个证实了与阿扎胞苷联用可提高初治IDH1突变型急性髓系白血病(AML)患者无事件生存期(EFS)和总生存期(OS)的靶向疗法,为该类患者的一线治疗带来重大进展。
2022-04-22
FDA受理基石药业拓舒沃®(艾伏尼布片)一线治疗AML补充新药上市申请并授予优先审评
在欧洲,拓舒沃®两项适应症的上市许可申请已递交至欧洲药品管理局(EMA),分别为联合阿扎胞苷一线治疗不适合强化疗的IDH1突变型AML患者和既往接受过治疗的局部晚期或转移性IDH1突变型胆管癌患者,拓舒沃®成为全球首个在欧洲申报上市的IDH1靶向治疗药物。
2022-03-16
白血病(AML)新药!第一三共FLT3抑制剂Vanflyta+化疗一线治疗FLT3-ITD阳性AML显著延长生存期!
Vanflyta是一款高效和选择性FLT3抑制剂,已在日本获批上市。
2021-11-20
线粒体三羧酸循环靶向药物devimistat(CPI-613)治疗胰腺癌和白血病(AML)3期临床失败!
devimistat以线粒体三羧酸循环为靶点,影响癌细胞能量代谢,提高癌细胞对化疗的敏感性。
2021-10-30