PPARα激动剂WY14643的预治疗降低了脂多糖处理小鼠心脏中线粒体功能障碍引起的心肌病
脓毒症被定义为对感染的全身炎症反应综合征(SIRS),是重症监护病房最常见的死亡原因。败血症病死率上升的主要原因是感染性休克。败血症不断损害心血管系统,心功能不全是感染性休克的主要原因。
天津医科大学肿瘤研究所研究者揭示HSPA8作为ETV4的辅助激活剂是治疗肝癌的潜在靶点
肝细胞癌是癌症相关死亡的第二大常见原因。虽然大约50%的肝癌患者接受了系统治疗,但2年无进展生存率(PFS)和5年总生存率(OS)远不能令人满意,其详细机制尚不清楚。
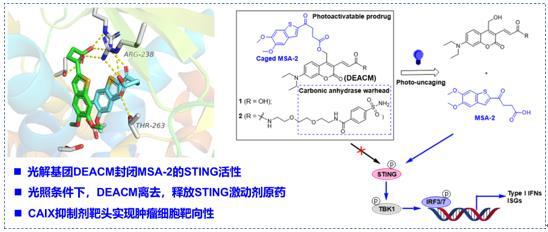
上海交大药学院合作发现肿瘤靶向的光控STING激动剂
靶向免疫检查点的抗肿瘤免疫疗法在临床上已获得巨大成功,但患者总体响应率较低。临床研究表明,免疫检查点抗体治疗的有效性取决于肿瘤预先存在的抗肿瘤T细胞反应。其中,先天免疫核酸感受通路中干扰素基因刺激蛋白
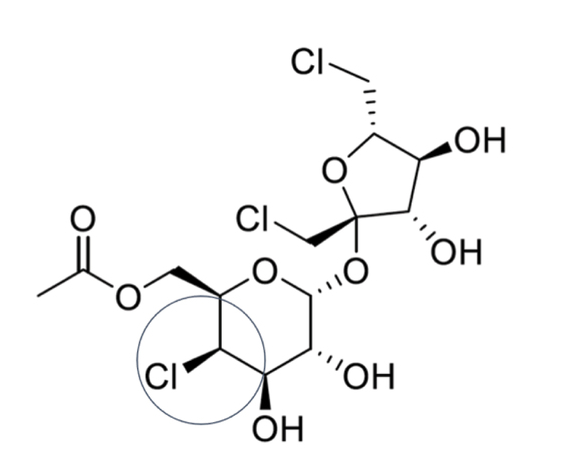
JTEHPB:常见甜味剂中的化学物质或具有遗传毒性 会损伤机体细胞的DNA
来自北卡罗来纳州立大学等机构的科学家们通过研究发现,当机体在消化一种广泛使用的甜味剂时所形成的一种化合物或许具有一定的“遗传毒性”(genotoxic),也就意味着其会破坏机体的DNA。
Cancer Cell:揭开CD11b激动剂发挥抗肿瘤免疫反应的机制
使用1期临床研究的人体组织,研究团队证明了GB1275(口服小分子CD11b激动剂)治疗可以激活人类肿瘤TAM中的STING和STAT1信号。此外,化疗或放疗联合GB1275,可以放大STING/IF
Nature:陈雷团队揭示人源UCP1识别小分子抑制剂和激活剂的机制
该研究通过冷冻电镜对不同状态下的UCP1的结构进行解析,从原子水平上观察到了DNP和ATP是如何与UCP1结合并引起构象变化的,为深入理解UCP1的工作机制提供了结构基础。
颜宁最新论文:Nav1.7拮抗剂的结构映射,为止痛药开发奠定基础
在这项研究中,研究团队将已知的配体结合位点映射到Nav通道的解析结构上,并提出了一个字母编码的命名系统来描述这些三维空间中的可成药位点。
告别染发剂?Nature重磅:科学家发现白发可逆变黑的“开关”!
随着生活压力的增大,“白发”已不仅仅是中老年人的标配,越来越多的青壮年年纪不大却已“早生华发”,武侠小说和影视剧中也常常有“一夜白头
超28万人数据显示,SGLT2抑制剂和GLP-1受体激动剂降低主要不良心血管事件效果更好
这项对比四个常用二线降糖药的研究发现,在降低MACE的风险上,新一代降糖药SGLT2抑制剂和GLP-1受体激动剂比经典降糖药DPP-4抑制剂和磺酰脲类药物更具优势,它们的心血管获益可作为指导2型糖尿病