研究揭示细胞分裂素快速激活基因表达的分子机制
细胞分裂素(cytokinin)是一种重要的植物激素,在植物的生长发育中扮演着多种角色,包括维持分生组织、促进维管组织分化、调控叶片衰老和促进再生等。
2024-01-17
陈椰林团队发现快速抗抑郁机制,为开发无致幻副作用的快速抗抑郁药物奠定基础
陈椰林研究员表示,相关药物研发有望明年进入临床试验阶段,让我们一起期待一款造福数亿人的抗抑郁症新药正式面世。
2023-09-19
NEJM:少数人在家庭快速新冠抗原检测中持续出现假阳性
1.7% 的参与者在进行快速抗原检测时至少出现过一次假阳性。在 191 名出现假阳性结果的参与者中,有 13 人(6.8%)的假阳性结果持续存在。
2024-03-28
仁济医院肝脏外科团队为肝硬化患者快速建立“生命通道”,一周制敌!
中国肝硬化患者约700万,肝硬化门静脉高压症是肝硬化的主要症状之一, 由于门静脉系统血流受阻或血流量增加,导致门静脉及其属支压力升高。
2024-01-24
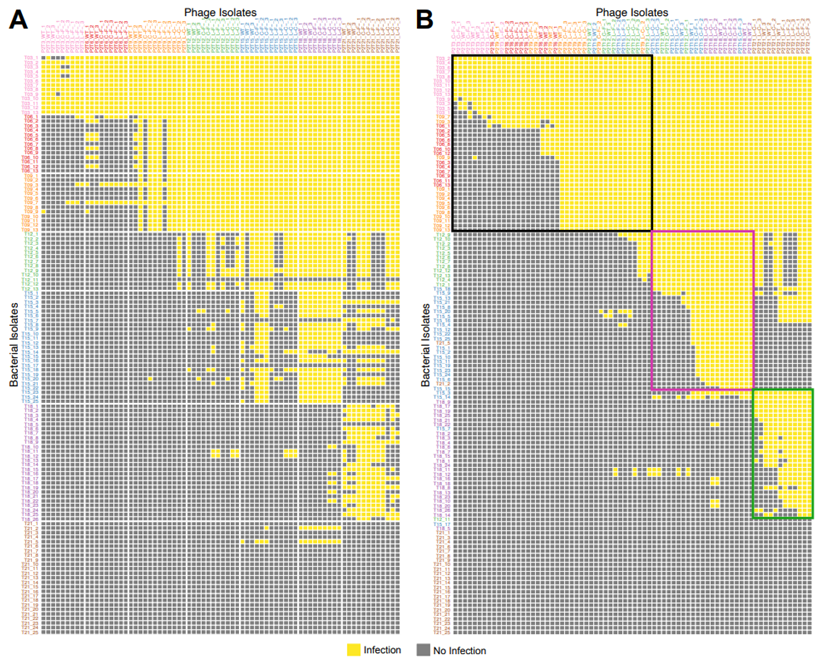
Science:快速的细菌-噬菌体共同进化促进高度复杂的生态网络的出现
按照查尔斯-达尔文在 19 世纪的构想,进化是一个缓慢而渐进的过程,在这一过程中,物种的适应能力是代代相传的。然而,如今生物学家可以看到进化变化是如何在更快的时间尺度上展开的。
2023-11-24