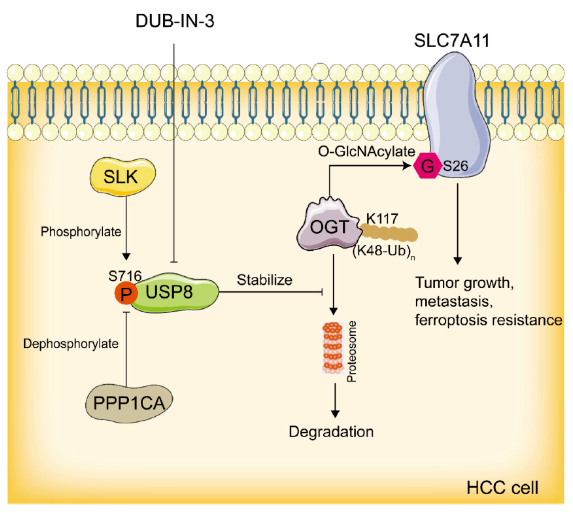
Adv Sci:陶永光/周乐杜/肖亮团队揭示靶向USP8促进肝癌铁死亡的新机制
该研究表明,使用小分子抑制剂靶向USP8可引起肝癌铁死亡,抑制肝癌的生长,为肿瘤新药研发提供了潜在有效的治疗靶点。
2023-11-21
Cell:吴军/谭韬/季维智/魏育蕾/于乐谦合作阐明胚胎发育早期细胞互作关系及机制
该研究成功在同一培养条件下获得小鼠与灵长类食蟹猴胚胎干细胞和胚外干细胞系,为剖析哺乳动物早期发育过程中不同谱系间细胞互作的分子机制开辟了新的途径。
2023-12-06
Cell | 于乐谦/郭靖涛/魏育蕾/王晓琰在世界上首次3D重构人类原肠期胚胎
该研究对一个完整的原肠胚CS8胚胎的62个切片进行了连续横切面,这使研究人员能够将所有切片的空间转录组从前侧面到后侧面结合起来,从而实现胚胎的完整3D重建。
2024-04-29
Cell:开发出一种类似乐高积木的基因编辑工具---ModPoKI,有望改善CAR-T细胞疗法
近年来,科学家们利用基因修饰技术将免疫细胞重编程为可以攻击癌症的疗法。但这类免疫疗法并非对所有患者或所有癌症类型都有效,而且筛选每一种可能改善这些经过重编程的免疫细胞的基因变化组合是一项艰巨而缓慢的任
2023-09-21
品质与技术的结晶:Venust皓昕与Invisalign隐适美联合举办正畸贴面嘉年华
1月6日至7日,Venust皓昕与Invisalign隐适美在上海外滩W酒店携手举办了一场盛大的“2024正畸贴面嘉年华”。
2024-01-11
北京因美未来溶瘤病毒YH01注射液I期临床顺利启动
2023年11月27日,北京因美未来生物医药有限公司(以下简称“因美未来”)的YH01注射液I期临床试验启动会在中国医学科学院肿瘤医院(以下简称“医科院肿瘤医院”)顺利召开。
2023-12-04
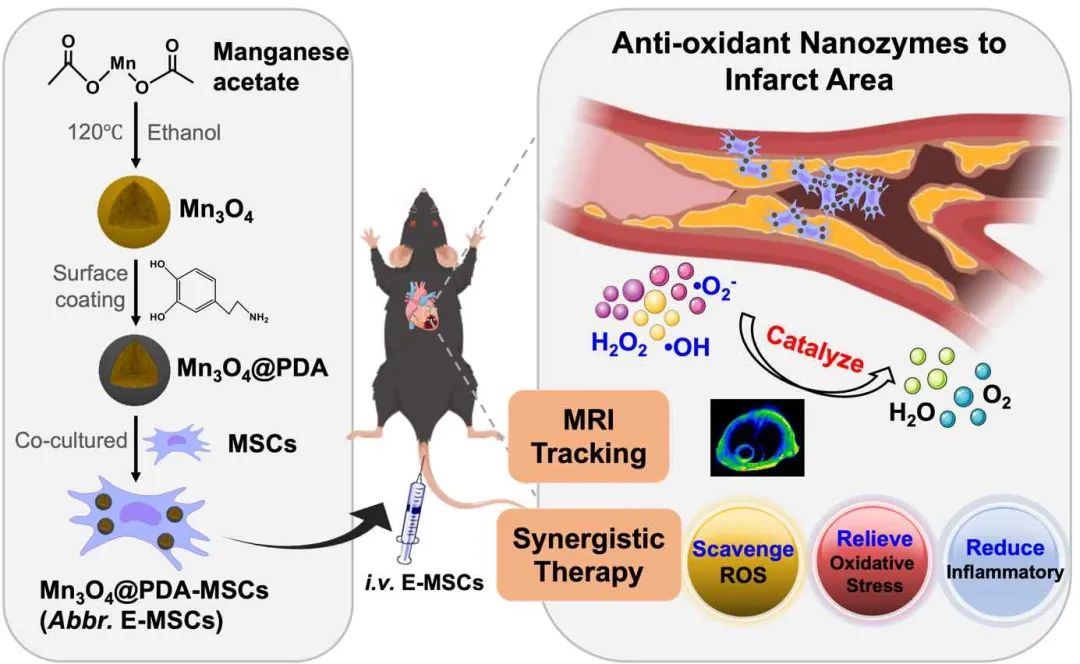
Adv Funct Mater | 刘中民/胡益辉/乐文俊/孙文等制备抗氧化纳米酶工程化干细胞,用于体内MRI示踪及协同治疗心梗
研究中详细研究了抗氧化纳米酶的MRI示踪和抗氧化、抗炎、迁移等性能,论述了工程化干细胞的抗炎和促血管生成作用,并应用于具有临床研究意义的心梗治疗研究。
2024-02-17
味之素(中国)与生物反应器工程郭美锦教授团队在沪签署合作协议
味之素近年来积极支持中国生物医药行业,为中国市场提供高性价比的CHO细胞培养基;并于2022年在上海成立了CSC-SH,以此为依托向中国生物医药客户提供培养基方面的技术支持和技术服务。
2024-01-31
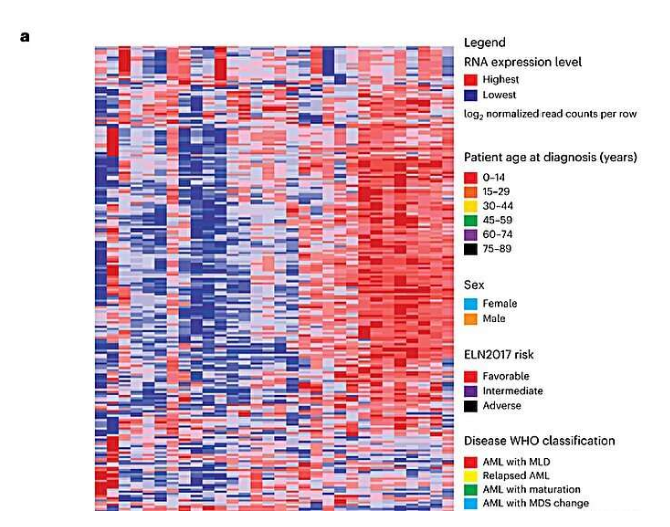
Nat Cancer:药物伊美司他有望治疗人类急性髓性白血病和其它类型癌症
来自澳大利亚QIMR Berghofer医学研究所等机构的科学家们通过研究有望开启一种靶向作用急性髓性白血病的全新疗法,或能为那些对当前疗法不再产生反应的患者带来一定的治疗希望。
2023-11-03