10年来系统性红斑狼疮(SLE)新药!阿斯利康Saphnelo在欧盟即将获批:I型干扰素受体抗体!
来源:本站原创 2021-12-22 23:40
Saphnelo已在美国获得批准,是首个I型干扰素(I型IFN)受体拮抗剂,也是过去10年来美国FDA唯一批准用于SLE的新疗法。
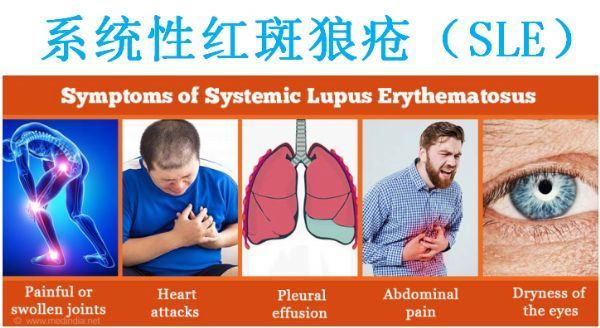
系统性红斑狼疮(SLE,图片来源:medindia.net)
2021年12月21日讯 /生物谷BIOON/ --阿斯利康(AstraZeneca)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布一份积极审查意见,建议批准Saphnelo(anifrolumab):作为一种附加疗法,用于治疗在接受标准治疗的中度至重度活动性自身抗体阳性系统性红斑狼疮(SLE)成人患者。现在,CHMP的意见将递交至欧盟委员会(EC)审查,后者通常会在2个月内做出最终审查决定。如果获批,Saphnelo将成为欧洲十多年来首个治疗SLE的新疗法。
Saphnelo是一种首创的(first-in-class)I型干扰素受体(IFNAR)抗体,I型IFN在狼疮的病理生理学中起着核心作用,I型IFN信号的增加与疾病活动性和严重性的增加相关。
2021年8月,Saphnelo获得美国FDA批准,用于治疗正在接受标准治疗的中度至重度SLE成人患者。值得一提的是,此次Saphnelo批准,标志着监管机构对I型干扰素(I型IFN)受体拮抗剂的首次批准,该药也是过去10年来美国FDA批准的首个用于SLE的新疗法。
SLE是最常见的狼疮类型,影响美国多达30万人。该病是一种复杂的自身免疫疾病,可影响任何器官,患者通常会经历疾病控制不足、长期器官损害、以及与健康相关的生活质量低下。2011年3月,葛兰素史克Benlysta(中文商品名:倍力腾,通用名:belimumab,贝利尤单抗)获得美国FDA批准,成为继1955年羟氯喹被批准之后,近60年来第一个治疗SLE的疗法。
Saphnelo的活性药物成分为anifrolumab,这是一种全人单克隆抗体,与I型干扰素受体亚基1结合,阻断包括IFNα、IFNβ和IFN-ω在内的所有I型干扰素的活性。I型干扰素是参与炎症通路的细胞因子。60%-80%的SLE成人患者具有升高的I型干扰素基因标志(gene signature),该基因标志已显示与疾病活动相关。临床数据显示,通过靶向I型干扰素受体,Saphnelo治疗显著降低了SLE患者疾病活动度。
美国FDA的批准、欧盟CHMP的积极审查意见,均基于Saphnelo临床开发项目的疗效和安全性数据,包括2项TULIP 3期试验和1项MUSE 2期试验。TULIP-2 试验结果于2020年1月发表于《新英格兰医学杂志》(New England Journal of Medicine),TULIP-1试验结果于2019年12月发表于《柳叶刀-风湿病学》(The Lancet Rheumatology),MUSE试验结果于2016年11月发表于《Arthritis & Rheumatology》。
在这些试验中,患者均接受标准治疗,与安慰剂组相比,Saphnelo治疗组有更高比例的患者经历了包括皮肤和关节在内的整个器官系统疾病活动的减少,并实现了口服皮质类固醇(OCS)使用的持续减少。在这3项临床试验中,接受Saphnelo治疗的患者中,更常发生的不良反应包括鼻咽炎、上呼吸道感染、支气管炎、输液相关反应、带状疱疹和咳嗽。
SLE的治疗目标是减少疾病活动,防止疾病本身或药物对器官的损害,特别是类固醇,以提高生活质量。Saphnelo将为狼疮社区提供一种有效的新治疗方法,在减少皮质类固醇使用的同时,显著改善整体疾病活动。这种开创性的药物,有潜力有意义地改善SLE患者的生活。
目前,Saphnelo皮下制剂治疗SLE的3期试验已经启动。阿斯利康还计划开展多项3期研究,评估Saphnelo治疗狼疮性肾炎、皮肤红斑狼疮和肌炎。
中国SLE现状:2款新药上市——Benlysta(倍力腾)和泰爱(泰它西普)
SLE是一种慢性自身免疫性疾病,免疫系统攻击机体健康组织,如果病情得不到控制,将会导致一系列症状,包括疼痛、皮疹、疲劳、关键肿胀、发烧、长期器官损伤,甚至过早死亡,该病同时也会对患者的身心健康造成巨大影响。据估计,全球有大约500万狼疮患者,传统的治疗方法包括类固醇和免疫抑制剂。
2011年,葛兰素史克Benlysta(倍力腾,通用名:belimumab,贝利尤单抗)获美国和欧盟批准用于治疗自身抗体阳性SLE成人患者,成为近60年来第一个治疗SLE的新药。2020年12月和2021年5月,Benlysta获美国和欧盟批准,用于治疗狼疮性肾炎(LN)。随着LN新适应症的获批,Benlysta成为了第一个也是唯一一个同时被批准用于治疗SLE和LN的生物制剂,
Saphnelo与Benlysta作用机理不同,后者是首个B淋巴细胞刺激因子(BLyS)特异性抑制剂,能阻断可溶性BLyS(一种B细胞生存因子)与B细胞上的BLyS受体的结合。Benlysta与B细胞不直接结合,但通过与BLyS结合,Benlysta可抑制B细胞(包括自身反应性B细胞)的生存、减少B细胞向制造免疫球蛋白的浆细胞的分化。Benlysta能够减少导致狼疮患者病情加重的异常B淋巴细胞的数量,这些异常的B淋巴细胞会导致免疫系统产生细胞错误攻击血管和自身其他健康组织,从而引起狼疮和其他免疫系统疾病。
在中国,Benlysta(商品名:倍力腾)于2019年7月获得NMPA的上市批准。作为全球首个获批应用于治疗SLE的生物制剂,倍力腾此次在中国被批准与常规治疗联合,适用于在常规治疗基础上仍具有高疾病活动的活动性、自身抗体阳性的SLE成年患者。贝利尤单抗是一种全人单抗,静脉给药,抑制B细胞增殖及分化,诱导自身反应性B细胞凋亡,从而减少血清中自身抗体,达到治疗SLE目的。
值得一提的是,2021年3月,荣昌生物制药宣布:全球首个用于治疗系统性红斑狼疮(SLE)的“双靶”一类生物新药——泰爱(通用名:泰它西普)获得国家药监局上市批准,也是60年来首个在我国获批上市的国产双靶点I类新药。
泰它西普的特别之处在于,它可以同时靶向BLyS和APRIL这2个关键细胞因子。研究发现,BLyS和APRIL是异常B细胞成熟分化的关键因子,且SLE患者体内的BLyS和APRIL水平,决定着疾病的严重程度。通过抑制BLyS和APRIL,能够完整抑制异常B细胞的信号通路,有效降低机体的自身免疫反应,达到治疗SLE的目的。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


