痴呆相关精神病(DRP)新药!选择性血清素反向激动剂Nuplazid 3期疗效显著:有效预防DRP相关幻觉和妄想!
来源:本站原创 2021-07-26 18:19
Nuplazid已被批准治疗与帕金森病精神病相关的幻觉和妄想,其独特药理学开创了一种新的药物类别:选择性5羟色胺反向激动剂(SSIA)。

痴呆相关精神病(图片来源:pdjnews.com)
2021年07月26日讯 /生物谷BIOON/ --Acadia制药公司致力于开发创新疗法治疗中枢神经系统(CNS)疾病。近日,该公司宣布,3期HARMONY研究(NCT03325556)的结果已发表于国际医学期刊《新英格兰医学杂志》(NEJM)。这是一项国际性、双盲、安慰剂对照、复发预防试验,旨在评估Nuplazid(pimavanserin)治疗与痴呆相关精神病(DRP)相关的幻觉和妄想。该研究包括痴呆的5个亚组患者:阿尔茨海默病(AD)、路易体痴呆(DLB)、额颞叶痴呆(FTD)、帕金森病痴呆(PDD)、血管性痴呆(VD)。研究共入组392例患者,平均年龄74.5岁、平均简易精神状态检查(MMSE)评分为16.7分。
Nuplazid的活性药物成分为pimavanserin,这是一种选择性血清素受体反向激动剂(SSIA),能够选择性地靶向5-HT2A受体,通过降低5-HT2A受体的基础活性,从而减少中枢神经系统的兴奋程度,降低出现幻觉或妄想的风险。
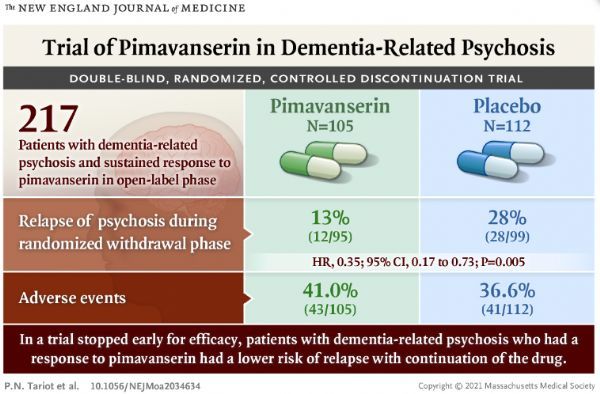
HARMONY研究因疗效显著提前终止,结果显示:在12周开放标签稳定期接受Nuplazid(34mg,每日一次)治疗获得持久反应的DRP患者,进入26周双盲随机撤药期后,与改用安慰剂相比,继续Nuplazid治疗将精神病复发的风险显著降低近3倍(2.8倍)。该研究中,Nuplazid耐受性良好,双盲期不良事件发生率与安慰剂相似。研究结果详见:Trial of Pimavanserin in Dementia-Related Psychosis。
该研究的首席研究员、班纳阿尔茨海默病研究所Pierre N. Tariot博士表示:“HARMONY研究的复发预防设计正好反映了我们在临床实践中所做的工作。这项具有里程碑意义的试验表明,当患者对Nuplazid有反应,然后继续治疗时,他们出现幻觉和妄想复发的可能性比那些停止Nuplazid治疗的患者几乎低3倍(2.8倍)。这是一个实质性的发现,也是我们领域关键公共卫生需求的一个重大进展。目前还没有美国FDA批准的DRP治疗方法,目前使用的大多数非处方抗精神病药物的疗效不明确,可能会加速认知能力的下降。”
Acadia首席执行官Steve Davis表示:“HARMONY研究的结果显示了3个重要的结果。首先,在12周的开放标签期内,Nuplazid治疗显示精神病症状持续减轻。其次,在26周的双盲期内,与安慰剂组相比,Nuplazid组患者精神病复发的风险降低了近3倍。第三,Nuplazid对老年DRP患者的耐受性良好。我们很高兴《新英格兰医学杂志》选择发表这项研究的重要成果。”
HARMONY研究结果(图片来源:NEJM)
HARMONY研究包括一个为期12周的开放标签稳定期,在此期间,DRP患者开始接受Nuplazid(34mg,每日一次)治疗。在开放标签期,符合资格的患者(n=351)中,大多数(61.8%,n=271)在第8周和第12周达到预先规定的持久治疗反应标准,并进入为期26周的双盲随机撤药期。进入双盲随机撤药期的患者(n=271),按1:1的比例随机分配,继续服用Nuplazid(34mg,每日一次,n=105)或改用安慰剂(112),治疗随访26周或直至精神病复发。
根据试验独立数据安全监测委员会的建议,由于在预先计划的中期分析中显示出积极疗效,HARMONY研究已提前停止。该研究达到了主要终点:在双盲随机撤药期,与改用安慰剂相比,继续Nuplazid治疗将精神病复发风险显著降低了2.8倍(风险比[HR]=0.35,双侧p=0.005;单侧p=0.0023)。具体而言,在双盲随机撤药期,安慰剂组患者中有28%(28/99)发生精神病复发,而Nuplazid组患者中仅有13%(12/95)发生精神病复发。该研究还达到了次要终点:与安慰剂相比,Nuplazid将任何原因导致中止试验的患者比例显著降低了2.2倍(HR=0.45,双侧p=0.005;单侧p=0.0024)。在一项预先指定的分析中,Nuplazid与简易精神状态检查(MMSE)测量的认知能力下降或锥体外系症状评定量表A(ESRS-A)测量的运动症状的发生或恶化无关。
该研究中,在为期9个月(12周开放标签期+26周双盲随机撤药期)的研究期间,Nuplazid的耐受性良好。在双盲期,观察到类似的低不良事件发生率,Nuplazid组105例患者中有43例(41.0%)、安慰剂组有41例(36.6%)发生不良事件。双盲期因不良事件导致的停药率较低,Nuplazid组为2.9%、安慰剂组为3.6%。严重不良事件发生率也很低,Nuplazid组为4.8%、安慰剂组为3.6%。Nuplazid治疗的患者中,发生2例死亡,1例发生在开放标签期,1例发生在双盲期。经研究调查员确认,2例死亡均与研究药物无关。
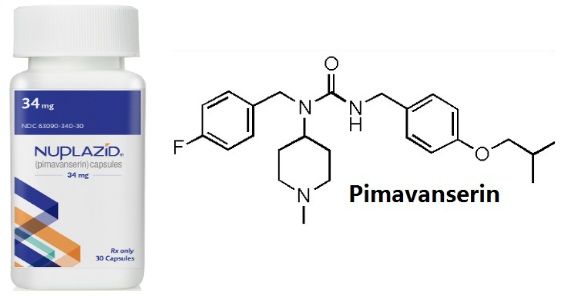
pimavanserin化学结构式(图片来源:chemicalbook.com)
Nuplazid的活性药物成分为pimavanserin,这是一种选择性5-羟色胺反向激动剂和拮抗剂,优先靶向5-HT2A受体。这些受体被认为在神经精神疾病中起重要作用。在体外,pimavanserin对多巴胺(包括D2)、组胺、毒蕈碱或肾上腺素能受体没有明显的结合亲和力。
Nuplazid于2016年5月获美国FDA批准上市,用于治疗与帕金森病(PD)精神病相关的幻觉和妄想。之前,FDA已于2014年授予Nuplazid突破性药物资格。Nuplazid是第一个获FDA批准治疗与帕金森病精神病相关的幻觉和妄想的药物。Nuplazid的批准上市,标志着帕金森病精神病临床治疗的一个重大里程碑。
Nuplazid独特的药理学开创了一种新的药物类别——选择性5羟色胺反向激动剂(SSIA),该药不仅优先靶向5-HT2A受体,同时可避免多数精神分裂症药物所具有的多巴胺受体及其他受体激活副作用。常规的帕金森病疗法所包含的药物刺激多巴胺来治疗患者的运动症状,如震颤、肌肉僵硬和行走困难。Nuplazid具有一种新颖的选择性作用机制,以全新的作用方式治疗幻觉和妄想,该药不具有多巴胺受体活性,并不干扰患者的多巴胺能疗法,因此不会影响帕金森患者的运动功能。
今年4月,Nuplazid治疗与痴呆症相关精神病(DRP)相关的幻觉和妄想的新适应症申请(sNDA)遭到了美国FDA拒绝批准。FDA向该公司发布了一封完整回应函(CRL),称已完成sNDA审查,并确定sNDA不能以目前的形式获得批准。CRL中指出,某些痴呆亚型缺乏统计学意义。同时,某些不太常见的痴呆亚型的患者数量不足,缺乏有效的证据支持批准。
Nuplazid尚未被批准治疗与DRP相关的幻觉和妄想。当前,Acadia正在其他神经精神疾病中开发pimavanserin。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->