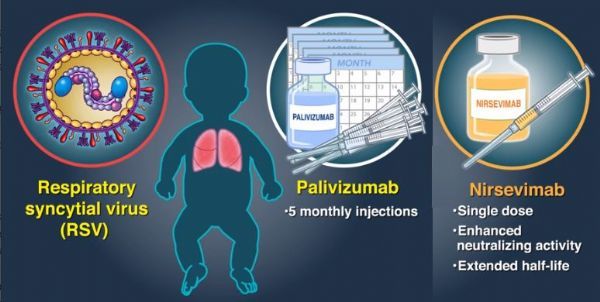
呼吸道合胞病毒(RSV)创新药!阿斯利康/赛诺菲nirsevimab 3期成功:显著减少健康婴儿下呼吸道感染(LRTI)!
来源:本站原创 2021-04-26 23:02
nirsevimab已获全球三大监管机构授予突破性药物资格,包括中国。该药是一种被动免疫疗法,可直接为婴儿提供即时保护作用。

2021年04月26日讯 /生物谷BIOON/ --阿斯利康(AstraZeneca)近日宣布,评估呼吸道合胞病毒(RSV)单抗药物nirsevimab的3期MELODY试验达到了主要终点:在健康晚期早产儿和足月儿(≥35周)的第一个RSV季节,与安慰剂相比,nirsevimab单剂量肌肉注射使RSV引起的下呼吸道感染(LRTI)的发生率在统计学上显著降低。对nirsevimab安全性的初步分析与先前的试验数据一致。nirsevimab组和安慰剂组的安全性结果没有临床意义的差异。
值得一提的是,这是首次在一项3期试验中对于一般婴儿群体针对RSV显示出保护作用的潜在被动免疫。RSV是一种非常常见的传染性病原体,可引起LRTI(包括毛细支气管炎和肺炎)的季节性流行。在全球范围内,RSV是导致婴幼儿住院的首要原因,大多数住院都发生在足月出生的健康婴儿身上。很显然,所有婴儿都需要获得针对RSV的保护,nirsevimab有潜力成为常规预防项目的重要补充。
nirsevimab是一种具有延长半衰期(平均59.3天)的RSV单克隆抗体,采用了阿斯利康的专有技术,由阿斯利康和赛诺菲共同开发,作为一种被动免疫疗法,有潜力直接为婴儿提供免疫力、针对RSV提供即时保护。
nirsevimab是首个潜在的婴儿被动免疫疗法,已被证实单剂量肌肉注射能够在整个RSV流行季提供持续的保护作用。截至目前,nirsevimab已获全球三大监管机构授予突破性资格,包括:中国国家药品监督管理局(NMPA)药品审评中心(CDE)授予的突破性疗法认定、美国FDA授予的突破性疗法认定、欧洲药品管理局(EMA)授予的优先药物资格(PRIME)。
RSV-呼吸道合包病毒
MELODY试验的主要研究员、美国西北大学范伯格医学院儿科副教授William Muller医学博士表示:“尽管RSV是婴儿出生后第一年引起肺炎和毛细支气管炎的首要原因,但目前还没有针对所有婴儿的常规预防措施。这些令人兴奋的试验数据表明,nirsevimab不仅可以在整个RSV季节为广大婴儿提供保护,而且可以通过单剂量达到这一目的,从而改变预防格局。”
阿斯利康生物制药研发部执行副总裁Mene Pangalos表示:“这些突破性的结果标志着我们在为所有婴儿提供RSV防护方面取得了重大的科学进展。几乎所有婴儿在2岁之前都会感染这种病毒,导致全球每年有近3000万急性下呼吸道感染。nirsevimab作为第一种针对一般婴儿群体的RSV被动免疫疗法,有潜力为公众健康带来重大益处,这些数据使我们距离向全世界婴儿提供nirsevimab又近了一步。”
赛诺菲巴斯德全球研发主管Jean-François Toussaint表示:“RSV是导致所有婴儿住院的首要原因。事实上,大多数住院都发生在足月出生的健康婴儿身上。很明显,所有的婴儿都需要针对这种病毒的保护,我们希望nirsevimab能成为常规免疫计划的重要补充。”

已上市的预防婴幼儿RSV的产品Synagis
MELODY试验中主要疗效终点的评估比预期更早进行。控制COVID-19的全球公共卫生措施减少了包括RSV在内的所有呼吸道病毒的传播。在COVID-19大流行之前已经积累了足够的病例来评估nirsevimab与安慰剂预防RSV-LRTI的能力。该试验正在进行中,以收集更多的安全数据。MELODY试验的结果将在即将召开的医学会议上公布。
nirsevimab也正在MEDLEY 2/3期试验中进行评估,在即将进入第一个和第二个RSV流行季的早产儿和患有慢性肺病(CLD)和先天性心脏病(CHD)的儿童中,比较nirsevimab与Synagis(palivizumab)的安全性和耐受性。MEDLEY试验也预计会比预期更早公布数据,首批数据预计2021年下半年公布。MELODY、MEDLEY和一项IIb期试验(NCT02878330)的数据,将构成阿斯利康计划于2022年提交nirsevimab上市申请的基础。
nirsevimab相对于市售药物Synagis的优势
呼吸道合胞病毒(RSV)是一种感染呼吸道的常见传染性病毒,是婴幼儿急性下呼吸道感染(LRTI,主要是毛细支气管炎和肺炎)的首要致病原。有资料显示,2岁前几乎所有的婴幼儿都罹患过至少一次RSV感染,6个月以下婴儿是主要患病人群。RSV具有高度传染性,可在人与人之间通过飞沫或接触传播。RSV流行季节为每年秋季至次年春季,典型的RSV流行季为5个月。
目前的抗RSV抗体Synagis(palivizumab)仅限于高危婴儿,只能提供一个月的保护,需要注射5次才能覆盖一个典型的RSV流行季。
nirsevimab是一种具有延长半衰期的RSV单抗,被开发作为一种被动免疫疗法,预防RSV引起的LRTI。该产品的开发目的是用于比当前护理标准更广泛的婴儿群体,包括:正经历第一个RSV流行季的婴儿群体、将进入第一个和第二个RSV流行季的先天性心脏病或慢性肺病婴儿群体。
nirsevimab是一种被动免疫疗法,即直接向婴儿提供抗体以帮助预防RSV;被动免疫不同于主动免疫,后者是通过疫苗激活人体的免疫系统来预防或抗击RSV感染。被动免疫可以提供即时的保护,而主动免疫则需要数周才能产生保护作用。
2017年3月,阿斯利康和赛诺菲达成了开发和商业化nirsevimab的协议。根据协议条款,阿斯利康领导所有的开发活动和初步的监管批准、并保留生产活动,赛诺菲将领导商业化活动。(生物谷Bioon.com)
原文出处:Nirsevimab MELODY Phase III trial met primary endpoint of reducing RSV lower respiratory tract infections in healthy infants
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->