中国胃肠道间质瘤(GIST)新药!再鼎医药瑞普替尼(ripretinib)上市申请获国家药监局受理!
来源:本站原创 2020-07-21 19:39
ripretinib一种KIT/PDGFRα激酶抑制剂,已获美国批准,是首个四线GIST药物。

2020年07月21日讯 /生物谷BIOON/ --再鼎医药(Zai Lab)与合作伙伴Deciphera制药公司近日联合宣布,国家药品监督管理局(NMPA)已受理瑞普替尼(ripretinib)的新药上市申请,用于治疗已接受过包括伊马替尼在内的3种或更多种激酶抑制剂治疗的晚期胃肠道间质瘤(GIST)成人患者。
瑞普替尼(ripretinib)是一种酪氨酸激酶开关控制抑制剂,通过使用独特的双重作用机制来调节激酶开关和激活环,从而广泛抑制KIT和PDGFRα突变激酶。ripretinib抑制参与GIST的外显子9、11、13、14、17和18中的起始和继发性KIT突变,以及参与SM的主要外显子17 D816V突变。ripretinib还抑制GIST子集有关的外显子12、14和18中的主要PDGFRα突变,包括外显子18 D842V突变。该药开发用于治疗KIT和/或PDGFRα驱动的癌症,包括GIST、全身性肥大细胞增多症(SM)及其它癌症。

最近,ripretinib在美国、加拿大、澳大利亚获批上市,英文商品名为Qinlock,用于四线治疗晚期GIST成人患者,具体为:先前接受过3种或3种以上激酶抑制剂治疗的成人患者,包括:伊马替尼[imatinib]、舒尼替尼[sunitinib]、瑞戈非尼[regorafenib])。
2019年6月,再鼎医药与Deciphera签署协议,获得了ripretinib在大中华区(中国大陆、香港、澳门和台湾)开发和推广的独家许可。在中国,每年有超过3万名新诊断的GIST患者。GIST患者,特别是那些对过往治疗方案已经发生耐药的患者,仍存在着显著的未满足需求。基于近期美国FDA的批准以及INVICTUS研究(NCT03353753)卓越的临床数据,瑞普替尼将有望改变国内GIST患者的治疗现状。
INVICTUS是一项随机(2:1)、双盲、安慰剂对照、国际多中心III期研究,共入组了129例既往已接受多种疗法(至少包括伊马替尼、舒尼替尼、瑞戈非尼)的晚期GIST患者,评估了Qinlock相对于安慰剂的疗效和安全性。
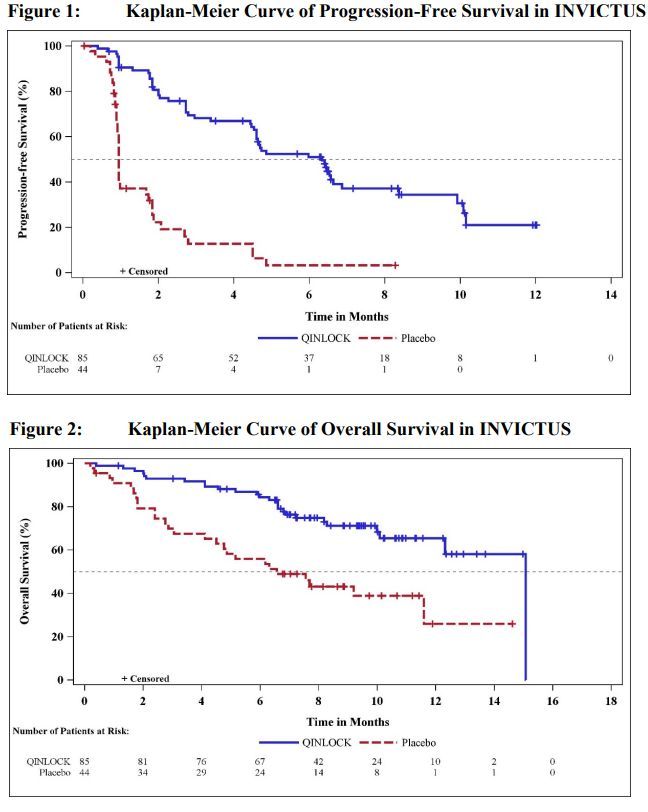
结果显示,研究达到了主要终点:与安慰剂组相比,Qinlock治疗组无进展生存期显著延长(中位PFS:6.3个月 vs 1.0个月)、疾病进展或死亡风险显著降低85%(HR=0.15,p<0.0001)。次要终点总生存期(OS)方面,Qinlock治疗组与安慰剂组相比显著延长(中位OS:15.1个月 vs 6.6个月)、死亡风险降低64%(HR=0.36,名义p=0.0004);值得注意的是,安慰剂组的OS数据包括接受安慰剂治疗病情进展后转向Qinlock治疗的患者数据。另一个次要终点总缓解率(ORR)方面,Qinlock治疗组与安慰剂组相比大幅提高(ORR:9.4% vs 0%,p=0.0504)。
安全性方面,最常见的不良反应(>20%)为脱发、疲劳、恶心、腹痛、便秘、肌痛、腹泻、食欲减退、掌跖红细胞感觉异常综合征(PPES) 、呕吐。在接受Qinlock治疗的患者中,导致永久停药的不良反应发生在8%的患者中,因不良反应导致的剂量中断发生在24%的患者中,因不良反应导致的剂量减少发生在7%接受Qinlock治疗的患者中。(生物谷Bioon.com)
原文出处:再鼎医药
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


