研究揭示淋巴结靶向纳米疫苗免疫新机制
来源:生物物理所 2020-03-07 22:44
3月2日,中国科学院生物物理研究所感染与免疫重点实验室朱明昭课题组在《自然-纳米技术》(Nature Nanotechnology)上发表Article论文:Dual-targeting nanoparticle vaccine elicits a therapeutic antibody response against chronic hepatitis
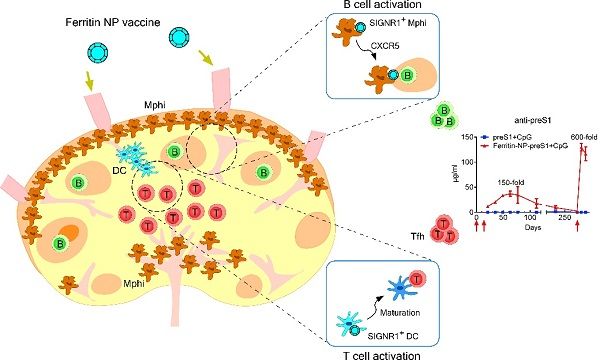
3月2日,中国科学院生物物理研究所感染与免疫重点实验室朱明昭课题组在《自然-纳米技术》(Nature Nanotechnology)上发表Article论文:Dual-targeting nanoparticle vaccine elicits a therapeutic antibody response against chronic hepatitis B。该研究设计了基于铁蛋白纳米颗粒的乙型肝炎病毒(HBV)preS1纳米疫苗,在小鼠模型中,诱导产生了高水平、高亲和力、持久的抗体应答和免疫记忆,不但具有出色的预防作用,而且在治疗模型中获得功能性治愈和HBsAg血清学转换,并显着降低HBVcccDNA。该研究还进一步揭示了铁蛋白纳米颗粒抗原被淋巴结SIGNR1+抗原呈递细胞主动靶向识别、转运、诱导Tfh和B细胞活化应答的免疫学新机制。
HBV感染是全球性重大公共卫生健康问题之一。全球目前乙肝病毒慢性感染者约2.6亿人,每年接近100万人死于慢性乙肝导致的肝功能衰竭、肝硬化和肝细胞癌。尽管预防性乙肝疫苗在临床应用中取得了显着效果,迄今为止,尚无有效的治疗性乙肝疫苗上市。这其中最具挑战的重大问题是如何突破慢性乙肝感染患者体内长期建立起来的免疫耐受,诱导有效、持续的免疫应答,获得功能性治愈,甚至完全清除cccDNA。HBV preS1作为治疗性乙肝疫苗的新功能靶点,最近获得了概念性验证。但是,preS1是弱免疫原性的功能表位,如何充分合理调动机体免疫系统,诱导针对弱免疫原性表位的高效抗体应答,仍然是目前的关键问题,也是疫苗免疫学领域的普遍问题。
病毒样颗粒(以及近些年受到日益关注的铁蛋白)等纳米颗粒载体对于提高抗原的免疫原性,提高抗体应答的效果早就得到广泛重视和认可。但是其免疫学机制并不十分清楚,长期以来停留在淋巴结靶向递送、理想抗原展示密度等传统认知,以及铁蛋白颗粒载体的三聚体构象抗原展示等方面,限制了这一类疫苗改进优化的思路。
在该研究中,研究人员利用课题组前期建立的铁蛋白纳米点击疫苗技术,设计了HBV preS1纳米疫苗Ferritin NP-preS1。在小鼠模型中,两次免疫后诱导了比对照组高150倍的抗体应答,而且持续时间长达至少8个月,且再次免疫时的抗体应答水平比对照组高约600倍。在AAV-HBV1.3感染小鼠模型中,该疫苗不仅具有出色的预防保护作用,而且具有出色的治疗效果,显着降低了外周血HBV DNA、HBsAg水平,降低了肝脏中的HBcAg和cccDNA水平,部分小鼠获得功能性治愈和HBsAg血清学转换(外周血HBsAg和DNA转阴,抗-HBs转阳)。
进一步的免疫学机制研究发现,铁蛋白纳米颗粒同时主动靶向小鼠淋巴结中常驻的SIGNR1+巨噬细胞和SIGNR1+树突状细胞,分别促进了B细胞和Tfh细胞的活化应答,协同诱导抗体产生。这种SIGNR1+细胞靶向特性也利用人淋巴结的临床样品获得验证(人DC-SIGN是小鼠SIGNR1的同源分子)。有趣的是,研究人员还发现,定位于淋巴窦的SIGNR1+巨噬细胞可以携带铁蛋白纳米抗原,向淋巴滤泡(B细胞区)迁移,传递抗原给B细胞,促进B细胞活化;CXCR5基因敲除的巨噬细胞,不能向淋巴滤泡迁移,无法有效活化B细胞。这与人们长期以来推测的淋巴窦巨噬细胞原地不动通过胞吞/胞吐或细胞膜流动传递纳米颗粒抗原给B细胞的模式完全不同。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


