肌肉浸润性膀胱癌(MIBC)!百时美Opdivo联合化疗用于新辅助治疗,病理完全缓解率(pCR)达49%!
来源:本站原创 2020-02-18 14:54
2020年02月18日讯 /生物谷BIOON/ --近日,在旧金山举行的2020年美国临床肿瘤学会泌尿生殖系统癌症研讨会(ASCO-GU 2020)上公布的一项膀胱癌临床试验BLASST-1的结果显示,百时美施贵宝抗PD-1疗法Opdivo(欧狄沃,通用名:nivolumab,纳武利尤单抗)联合吉西他滨(gemcitabine)和顺铂(cisplatin)新

2020年02月18日讯 /生物谷BIOON/ --近日,在旧金山举行的2020年美国临床肿瘤学会泌尿生殖系统癌症研讨会(ASCO-GU 2020)上公布的一项膀胱癌临床试验BLASST-1的结果显示,百时美施贵宝抗PD-1疗法Opdivo(欧狄沃,通用名:nivolumab,纳武利尤单抗)联合吉西他滨(gemcitabine)和顺铂(cisplatin)新辅助治疗肌肉浸润性膀胱癌(MIBC)患者获得了强劲疗效:病理学非肌肉浸润率(PaR)为66%、病理学完全缓解率(pCR)为49%。研究中,这种组合疗法是安全的,没有增加的毒性或死亡,并且没有导致膀胱切除延迟或导致意外的手术并发症。这些结果非常令人鼓舞,长期随访将进一步证实其安全性。
研究报告者、克利夫兰诊所泌尿生殖肿瘤副教授Shilpa Gupta表示:“以顺铂为基础的新辅助化疗与30%左右的pCR率相关。新辅助化疗的生存优势主要发生在实现肿瘤病理分级降低的患者中。然而,相当多的患者仍然复发,导致早期死亡。因此,该领域存在一个显著未满足的医疗需求,即通过新的联合疗法以及生物标记物驱动的方法来更好地选择患者,提高病理学缓解率。”
Shilpa Gupta表示,先前对肌肉浸润性膀胱癌进行的单药新辅助免疫治疗的研究已经显示出益处,即PURE-01和ABACUS试验。默沙东抗PD-1疗法Keytruda(帕博利珠单抗)联合吉西他滨/顺铂这一新辅助免疫化学方案在I/IIb期试验中也显示出活性。Opdivo已经被批准用于治疗接受铂类化疗后病情进展的转移性尿路上皮癌患者。
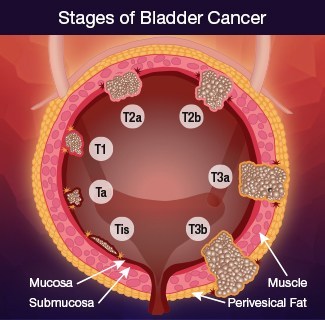
BLASST-1研究的患者为cT2~T4aN≤1、以尿路上皮癌为主的M0疾病,并被确定为根治性膀胱切除术的候选者,所有患者都被认为符合顺铂治疗的条件。肌酐清除率的临界值≥50mL/min。
诊断为肌肉浸润性疾病后,患者接受4个周期的吉西他滨/顺铂治疗。顺铂在每个疗程(21天/疗程)的第1天70mg/m2。顺铂的分割剂量由研究者决定。吉西他滨在每个疗程(21天/疗程)的第1天、第8天给药1000mg/m2,共4个疗程。Opdivo在每个疗程的第8天以固定剂量360mg/m2每3周一次给药。患者在完成系统治疗后的6~8周进行膀胱切除术。在研究治疗前进行CT和氟脱氧葡萄糖(FDG)-PET扫描,采集组织和血液进行相关分析。治疗结束时重复CT/FDG-PET检查,并收集组织。主要目标是病理学反应,定义为手术时病理学非肌肉浸润率。
该研究在3个临床中心入组了41例患者(63%男性,37%女性),中位年龄为66岁(45-82岁)。临床分期T2N0占90%、T3N0占7%、T2-4N1占3%。2例(4.8%)接受过卡介苗(BCG)治疗。38例患者完成全部4个疗程,2例完成2个疗程,1例仅完成1个疗程。任何接受至少1个疗程的患者都是可评价的。40例患者接受了膀胱切除术;1名患者在1个疗程后退出同意书,失去随访,但纳入意向治疗分析。所有患者在完成治疗后8周内均行膀胱切除术。
肿瘤分期降期(downstage)至非肌肉浸润状态的27例患者中,14例(51.8%)降至pT0、2例(7.4%)降至pT1、5例(18.5%)降至pTa、6例(22.2%)降至pTis。pCR率为49%(41例中的20例),定义为肿瘤分期降期至pT0或pTis。
39个肿瘤中有15个(39%)的PD-L1检测呈阳性。PD-L1阳性状态与缓解之间没有相关性。15例PD-L1阳性肿瘤患者中有10例(67%)出现肿瘤缩小,而24例PD-L1阴性肿瘤患者中有17例(71%)出现肿瘤缩小。

通过分子亚型的缓解分析显示,1例claudin-low肿瘤(以高免疫浸润和基础标记物表达为特征)患者对治疗有完全缓解(pT0N0);另1例管腔浸润亚型(以高基质浸润和中等管腔标记物表达为特征)的患者,是一个无应答者(pT3N2)。
对50个癌症标志(cancer hallmark)进行基因标记评分。在这例claudin-low肿瘤患者中,显示出“高免疫标志物活性”,immune 190、γ-干扰素、α-干扰素和炎症标志物呈高表达。相反,在这例管腔浸润性亚型疾病患者中,显示强血管生成活性、低增殖。
研究中,大多数与治疗相关的不良事件(AE)都归因于化疗。大多数血液学毒性与所见的吉西他滨和顺铂的是一致的。其中大部分是1/2级贫血、中性粒细胞减少症和血小板减少症。贫血患者总数为10例(24%),中性粒细胞减少20例(48%),血小板减少13例(31%)。1/2级疲劳60%,1/2级恶心70%。24%的患者的丙氨酸转氨酶和天冬氨酸转氨酶水平升高。急性肾损伤6例(14%),除1例外均为1/2级。免疫相关不良事件1例为皮疹,1例为甲状腺功能减退,2例为淋巴结发炎(均为完全缓解者,活检为良性),1例为格林-巴利综合征。
Shilpa Gupta表示:“正在进行的生物标记物分析将有助于确定肌肉浸润性膀胱癌对化学免疫治疗的反应和抵抗的预测因子。正在进行III期ENERGIZE试验(NCT03661320),将确认这些结果。”(生物谷Bioon.com)
原文出处:ASCO-GU 2020: Abstract 439
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


