中国结核病新药!TB联盟与复星医药达成合作,在中国商业化高度耐药结核新疗法pretomanid!
来源:本站原创 2020-01-21 14:50
2020年01月21日讯 /生物谷BIOON/ --近日,非盈利药物研发组织TB Alliance(结核病联盟)授予上海复星医药(集团)股份有限公司(以下简称“复星医药”)全资子公司沈阳红旗制药有限公司(以下简称“红旗制药”)在中华人民共和国境内销售结核病药物pretomanid的许可。该药与贝达喹啉(bedaquilin)和利奈唑胺 (linezolid)

2020年01月21日讯 /生物谷BIOON/ --近日,非盈利药物研发组织TB Alliance(结核病联盟)授予上海复星医药(集团)股份有限公司(以下简称“复星医药”)全资子公司沈阳红旗制药有限公司(以下简称“红旗制药”)在中华人民共和国境内销售结核病药物pretomanid的许可。该药与贝达喹啉(bedaquilin)和利奈唑胺 (linezolid)组成的三药“BPaL”方案,针对广泛耐药结核病(XDR-TB)或耐多药结核病(MRD-TB)患者,统称为“高度耐药结核病”患者。
TB Alliance主席兼首席执行官梅尔斯皮格尔曼(Mel Spigelman)表示:“TB Alliance很自豪能与中国领先的结核病药物制造商红旗制药合作,以确保中国各地的结核病患者都能获得这种治疗。我们致力于通过我们开发的所有的结核病治疗方案,为市场提供一个可负担和可持续的治疗方案。”
红旗制药总经理杨波表示,“红旗制药致力于持续为中国结核患者提供高质量、可负担的治疗用药。很荣幸能与TB Alliance合作,我们与TB Alliance的共同目标是为中国的结核病患者提供最新的治疗。”
本次TB Alliance与红旗制药的合作,是作为三药“BPaL”方案组成部分的pretomanid全球商业化战略的一部分。这项协议的签署,完善了早前TB联盟与Mylan及Maleods制药公司就该治疗方案在其他国家商业化合作。
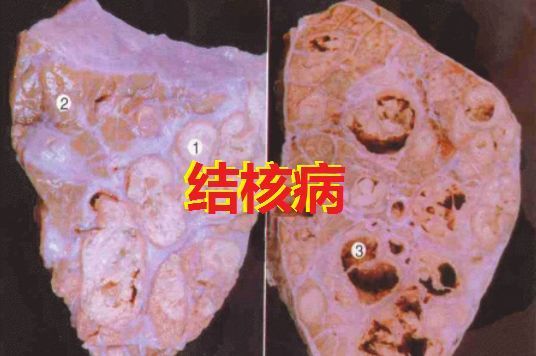
结核病(tuberculosis,TB)是一种全球性疾病,在每个国家都有发现,是导致死亡的首要传染病。所有类型的结核病都必须采用药物联合治疗,对药物最敏感的结核病需要用4种抗结核药物治疗6个月。广泛耐药结核病或治疗不耐受/无应答的耐多药结核病的治疗疗程更长且非常复杂,大多数XDR-TB患者目前需要服用多达8种抗生素(部分需要每日注射)的组合方案治疗18个月或更长时间。根据WHO的报告,在近年来推出治疗耐药结核病的新药之前,广泛耐药结核病(XDR-TB)疗法的成功率约34%,耐多药结核病(MDR-TB)疗法的成功率约55%。
pretomanid是一种新型化合物,于2019年8月获得美国FDA批准,作为三药、六个月全口服方案BPaL的一部分,用于药物不耐受或无应答的XDR-TB或MDR-TB(统称为“高度耐药结核病”)的治疗。
值得一提的是,pretomanid是美国FDA在过去40多年来批准的第三款抗结核新药,同时也是首个由非盈利组织开发的抗结核药物。在美国,FDA已授予Pretomanid优先审查、合格传染病产品(QIDP)、孤儿药资格。
pretomanid是一种新化学实体,属于名为硝基咪唑嗪类化合物。该药已在20项临床试验中单独或与其他抗结核药物联合进行了研究。自从2002年TB Alliance开始开发pretomanid以来,该药已在14个国家对1000多人进行了临床试验。

pretomanid分子结构式(图片来源:Wikipedia)
Pretomanid的新药申请包括了1168例患者的数据,这些患者在19项临床试验中接受了Pretomanid治疗。III期临床研究Nix-TB入组了109例XDR-TB以及药物不耐受或非反应性MDR-TB患者。数据显示,接受BPaL方案治疗6个月并在完成治疗后随访6个月,前107例患者中有95例患者取得了治疗成功——临床感染得到解决、TB痰培养呈阴性。有2例患者的治疗时间延长至9个月。该研究中,报告的不良反应包括肝毒性、骨髓移植、周围神经病变。
Nix-TB研究的首席调查员FrancescaConradie博士此前表示:“直到最近,高度耐药结核感染者的治疗选择和预后都很差。此次批准的这一新的治疗方案,为90%的患者在接受这种短疗程全口服方案完成治疗后6个月达到培养阴性状态提供了希望。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


