抗精神病新药!ALKS3831(奥氮平/samidorphan)在美申请上市,治疗精神分裂症和双相I型障碍
来源:本站原创 2019-11-20 14:55
2019年11月20日/生物谷BIOON/--Alkermes是一家全面整合的爱尔兰生物制药公司,致力于开发治疗中枢神经系统(CNS)疾病和肿瘤的创新药物。该公司拥有多元化的商业产品组合及大量的临床候选产品,用于治疗多种疾病,包括精神分裂症、抑郁症、成瘾、多发性硬化症和肿瘤。近日,该公司宣布,已向美国食品和药物管理局(FDA)提交了ALKS3831(olanzapine/samidorphan)的

2019年11月20日/生物谷BIOON/--Alkermes是一家全面整合的爱尔兰生物制药公司,致力于开发治疗中枢神经系统(CNS)疾病和肿瘤的创新药物。该公司拥有多元化的商业产品组合及大量的临床候选产品,用于治疗多种疾病,包括精神分裂症、抑郁症、成瘾、多发性硬化症和肿瘤。
近日,该公司宣布,已向美国食品和药物管理局(FDA)提交了ALKS3831(olanzapine/samidorphan)的新药申请(NDA),该药是一种新型口服非典型抗精神病药物,每日一次,用于治疗精神分裂症和双相I型障碍。
ALKD3831是由一种新颖的新分子实体samidorphan(新型选择性μ-阿片受体拮抗剂)和一种已上市抗精神病药物奥氮平(olanzapine)制成的一种双层片剂。体重增加和临床相关的代谢问题是非典型抗精神分裂药物常见的副作用。奥氮平是一种有效的抗精神病药物,但临床使用受限于其高发的体重增加。ALKD3831的设计力图在提供奥氮平的强力抗精神病疗效的同时,降低对体重和新陈代谢的副作用,从而提高治疗的安全性。
ALKD3831 NDA中纳入了在精神分裂症患者中开展的ENLIGHTEN临床开发项目数据。该项目包括2项关键III期研究(ENLIGHTEN-1,ENLIGHTEN-2),还包括评估ALKS3831药代动力学和代谢特征以及长期安全性的支持性研究,以及比较ALKS3831和已上市药物Zyprexa(奥氮平)药代动力学(PK)桥接研究。
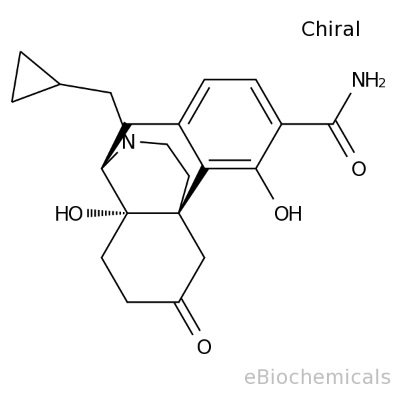
samidorphan分子结构式(图片来源:ebiochemicals.com)
ENLIGHTEN-1是一项为期4周的随机、双盲III期研究,在正经历急性加重的精神分裂症患者中开展,比较了ALKS3831相对于安慰剂的抗精神病疗效、安全性和耐受性。结果显示,研究达到了主要终点:与安慰剂组相比,ALKS3831治疗组阳性和阴性症状量表(PANSS)评分相对基线显示出统计学意义的显著降低。该研究中还纳入了一个奥氮平治疗组,但不是为了比较ALKS3831和奥氮平之间的疗效或安全性。研究数据显示,与安慰剂组相比,奥氮平治疗组在PANSS评分相对基线的变化具有相似的改善。
ENLIGHTEN-2是一项为期6个月的书籍、双盲III期研究,在病情稳定的精神分裂症患者中开展,评估了ALKS3831与安慰剂对体重的影响。结果显示,研究达到了共同主要终点,表明:与奥氮平治疗组相比,ALKS3831治疗组在治疗第6个月时体重从基线开始的平均体重增加百分比较低、在治疗第6个月时体重增加≥10%的患者比例较低。
Alkermes首席医疗官兼药物开发和医疗事务高级副总裁Craig Hopkinson医学博士表示:“抗精神病药物是精神分裂症和双相情感障碍治疗模式的重要组成部分,但对新治疗方法的需求仍未得到满足。ALKS3831 NDA的提交体现了Alkermes致力于开发治疗严重和普遍的中枢神经系统疾病的新疗法,以及我们对精神健康障碍患者的长期奉献精神。我们很高兴提交了这份申请,寻求批准ALKS3831这两种适应症,我们期待着与FDA合作,将这种潜在的新药物带给患者和医疗专业人员。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


